Clear Sky Science · de
Synthese, biologische Bewertung und molekulardocking-Studien von N‑propylsulfonylindol-gebundenen Hydrazincarbothioamiden als selektive Ecto‑5′‑Nucleotidase‑ und NTPDase‑Inhibitoren
Warum diese Forschung für künftige Krebstherapien wichtig ist
Unser Immunsystem patrouilliert ständig auf der Suche nach Krebszellen, doch Tumoren haben raffinierte Methoden entwickelt, diese Abwehrmechanismen auszuschalten. Eine dieser Strategien nutzt chemische Botenstoffe, die aus ATP entstehen, demselben Molekül, das unsere Zellen antreibt. Diese Arbeit beschreibt eine neue Familie kleiner Moleküle, die darauf ausgelegt sind, diesen chemischen Trick zu unterbrechen, mit dem langfristigen Ziel, das Immunsystem dabei zu unterstützen, Tumoren besser zu erkennen und anzugreifen.
Der chemische Schalter, der Immunzellen beruhigt
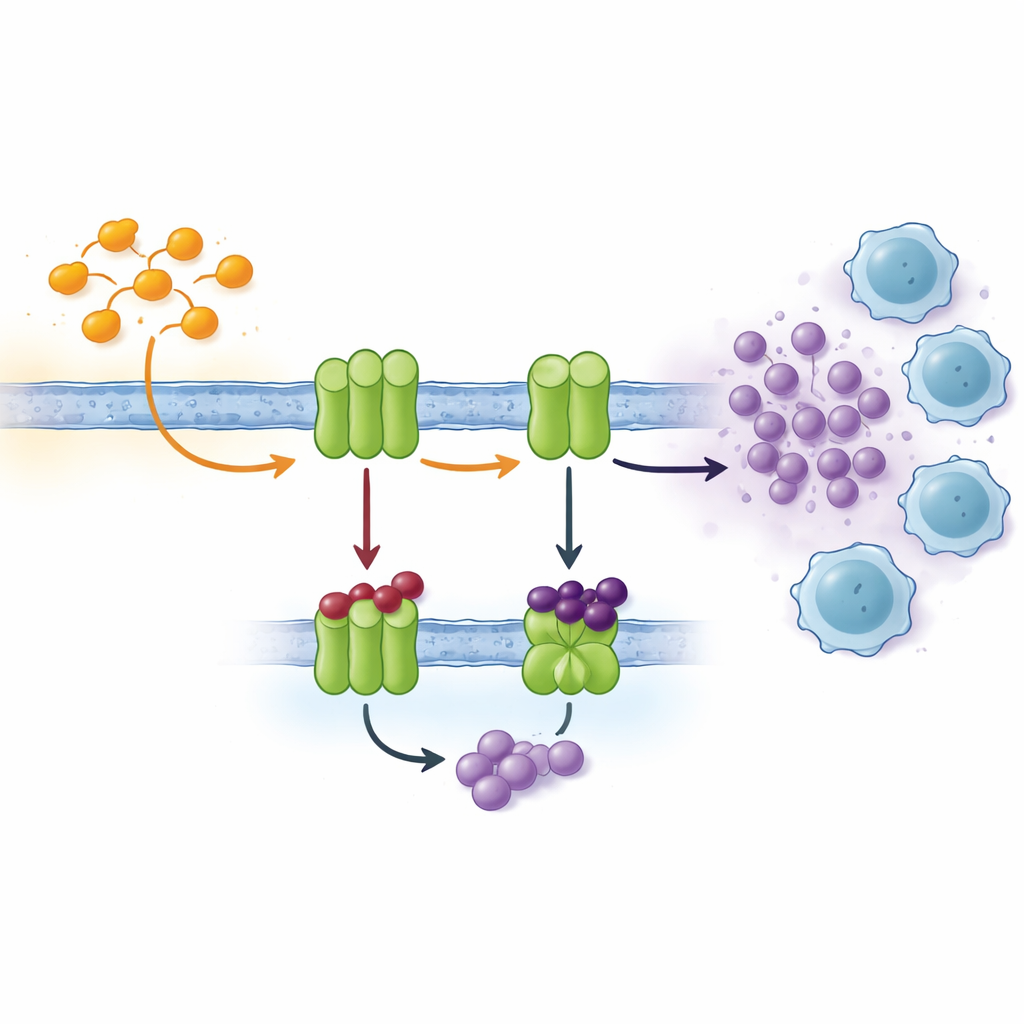
Zellen kommunizieren über viele Signale; ein wichtiger Kanal beruht auf Nukleotiden wie ATP und seinem Abbauprodukt Adenosin. Außerhalb der Zelle wandelt eine Kaskade von Enzymen in der Zellmembran ATP stetig in Adenosin um. Zwei Schlüsselfaktoren, bekannt als CD39 und CD73, sind in sauerstoffarmen Tumorbereichen häufig überexprimiert. Dort wandeln sie das von gestressten oder sterbenden Zellen freigesetzte ATP schnell in Adenosin um, das wie ein chemisches „Beruhigungsmittel" auf benachbarte Immunzellen wirkt. Hohe Adenosinspiegel dämpfen die T‑Zell‑Aktivität, fördern die Bildung von Blutgefäßen und begünstigen die Tumorausbreitung. Das Blockieren der Enzyme, die Adenosin erzeugen, ist daher eine attraktive Strategie in der modernen Krebsimmuntherapie.
Intelligentere Blocker entwerfen mit einem bewährten Ringsystem
Wirkstoffdesigner beginnen oft mit Ringsystemen, die bereits medizinischen Nutzen gezeigt haben. Der Indolring, der in mehreren zugelassenen Krebsmedikamenten vorkommt, ist ein solches Gerüst. Eine weitere nützliche Komponente, Thiosemicarbazon, kann Metalle koordinieren und interagiert stark mit vielen biologischen Zielstrukturen. In dieser Arbeit kombinierten die Forscher diese beiden Motive zu einem hybriden Gerüst und verfeinerten es durch Anbringen unterschiedlicher chemischer Seitenketten, wodurch eine kleine Bibliothek von 22 verwandten Verbindungen entstand. Sie variierten die Position der Thiosemicarbazon‑Einheit am Indolring und die angehängten Seitenketten, um zu untersuchen, wie diese Änderungen die Fähigkeit beeinflussen, CD73 und mehrere verwandte Enzyme der NTPDase‑Familie zu hemmen.
Welche Moleküle welches Enzym treffen
Das Team bestätigte zunächst Struktur und Reinheit aller neuen Moleküle mit gängigen Labortechniken wie Infrarot‑ und Kernspinresonanzspektroskopie, Massenspektrometrie und Hochleistungsflüssigkeitschromatographie. Anschließend bestimmten sie in Reagenzglas‑Assays, wie gut jede Verbindung fünf menschliche Enzyme hemmte: CD73 und vier NTPDase‑Typen (1, 2, 3 und 8). Mehrere Verbindungen blockierten ihre Ziele in niedrigen Mikromolar‑Bereichen und waren damit deutlich wirksamer als häufig verwendete Referenzinhibitoren. Verschiedene chemische Modifikationen des Gerüsts lenkten die Aktivität jeder Verbindung auf bestimmte Enzymtypen. So war beispielsweise das Molekül mit der Bezeichnung 5f besonders wirksam gegen NTPDase2 und NTPDase8, während 5i NTPDase1 bevorzugte. Zwei verwandte Verbindungen, 5n und 5o, stachen durch ihre starke Wirkung auf CD73 und ausgewählte NTPDases hervor und gelten damit als vielversprechende Leitkandidaten.
Ein Blick in die Bindungstasche am Computer
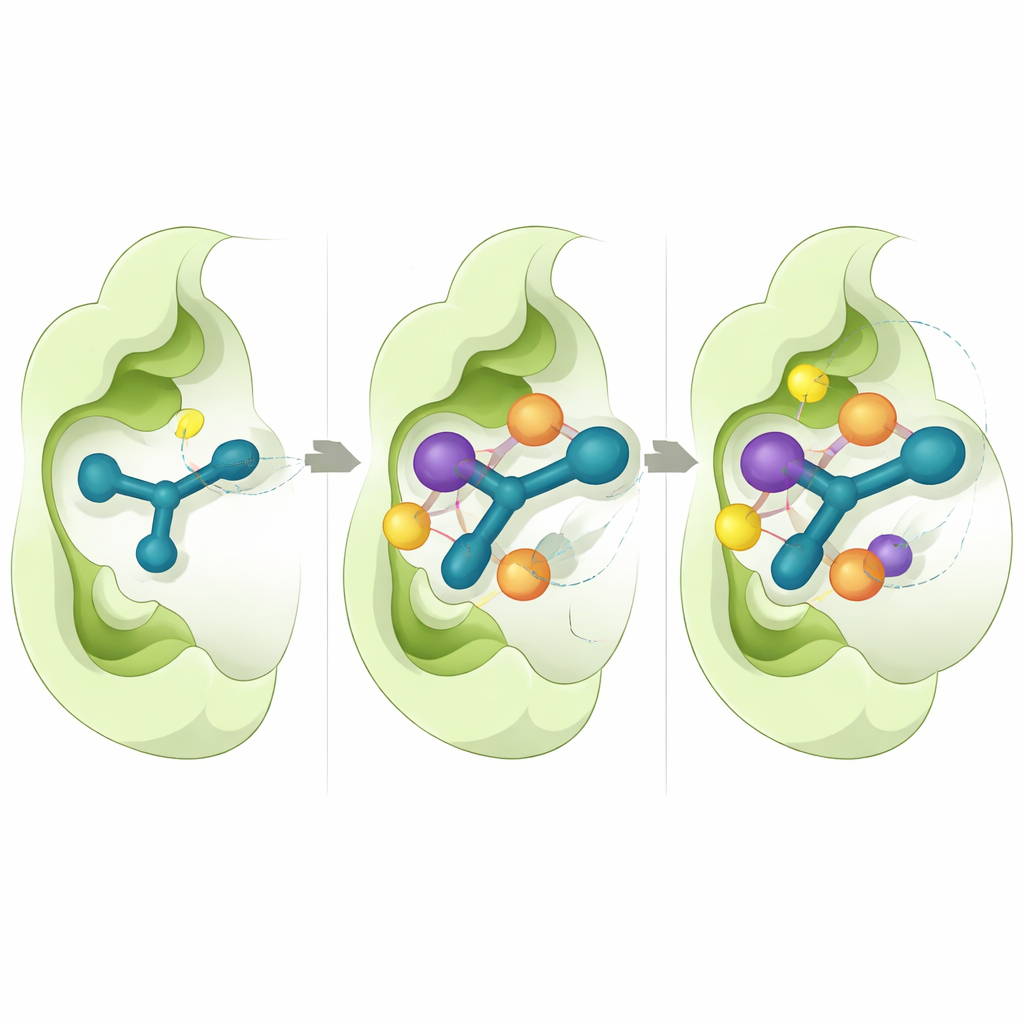
Um zu verstehen, warum manche Moleküle besser wirken als andere, nutzten die Forscher detaillierte Computersimulationen. Sie konzentrierten sich auf CD73, da eine hochauflösende dreidimensionale Struktur dieses Enzyms verfügbar ist. Virtuelle Docking‑Experimente zeigten, dass die aktiven Verbindungen konsistent in die katalytische Tasche des Enzyms gleiten, wobei der Indolring gegen aromatische Aminosäuren stackt und der Thiosemicarbazon‑Abschnitt Wasserstoffbrücken mit Schlüsselrestgruppen bildet. Berechnungen der Bindungsenergie deuteten darauf hin, dass enge hydrophobe Kontakte und van‑der‑Waals‑Kräfte wesentliche Beiträge zur starken Bindung von 5n und 5o leisten. Lange Molekulardynamik‑Simulationen, die die Bewegung der Atome über jeweils eine halbe Mikrosekunde verfolgten, zeigten, dass diese Komplexe stabil bleiben und nur geringe Schwankungen sowohl in der Proteinfaltung als auch in der Lage des Inhibitors über die Zeit auftreten.
Erste Hinweise auf wirkstoffähnliches Verhalten
Neben der Zielhemmung müssen potenzielle Medikamente geeignete pharmakokinetische Eigenschaften aufweisen. Die Autoren sagten daher Absorptions‑, Verteilungs‑ und andere pharmakokinetische Eigenschaften in silico voraus. Die meisten Verbindungen der Serie, insbesondere 5n und 5o, zeigten eine vorteilhafte Balance aus Größe, Löslichkeit und Membranpermeabilität, mit guter vorhergesagter oraler Aufnahme und nur geringen Verletzungen einfacher Faustregeln. Diese Daten, kombiniert mit ihrer starken und selektiven Enzyminhibition und stabiler Bindung in Simulationen, stützen die Sichtweise, 5n und 5o als Ausgangspunkte für weitere Optimierungen und nicht als fertige Medikamentenkandidaten zu betrachten.
Was das für Patienten bedeuten könnte
Wenn Tumoren CD39 und CD73 nutzen, um ihre Umgebung mit Adenosin zu überschwemmen, werden Immunzellen träge und weniger fähig, anzugreifen. Diese Studie stellt eine neue Reihe indolbasierter Moleküle vor, die diesen Weg im Reagenzglas selektiv stören und in Computermodellen vielversprechend abschneiden. Obwohl noch viel Arbeit bevorsteht – einschließlich Tests in Zellen, Tieren und schließlich im Menschen – legen die Ergebnisse nahe, dass dieses chemische Gerüst zu künftigen Arzneimitteln weiterentwickelt werden könnte, die die chemischen „Bremsen“, die Tumoren dem Immunsystem auferlegen, lösen und so bestehende Krebstherapien wirksamer machen könnten.
Zitation: Batool, Z., Dutt, S.M., al-Rashida, M. et al. Synthesis, biological evaluation and molecular docking studies of N-propylsulfonyl indole-linked hydrazinecarbothioamides as selective ecto-5′-nucleotidase and NTPDase inhibitors. Sci Rep 16, 14419 (2026). https://doi.org/10.1038/s41598-026-50728-3
Schlüsselwörter: Inhibition der Ecto‑5‑Nucleotidase, NTPDase‑Inhibitoren, Adenosin‑Signalübertragung, Krebsimmuntherapie, Indol‑Thiosemicarbazone