Clear Sky Science · it
Sintesi, valutazione biologica e studi di docking molecolare di N-propilsulfonil indolo-legati idrazinocarbothioammidi come inibitori selettivi di ecto-5′-nucleotidasi e NTPDasi
Perché questa ricerca conta per i futuri trattamenti contro il cancro
Il nostro sistema immunitario controlla costantemente la presenza di cellule tumorali, ma i tumori hanno evoluto stratagemmi sofisticati per disattivare queste difese. Uno di questi stratagemmi sfrutta messaggeri chimici derivati dall'ATP, la stessa molecola che fornisce energia alle nostre cellule. Questo articolo descrive una nuova famiglia di piccole molecole progettate per interrompere quel trucco chimico, con l'obiettivo a lungo termine di aiutare il sistema immunitario a riconoscere e attaccare meglio i tumori.
L'interruttore chimico che calma le cellule immunitarie
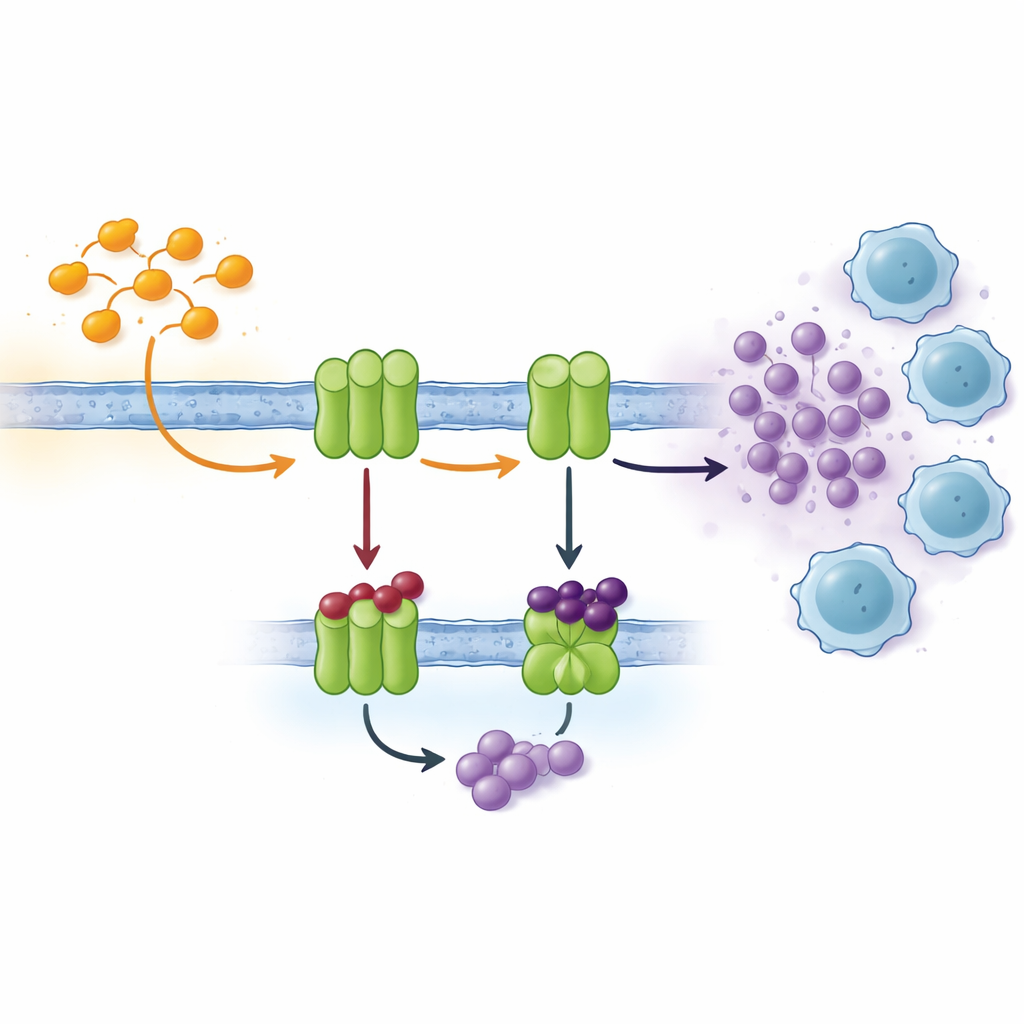
Le cellule comunicano tra loro usando molti segnali, e uno degli assi importanti si basa su nucleotidi come l'ATP e il suo prodotto di degradazione, l'adenosina. All'esterno della cellula, una catena di enzimi localizzati nella membrana cellulare converte progressivamente l'ATP in adenosina. Due attori chiave, noti come CD39 e CD73, sono spesso sovraespressi nei tessuti tumorali poveri di ossigeno. Lì trasformano rapidamente l'ATP rilasciato da cellule stressate o morenti in adenosina, che agisce come una sorta di "tranquillante" chimico sulle cellule immunitarie vicine. Livelli elevati di adenosina smorzano l'attività delle cellule T, favoriscono la crescita dei vasi sanguigni e facilitano la diffusione tumorale. Bloccare gli enzimi che producono adenosina è quindi una strategia interessante nell'immunoterapia oncologica moderna.
Progettare inibitori più intelligenti usando un sistema ad anello collaudato
I progettisti di farmaci spesso partono da sistemi ad anello che hanno già dimostrato valore clinico. L'anello indolico, presente in diversi farmaci anticancro approvati, è una di queste strutture. Un altro componente utile, il tiossemicarbazone, può legare metalli e interagire fortemente con molti target biologici. In questo lavoro i ricercatori hanno combinato questi due motivi in uno scaffold ibrido unico e lo hanno messo a punto aggiungendo diversi gruppi chimici, creando una piccola libreria di 22 composti correlati. Hanno variato la posizione dell'unità tiossemicarbazone sull'anello indolico e i gruppi laterali attaccati per vedere come questi cambiamenti influenzassero la capacità di inibire CD73 e diversi enzimi correlati chiamati NTPDasi.
Testare quali molecole colpiscono quali enzimi
Il team ha prima confermato la struttura e la purezza di tutte le nuove molecole usando tecniche di laboratorio standard come spettroscopia infrarossa e di risonanza magnetica nucleare, spettrometria di massa e cromatografia liquida ad alte prestazioni. Hanno quindi misurato quanto ciascun composto rallentasse cinque enzimi umani in saggi in provetta: CD73 e quattro tipi di NTPDasi (1, 2, 3 e 8). Diversi membri della serie hanno bloccato i loro target a concentrazioni micromolari basse, ossia erano molto più potenti rispetto agli inibitori di riferimento comunemente usati. Diverse decorazioni chimiche sullo scaffold hanno orientato ogni composto verso tipi enzimatici specifici. Per esempio, una molecola contrassegnata 5f è risultata particolarmente efficace contro NTPDase2 e NTPDase8, mentre 5i favoriva NTPDase1. Due molecole correlate, 5n e 5o, si sono distinte per la loro forte attività su CD73 e su NTPDasi selezionate, segnalando che sono promettenti candidati guida.
Osservare il sito di legame al computer
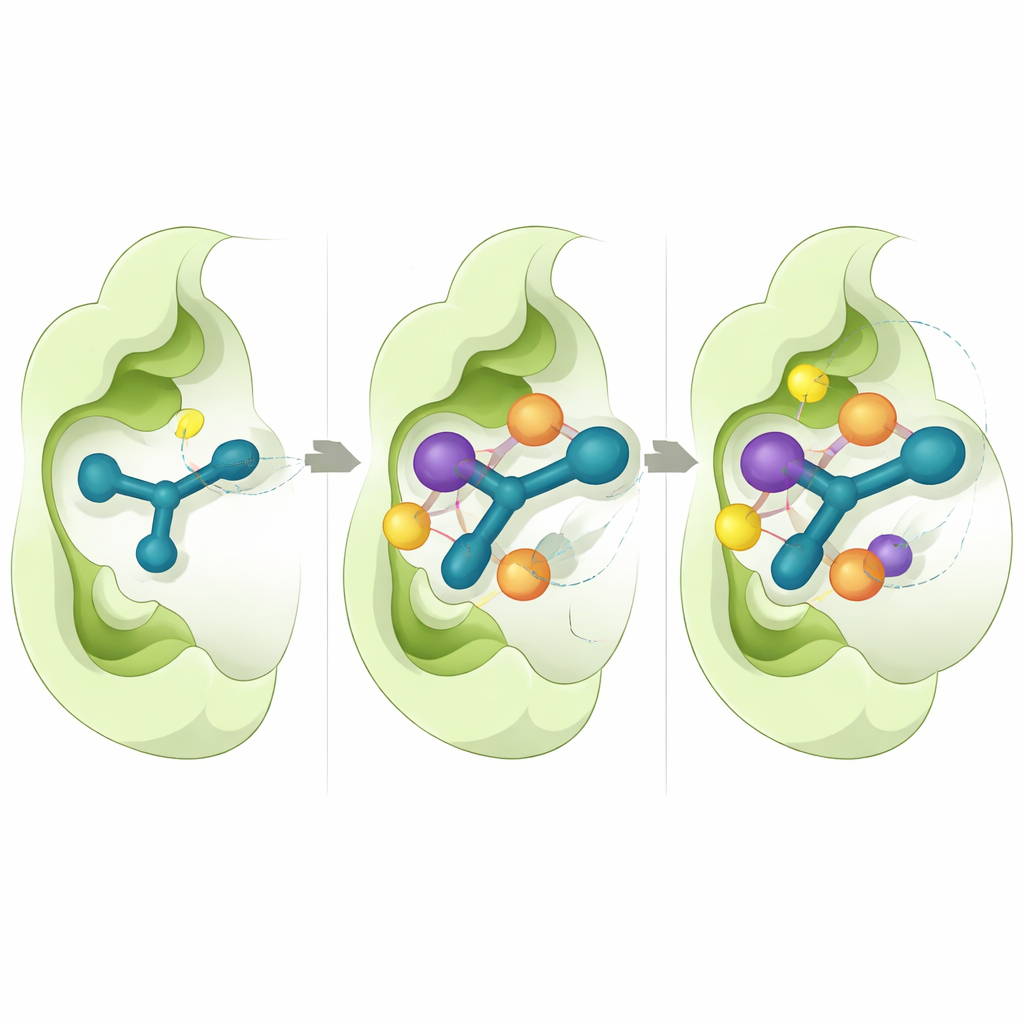
Per capire perché alcune molecole funzionassero meglio di altre, i ricercatori hanno utilizzato simulazioni al computer dettagliate. Si sono concentrati su CD73, perché è disponibile una struttura tridimensionale ad alta risoluzione di questo enzima. Esperimenti di docking virtuale hanno mostrato che i composti attivi si inseriscono nella tasca catalitica dell'enzima in modo coerente, dove l'anello indolico si sovrappone ad amminoacidi aromatici e il segmento tiossemicarbazone forma legami a idrogeno con residui chiave. I calcoli dell'energia di legame hanno suggerito che contatti idrofobici stretti e forze di van der Waals contribuiscono in modo rilevante al forte legame osservato per 5n e 5o. Lunghe simulazioni di dinamica molecolare, ciascuna calcolata per il moto degli atomi per mezzo microsecondo, hanno indicato che questi complessi rimangono stabili, con solo piccole fluttuazioni sia nella proteina sia nella posizione dell'inibitore nel tempo.
Primi indizi di comportamento simile a un farmaco
Oltre a colpire i loro target, i potenziali farmaci devono muoversi nel corpo in modo adeguato. Gli autori hanno quindi previsto in silico proprietà di assorbimento, distribuzione e altre proprietà farmacocinetiche. La maggior parte dei composti della serie, e in particolare 5n e 5o, ha mostrato un equilibrio favorevole di dimensione, solubilità e permeabilità della membrana, con una buona previsione di assorbimento orale e solo lievi violazioni delle regole empiriche. Questi dati, combinati con la loro forte e selettiva inibizione enzimatica e il legame stabile nelle simulazioni, supportano l'idea di considerare 5n e 5o come punti di partenza per ulteriori ottimizzazioni piuttosto che come candidati farmaco definitivi.
Cosa potrebbe significare per i pazienti
Quando i tumori sfruttano CD39 e CD73 per inondare l'ambiente circostante di adenosina, le cellule immunitarie diventano lente e meno capaci di attaccare. Questo studio introduce un nuovo insieme di molecole a base indolica che interferiscono selettivamente con quella via in provetta e mostrano comportamenti incoraggianti nei modelli al computer. Pur restando molto lavoro da fare — inclusi test su cellule, animali e infine sull'uomo — i risultati suggeriscono che questo scaffold chimico potrebbe essere modellato in futuri farmaci capaci di sollevare i "freni" chimici che i tumori applicano sul sistema immunitario, potenzialmente rendendo più efficaci le terapie oncologiche esistenti.
Citazione: Batool, Z., Dutt, S.M., al-Rashida, M. et al. Synthesis, biological evaluation and molecular docking studies of N-propylsulfonyl indole-linked hydrazinecarbothioamides as selective ecto-5′-nucleotidase and NTPDase inhibitors. Sci Rep 16, 14419 (2026). https://doi.org/10.1038/s41598-026-50728-3
Parole chiave: inibizione dell'ecto-5-nucleotidasi, inibitori delle NTPDasi, segnalazione dell'adenosina, immunoterapia del cancro, tiossemicarbazoni indolici