Clear Sky Science · fr
Synthèse, évaluation biologique et études de docking moléculaire de N-propylsulfonyl indole-liés hydrazinecarbothioamides en tant qu’inhibiteurs sélectifs de l’ecto-5′-nucléotidase et des NTPDases
Pourquoi cette recherche est importante pour les traitements futurs du cancer
Notre système immunitaire surveille en permanence la présence de cellules cancéreuses, mais les tumeurs ont développé des stratagèmes ingénieux pour désactiver ces défenses. L’un de ces stratagèmes utilise des messagers chimiques dérivés de l’ATP, la même molécule qui alimente nos cellules. Cet article décrit une nouvelle famille de petites molécules conçues pour interrompre ce « tour de passe‑passe » chimique, dans l’objectif à long terme d’aider le système immunitaire à mieux reconnaître et attaquer les tumeurs.
Le commutateur chimique qui calme les cellules immunitaires
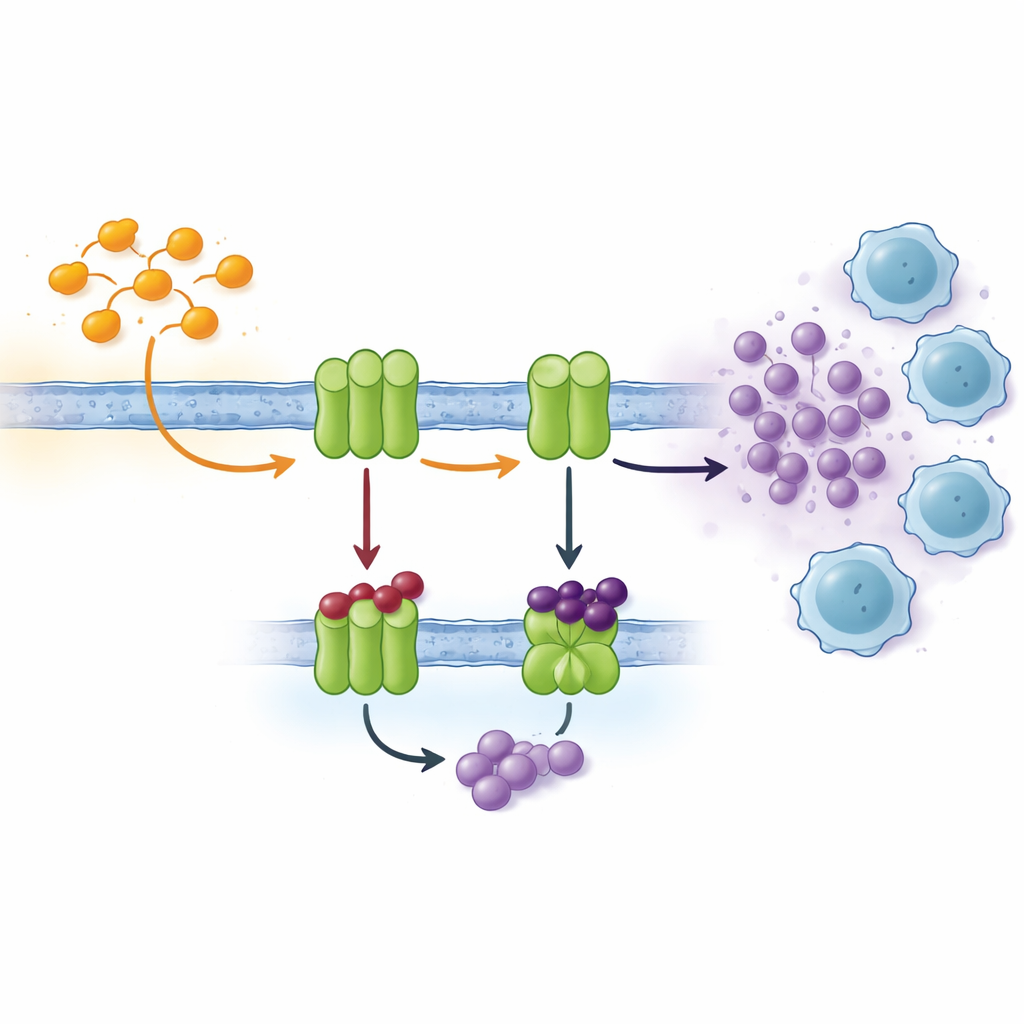
Les cellules communiquent entre elles via de nombreux signaux, et une voie importante repose sur des nucléotides comme l’ATP et son produit de dégradation, l’adénosine. À l’extérieur de la cellule, une chaîne d’enzymes ancrées dans la membrane transforme progressivement l’ATP en adénosine. Deux acteurs clés, connus sous les noms de CD39 et CD73, sont souvent surexprimés dans les tissus tumoraux pauvres en oxygène. Là, ils convertissent rapidement l’ATP libéré par des cellules stressées ou mourantes en adénosine, qui agit comme un « tranquillisant » chimique sur les cellules immunitaires voisines. Des niveaux élevés d’adénosine réduisent l’activité des lymphocytes T, favorisent la formation de vaisseaux sanguins et aident les tumeurs à se disséminer. Bloquer les enzymes qui créent l’adénosine constitue donc une stratégie attrayante en immunothérapie moderne du cancer.
Concevoir des bloqueurs plus intelligents en utilisant un noyau éprouvé
Les concepteurs de médicaments partent souvent de systèmes annulaires déjà reconnus pour leur valeur médicale. L’indole, présent dans plusieurs médicaments anticancéreux approuvés, en est un exemple. Un autre composant utile, la thiosemicarbazone, peut complexer des métaux et interagit fortement avec de nombreuses cibles biologiques. Dans ce travail, les chercheurs ont combiné ces deux motifs en un seul échafaudage hybride et l’ont affiné en greffant différents groupes chimiques, créant une petite bibliothèque de 22 composés apparentés. Ils ont modifié la position de l’unité thiosemicarbazone sur l’anneau indolique et varié les groupes latéraux pour observer comment ces changements affectaient la capacité à inhiber CD73 et plusieurs enzymes apparentées appelées NTPDases.
Tester quels composés ciblent quelles enzymes
L’équipe a d’abord confirmé la structure et la pureté de toutes les nouvelles molécules à l’aide de techniques de laboratoire standard telles que la spectroscopie infrarouge et la résonance magnétique nucléaire, la spectrométrie de masse et la chromatographie liquide haute performance. Ils ont ensuite mesuré l’efficacité de chaque composé à ralentir cinq enzymes humaines dans des essais in vitro : CD73 et quatre types de NTPDases (1, 2, 3 et 8). Plusieurs membres de la série ont bloqué leurs cibles à de faibles concentrations micromolaires, ce qui signifie qu’ils étaient beaucoup plus puissants que des inhibiteurs de référence couramment utilisés. Différentes décorations chimiques de l’échafaudage ont orienté chaque composé vers des types d’enzymes particuliers. Par exemple, une molécule désignée 5f était particulièrement efficace contre NTPDase2 et NTPDase8, tandis que 5i favorisait NTPDase1. Deux molécules apparentées, 5n et 5o, se sont distinguées par leur forte activité sur CD73 et certaines NTPDases sélectionnées, les identifiant comme des candidats prometteurs.
Examiner la poche de liaison par ordinateur
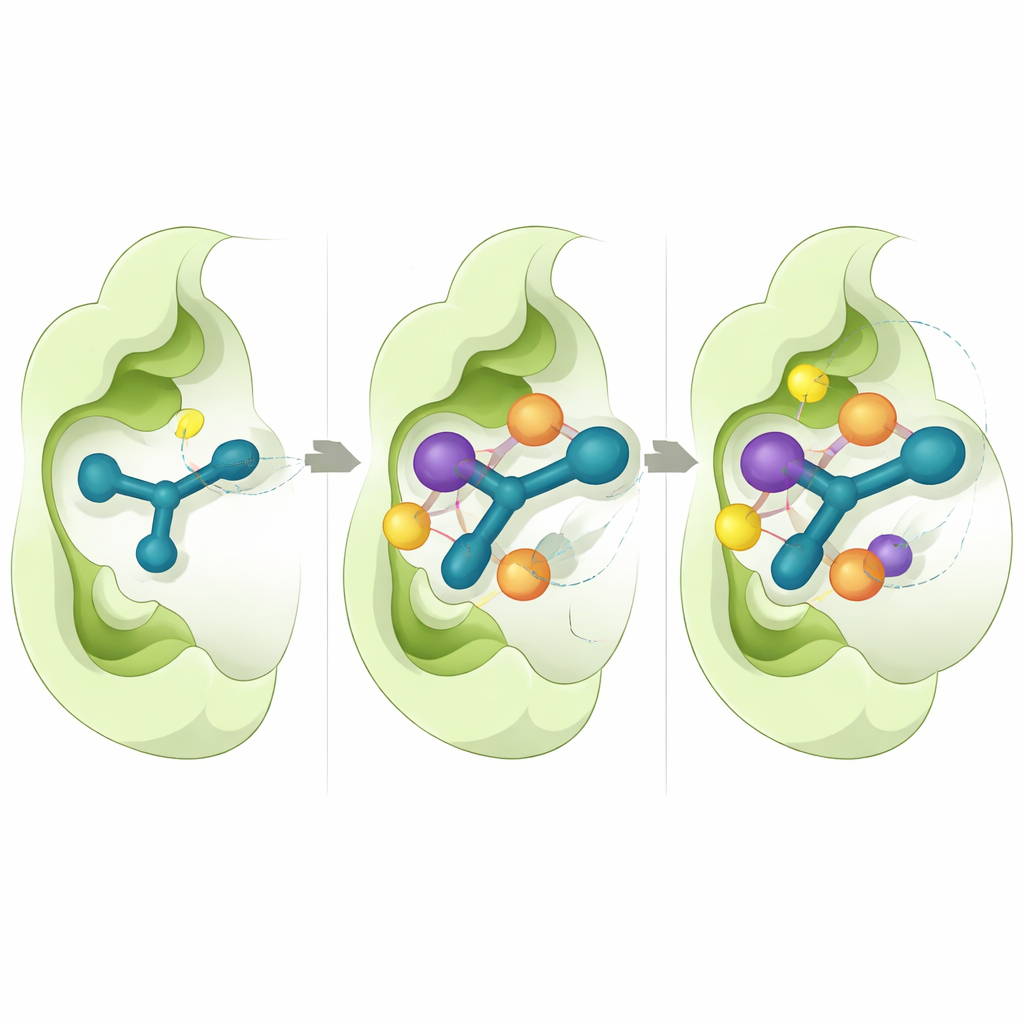
Pour comprendre pourquoi certains composés fonctionnaient mieux que d’autres, les chercheurs ont utilisé des simulations informatiques détaillées. Ils se sont concentrés sur CD73, car une structure tridimensionnelle haute résolution de cette enzyme est disponible. Des expériences de docking virtuel ont montré que les composés actifs s’insèrent de façon cohérente dans la poche catalytique de l’enzyme, où l’anneau indolique s’empile contre des acides aminés aromatiques et le segment thiosemicarbazone établit des liaisons hydrogène avec des résidus clés. Les calculs d’énergie de liaison ont suggéré que des contacts hydrophobes étroits et les forces de van der Waals contribuent majoritairement à la forte affinité observée pour 5n et 5o. De longues simulations de dynamique moléculaire, chacune suivant le mouvement des atomes sur une demi‑microseconde, ont indiqué que ces complexes restent stables, avec seulement de petites fluctuations tant du côté de la protéine que de l’inhibiteur au fil du temps.
Premiers indices d’un comportement de type médicamenteux
Au‑delà de l’inhibition des cibles, les candidats‑médicaments doivent se déplacer dans l’organisme de manière adaptée. Les auteurs ont donc prédit in silico les propriétés d’absorption, de distribution et d’autres paramètres pharmacocinétiques. La plupart des composés de la série, et en particulier 5n et 5o, ont montré un bon équilibre de taille, de solubilité et de perméabilité membranaire, avec une absorption orale prédite favorable et seulement de faibles violations des règles empiriques. Ces données, combinées à leur inhibition enzymatique forte et sélective et à une liaison stable dans les simulations, soutiennent l’idée que 5n et 5o constituent des points de départ pour une optimisation ultérieure plutôt que des candidats‑médicaments définitifs.
Ce que cela pourrait signifier pour les patients
Lorsque les tumeurs utilisent CD39 et CD73 pour inonder leur environnement d’adénosine, les cellules immunitaires deviennent léthargiques et moins aptes à attaquer. Cette étude introduit un nouvel ensemble de molécules à base d’indole qui interfèrent sélectivement avec cette voie in vitro et se comportent de manière encourageante dans les modèles informatiques. Bien qu’il reste beaucoup à faire — y compris des essais cellulaires, des études animales et, finalement, des essais cliniques — les résultats suggèrent que cet échafaudage chimique pourrait être transformé en futurs médicaments aidant à lever les « freins » chimiques que posent les tumeurs sur le système immunitaire, ce qui pourrait rendre les thérapies anticancéreuses existantes plus efficaces.
Citation: Batool, Z., Dutt, S.M., al-Rashida, M. et al. Synthesis, biological evaluation and molecular docking studies of N-propylsulfonyl indole-linked hydrazinecarbothioamides as selective ecto-5′-nucleotidase and NTPDase inhibitors. Sci Rep 16, 14419 (2026). https://doi.org/10.1038/s41598-026-50728-3
Mots-clés: inhibition de l’ecto-5‑nucléotidase, inhibiteurs des NTPDases, signalisation adénosinergique, immunothérapie du cancer, thiosemicarbazones indoliques