Clear Sky Science · ja
選択的ecto-5′-ヌクレオチダーゼおよびNTPDase阻害剤としてのN-プロピルスルホニルインドール連結ヒドラジンカルボチオアミドの合成、生物学的評価および分子ドッキング研究
将来のがん治療にとってこの研究が重要な理由
私たちの免疫系は常にがん細胞を見張っていますが、腫瘍はその防御を無力化する巧妙な手段を進化させてきました。その一つは、細胞のエネルギー分子であるATPから作られる化学伝達物質を使う方法です。本論文は、その化学的トリックを遮断するよう設計された新しい小分子群を記述しており、長期的には免疫系が腫瘍をよりよく認識し攻撃できるようにすることを目的としています。
免疫細胞を鎮める化学的スイッチ
細胞は多くの信号を用いて互いに通信しており、その重要な経路の一つがATPやその分解産物であるアデノシンのようなヌクレオチドに基づいています。細胞外では、膜上にある一連の酵素がATPをアデノシンへと着実に変換します。CD39およびCD73として知られる二つの主要な酵素は、低酸素の腫瘍組織で過剰に発現することが多く、そこでストレスや死を迎える細胞から放出されたATPを迅速にアデノシンに変換します。アデノシンは近傍の免疫細胞に対して化学的な「鎮静剤」のように働き、高アデノシン濃度はT細胞の活性を抑制し、血管新生を促し、腫瘍の浸潤を助長します。したがって、アデノシンを生み出す酵素を阻害することは、現代のがん免疫療法において魅力的な戦略です。
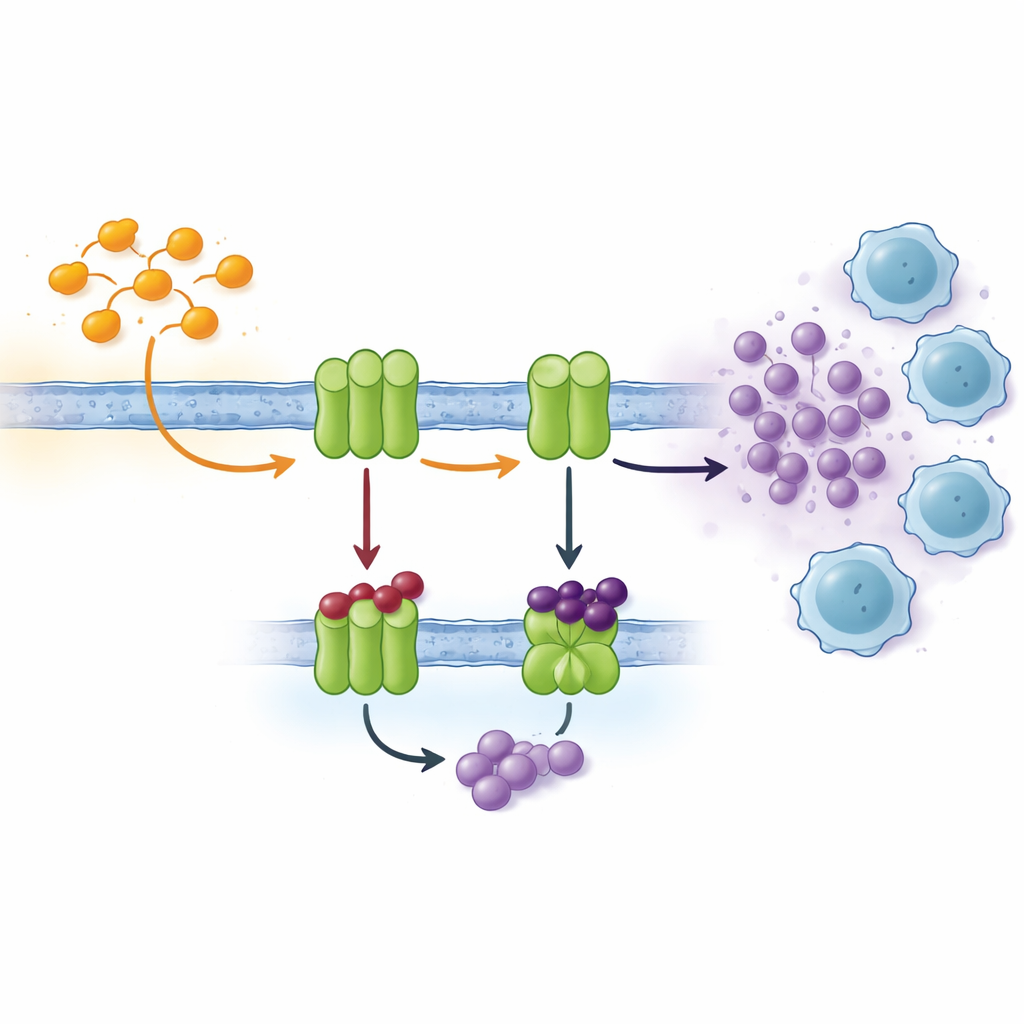
実績のある環状骨格を用いた巧妙な阻害剤の設計
薬剤設計者はしばしば、既に医療上の価値が示されている環状構造を出発点にします。いくつかの承認済み抗がん薬に含まれるインドール環はその一例です。もう一つ有用な構成要素であるチオセミカルバゾンは金属と配位し、多くの生体標的と強く相互作用します。本研究では、研究者たちはこれら二つのモチーフを単一のハイブリッド骨格に結合し、さまざまな化学基を付加して微調整することで、22の関連化合物からなる小さなライブラリを作成しました。インドール環のどの位置にチオセミカルバゾン単位を配置するかを変え、付加する側鎖を変えることで、CD73およびNTPDaseと呼ばれるいくつかの関連酵素を阻害する能力にどのような影響があるかを検討しました。
どの分子がどの酵素に効くかの検証
まず、チームは赤外分光法、核磁気共鳴分光法、質量分析、高速液体クロマトグラフィーなどの標準的な実験手法を用いて、すべての新規分子の構造と純度を確認しました。次に、各化合物が試験管内アッセイでどれほど五つのヒト酵素(CD73および四種のNTPDase:1、2、3、8)の活性を遅らせるかを測定しました。シリーズ中のいくつかの化合物は低マイクロモル濃度で標的を阻害し、一般に用いられる参照阻害剤よりもはるかに強力でした。骨格に施した化学的置換により、各化合物は特定の酵素タイプへと選択性を示しました。例えば、化合物5fは特にNTPDase2およびNTPDase8に有効であり、5iはNTPDase1を好む傾向がありました。5nおよび5oという二つの関連化合物は、CD73および選択的なNTPDaseに対して強い作用を示し、有望なリード候補として特に注目されました。
コンピュータで結合ポケットを覗く
なぜある分子が他よりよく働くのかを理解するために、研究者たちは詳細なコンピュータシミュレーションを用いました。解析対象はCD73に絞られました。これはこの酵素の高分解能三次元構造が利用可能であったためです。バーチャルドッキング実験は、活性化合物が酵素の触媒ポケットに一貫した形で入り込み、インドール環が芳香族アミノ酸と積層し、チオセミカルバゾン部分が重要残基と水素結合を形成することを示しました。結合エネルギーの計算は、緊密な疎水性接触とファンデルワールス力が5nおよび5oで見られる強い結合に主要な寄与をしていることを示唆しました。原子運動を数十万分の一秒(各シミュレーションは0.5マイクロ秒に相当する長い分子動力学)にわたって追跡する長時間の分子動力学シミュレーションは、これらの複合体が安定であり、タンパク質および阻害剤の位置にわずかな変動しか生じないことを示しました。
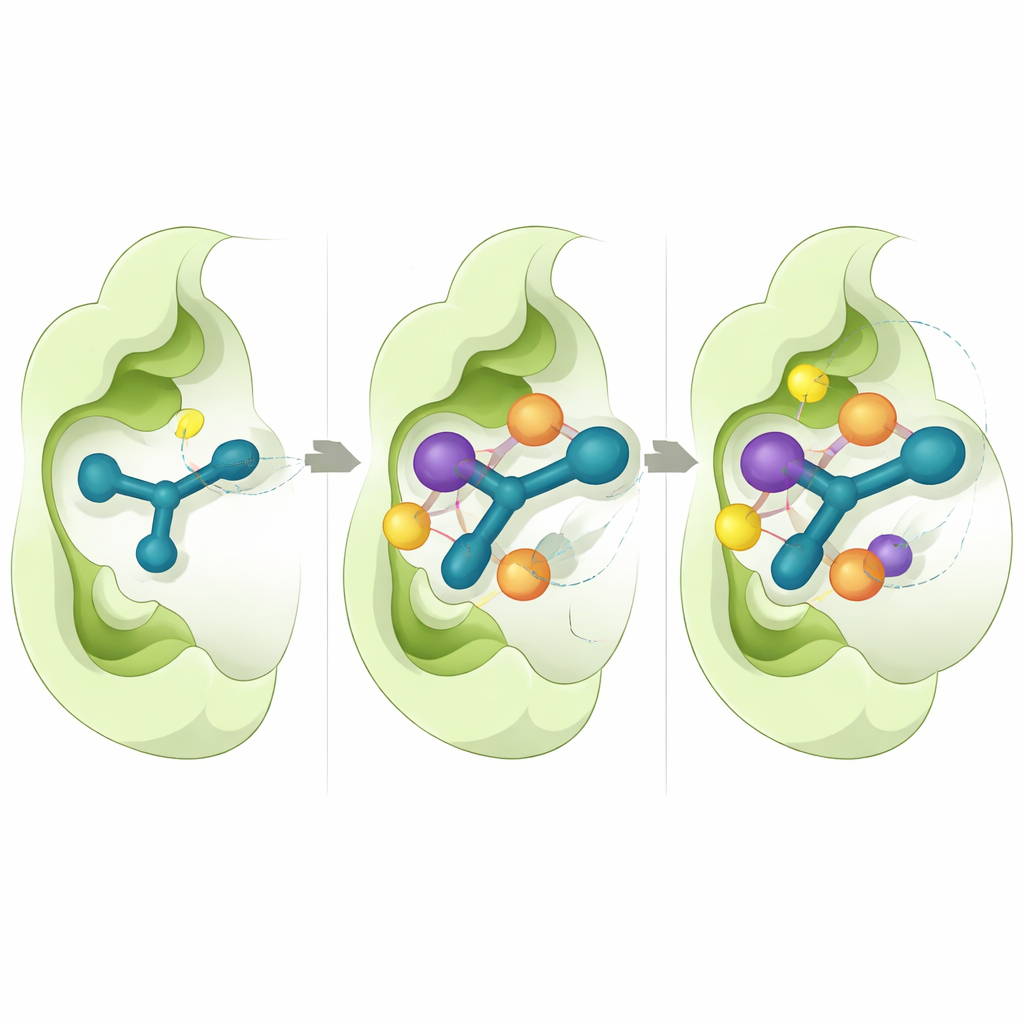
薬物らしい挙動の初期の兆候
標的を阻害するだけでなく、候補薬は適切に体内を移動できなければなりません。したがって著者らは吸収、分布およびその他の薬物動態特性をインシリコで予測しました。このシリーズの大部分の化合物、特に5nおよび5oは、サイズ、溶解性、膜透過性のバランスが良好で、経口吸収の予測も良く、定性的なルールに対する違反も少数にとどまりました。これらのデータは、強力かつ選択的な酵素阻害とシミュレーションでの安定した結合と相まって、5nおよび5oを完成した薬剤候補というよりはさらなる最適化の出発点と見なすことを支持します。
患者にとって意味するところ
腫瘍がCD39およびCD73を利用して周囲をアデノシンで満たすと、免疫細胞は鈍くなり攻撃力が低下します。本研究は、試験管内でその経路を選択的に妨げ、コンピュータモデルでも有望な挙動を示す新しいインドール系分子群を紹介します。細胞、動物、最終的には人における試験など多くの作業が残されているものの、これらの化学骨格は腫瘍が免疫系にかける化学的な「ブレーキ」を解除する将来の医薬品へと形作られる可能性があり、既存のがん治療をより効果的にする手助けとなることが示唆されます。
引用: Batool, Z., Dutt, S.M., al-Rashida, M. et al. Synthesis, biological evaluation and molecular docking studies of N-propylsulfonyl indole-linked hydrazinecarbothioamides as selective ecto-5′-nucleotidase and NTPDase inhibitors. Sci Rep 16, 14419 (2026). https://doi.org/10.1038/s41598-026-50728-3
キーワード: ecto-5-ヌクレオチダーゼ阻害, NTPDase阻害剤, アデノシンシグナル伝達, がん免疫療法, インドールチオセミカルバゾン