Clear Sky Science · es
Síntesis, evaluación biológica y estudios de acoplamiento molecular de hidrazincarbotiamidas N-propilsulfonil indol-enlazadas como inhibidores selectivos de ecto-5′-nucleotidasa y NTPDasa
Por qué esta investigación importa para los tratamientos oncológicos futuros
Nuestro sistema inmunitario vigila continuamente las células cancerosas, pero los tumores han desarrollado artimañas para desactivar esas defensas. Una de esas estrategias utiliza mensajeros químicos derivadas del ATP, la misma molécula que alimenta nuestras células. Este artículo describe una nueva familia de pequeñas moléculas diseñadas para interrumpir ese truco químico, con el objetivo a largo plazo de ayudar al sistema inmunitario a reconocer y atacar mejor a los tumores.
El interruptor químico que calma a las células inmunitarias
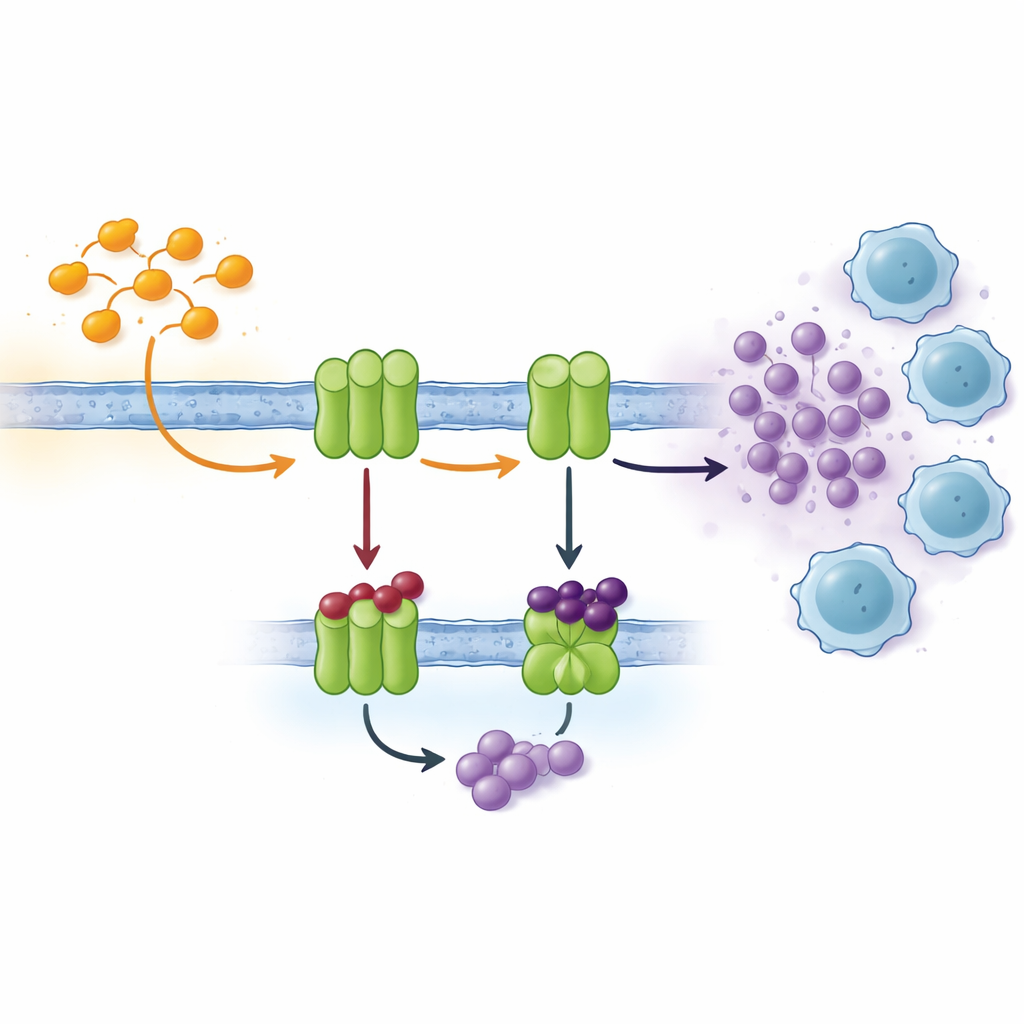
Las células se comunican mediante muchos tipos de señales, y una vía importante se basa en nucleótidos como el ATP y su producto de degradación, la adenosina. En el exterior celular, una cadena de enzimas ancladas en la membrana convierte continuamente el ATP en adenosina. Dos protagonistas clave, conocidas como CD39 y CD73, suelen sobreexpresarse en tejidos tumorales pobres en oxígeno. Allí, transforman rápidamente el ATP liberado por células estresadas o moribundas en adenosina, que actúa como un “tranquilizante” químico sobre las células inmunitarias cercanas. Niveles altos de adenosina apagan la actividad de los linfocitos T, promueven la formación de vasos sanguíneos y facilitan la diseminación tumoral. Bloquear las enzimas que generan adenosina es, por tanto, una estrategia atractiva en la inmunoterapia oncológica moderna.
Diseñar inhibidores más inteligentes a partir de un sistema de anillo probado
Los diseñadores de fármacos a menudo parten de sistemas de anillo que ya han demostrado valor terapéutico. El anillo de indol, presente en varios fármacos anticancerígenos aprobados, es una de esas estructuras. Otro componente útil, la tiosemicarbazona, puede quelar metales e interaccionar fuertemente con múltiples dianas biológicas. En este trabajo, los investigadores combinaron estos dos motivos en un solo andamiaje híbrido y lo afinaron mediante la adición de distintos grupos químicos, creando una pequeña biblioteca de 22 compuestos relacionados. Variaron la posición en el anillo de indol donde se sitúa la unidad de tiosemicarbazona y modificaron los grupos laterales para ver cómo afectaban a la capacidad de bloquear CD73 y varias enzimas relacionadas llamadas NTPDasas.
Probar qué moléculas afectan a cada enzima
El equipo confirmó primero la estructura y pureza de todos los nuevos compuestos mediante técnicas estándar de laboratorio, como espectroscopía infrarroja y de resonance magnética nuclear, espectrometría de masas y cromatografía líquida de alta resolución. A continuación midieron la capacidad de cada compuesto para ralentizar cinco enzimas humanas en ensayos in vitro: CD73 y cuatro tipos de NTPDasa (1, 2, 3 y 8). Varios miembros de la serie inhibieron sus dianas a concentraciones micromolares bajas, lo que significa que eran mucho más potentes que los inhibidores de referencia comúnmente usados. Diferentes decoraciones químicas del andamiaje dirigieron cada compuesto hacia tipos enzimáticos concretos. Por ejemplo, una molécula marcada como 5f fue especialmente eficaz contra NTPDasa2 y NTPDasa8, mientras que 5i mostró preferencia por NTPDasa1. Dos compuestos relacionados, 5n y 5o, destacaron por su fuerte acción sobre CD73 y ciertas NTPDasas, lo que los señala como candidatos líderes especialmente prometedores.
Examinar el bolsillo de unión en el ordenador
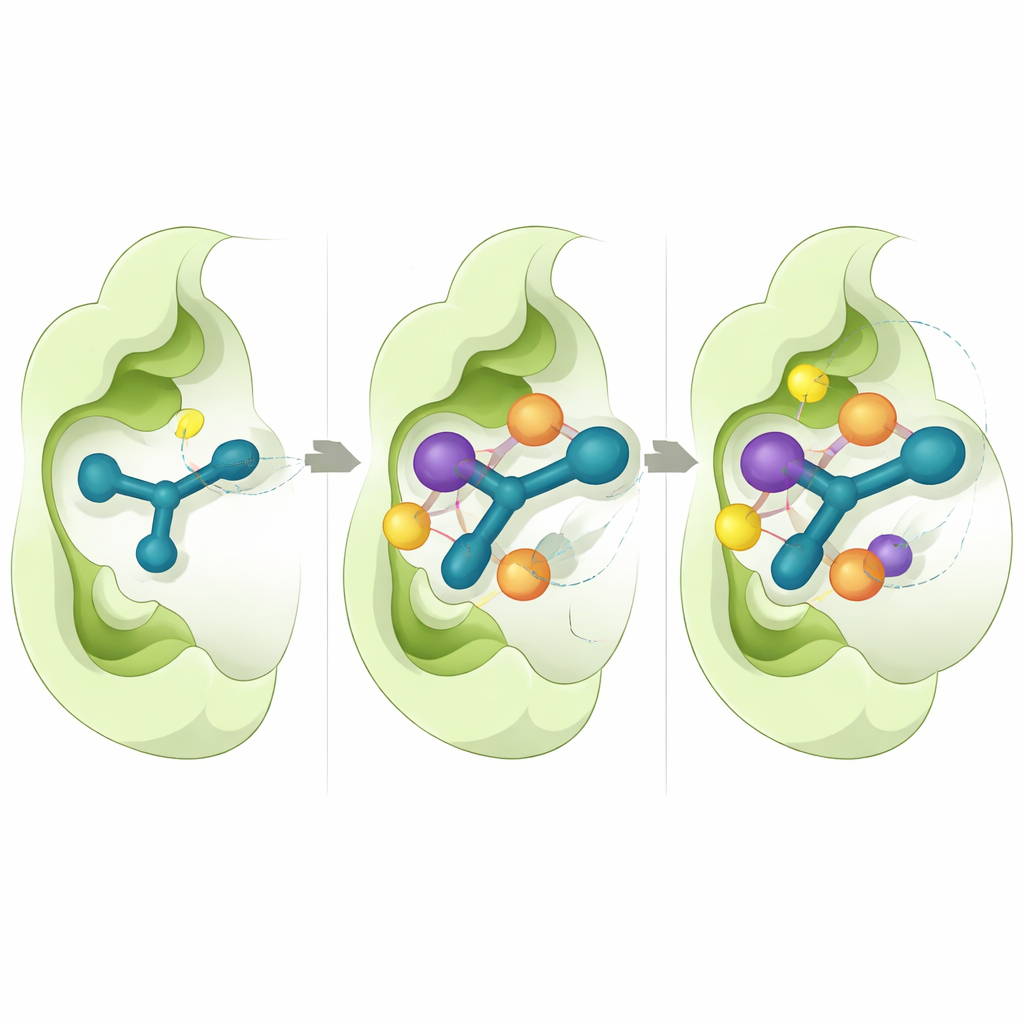
Para entender por qué algunas moléculas funcionaban mejor que otras, los investigadores emplearon simulaciones por ordenador detalladas. Se centraron en CD73, porque existe una estructura tridimensional de alta resolución de esta enzima. Experimentos virtuales de acoplamiento mostraron que los compuestos activos encajan en el bolsillo catalítico de la enzima de manera consistente: el anillo de indol se apila contra aminoácidos aromáticos y el fragmento de tiosemicarbazona forma enlaces de hidrógeno con residuos clave. Los cálculos de energía de unión sugirieron que contactos hidrofóbicos ajustados y fuerzas de van der Waals son contribuyentes importantes a la fuerte afinidad observada para 5n y 5o. Simulaciones de dinámica molecular prolongadas, cada una siguiendo el movimiento de los átomos durante medio microsegundo, indicaron que estos complejos permanecen estables, con fluctuaciones pequeñas tanto en la proteína como en la posición del inhibidor a lo largo del tiempo.
Primeros indicios de comportamiento tipo fármaco
Más allá de inhibir sus dianas, los candidatos a fármaco deben desplazarse por el organismo de manera adecuada. Los autores, por tanto, predijeron in silico propiedades de absorción, distribución y otras farmacocinéticas. La mayoría de los compuestos de la serie, y en especial 5n y 5o, mostraron un equilibrio favorable de tamaño, solubilidad y permeabilidad de membrana, con buena absorción oral predicha y solo violaciones menores de las reglas empíricas. Estos datos, combinados con su inhibición enzimática potente y selectiva y la unión estable en las simulaciones, respaldan considerar a 5n y 5o como puntos de partida para una mayor optimización más que como candidatos farmacológicos definitivos.
Qué podría significar esto para los pacientes
Cuando los tumores emplean CD39 y CD73 para inundar su entorno con adenosina, las células inmunitarias se vuelven lentas y menos capaces de atacar. Este estudio presenta un nuevo conjunto de moléculas basadas en indol que interfieren selectivamente con esa vía en ensayos in vitro y muestran un comportamiento alentador en modelos computacionales. Aunque queda mucho trabajo por delante —incluidas pruebas en células, animales y, finalmente, en humanos— los hallazgos sugieren que este andamiaje químico podría transformarse en futuros medicamentos que ayuden a levantar los “frenos” químicos que los tumores imponen sobre el sistema inmunitario, potencialmente haciendo que las terapias oncológicas existentes sean más eficaces.
Cita: Batool, Z., Dutt, S.M., al-Rashida, M. et al. Synthesis, biological evaluation and molecular docking studies of N-propylsulfonyl indole-linked hydrazinecarbothioamides as selective ecto-5′-nucleotidase and NTPDase inhibitors. Sci Rep 16, 14419 (2026). https://doi.org/10.1038/s41598-026-50728-3
Palabras clave: inhibición de la ecto-5-nucleotidasa, inhibidores de NTPDasa, señalización de adenosina, inmunoterapia contra el cáncer, tiosemicarbazonas de indol