Clear Sky Science · pt
Síntese, avaliação biológica e estudos de docking molecular de hidrazinocarbothioamidas ligadas ao indol N-propilsulfonil como inibidores seletivos de ecto-5′-nucleotidase e NTPDase
Por que esta pesquisa importa para tratamentos futuros do câncer
Nosso sistema imunológico está em constante vigilância às células cancerígenas, mas os tumores desenvolveram mecanismos engenhosos para desativar essas defesas. Um desses mecanismos usa mensageiros químicos derivados do ATP, a mesma molécula que fornece energia às nossas células. Este artigo descreve uma nova família de pequenas moléculas projetadas para interromper esse mecanismo químico, com o objetivo de longo prazo de ajudar o sistema imunológico a reconhecer e atacar melhor os tumores.
O interruptor químico que acalma as células imunes
As células se comunicam por muitos sinais, e um canal importante baseia-se em nucleotídeos como o ATP e seu produto de degradação, a adenosina. Fora da célula, uma cadeia de enzimas na membrana celular converte continuamente ATP em adenosina. Dois atores-chave, conhecidos como CD39 e CD73, costumam ser produzidos em excesso em tecidos tumorais com baixa oxigenação. Nesses locais, eles transformam rapidamente o ATP liberado por células estressadas ou moribundas em adenosina, que atua como um “tranquilizante” químico sobre células imunes próximas. Altos níveis de adenosina reduzem a atividade de linfócitos T, promovem a formação de vasos sanguíneos e ajudam a disseminação do tumor. Bloquear as enzimas que geram adenosina é, portanto, uma estratégia atraente na imunoterapia moderna do câncer.
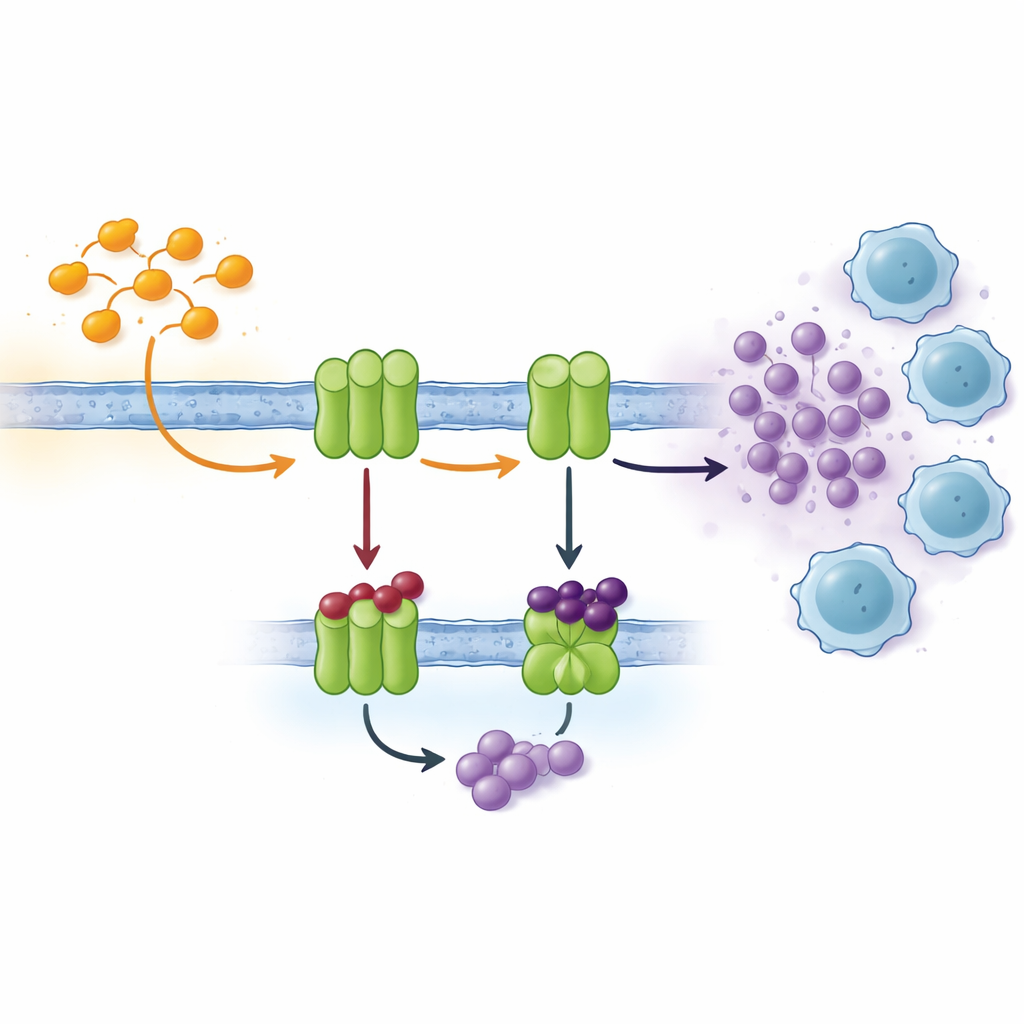
Desenhando bloqueadores mais inteligentes usando um sistema de anel comprovado
Projetistas de fármacos frequentemente partem de sistemas de anel já demonstrados como valiosos na medicina. O anel indol, presente em vários medicamentos anticâncer aprovados, é uma dessas estruturas. Outro componente útil, a tiosemicarbazona, pode coordenar metais e interage fortemente com muitos alvos biológicos. Neste trabalho, os pesquisadores combinaram esses dois motivos em um único esqueleto híbrido e o ajustaram ao anexar diferentes grupos químicos, criando uma pequena biblioteca de 22 compostos relacionados. Eles variaram a posição do grupo tiosemicarbazona no anel indol e alteraram os grupos laterais anexados para observar como essas mudanças afetavam a capacidade de bloquear a CD73 e várias enzimas relacionadas chamadas NTPDases.
Testando quais moléculas atingem quais enzimas
A equipe primeiro confirmou a estrutura e a pureza de todas as novas moléculas usando técnicas laboratoriais padrão, como espectroscopia no infravermelho e ressonância magnética nuclear, espectrometria de massas e cromatografia líquida de alta eficiência. Em seguida, mediram quão bem cada composto reduzia a atividade de cinco enzimas humanas em ensaios in vitro: CD73 e quatro tipos de NTPDase (1, 2, 3 e 8). Vários membros da série inibiram seus alvos em concentrações micromolares baixas, o que significa que eram muito mais potentes do que inibidores de referência comumente usados. Diferentes decorações químicas no esqueleto orientaram cada composto para tipos enzimáticos particulares. Por exemplo, uma molécula rotulada 5f foi especialmente eficaz contra NTPDase2 e NTPDase8, enquanto 5i favoreceu NTPDase1. Dois compostos relacionados, 5n e 5o, destacaram-se por sua forte ação sobre CD73 e NTPDases selecionadas, marcando-os como candidatos líderes especialmente promissores.
Observando o bolso de ligação no computador
Para entender por que algumas moléculas funcionaram melhor que outras, os pesquisadores usaram simulações computacionais detalhadas. Eles se concentraram em CD73 porque existe uma estrutura tridimensional de alta resolução dessa enzima disponível. Experimentos de docking virtual mostraram que os compostos ativos se acomodam no bolso catalítico da enzima de maneira consistente, onde o anel indol se empilha contra aminoácidos aromáticos e o segmento tiosemicarbazona forma ligações de hidrogênio com resíduos-chave. Cálculos da energia de ligação sugeriram que contatos hidrofóbicos bem ajustados e forças de van der Waals são contribuintes principais para a forte afinidade observada para 5n e 5o. Simulações longas de dinâmica molecular, cada uma acompanhando o movimento atômico por meio meio microsegundo, indicaram que esses complexos permanecem estáveis, com apenas pequenas flutuações tanto na proteína quanto na posição do inibidor ao longo do tempo.
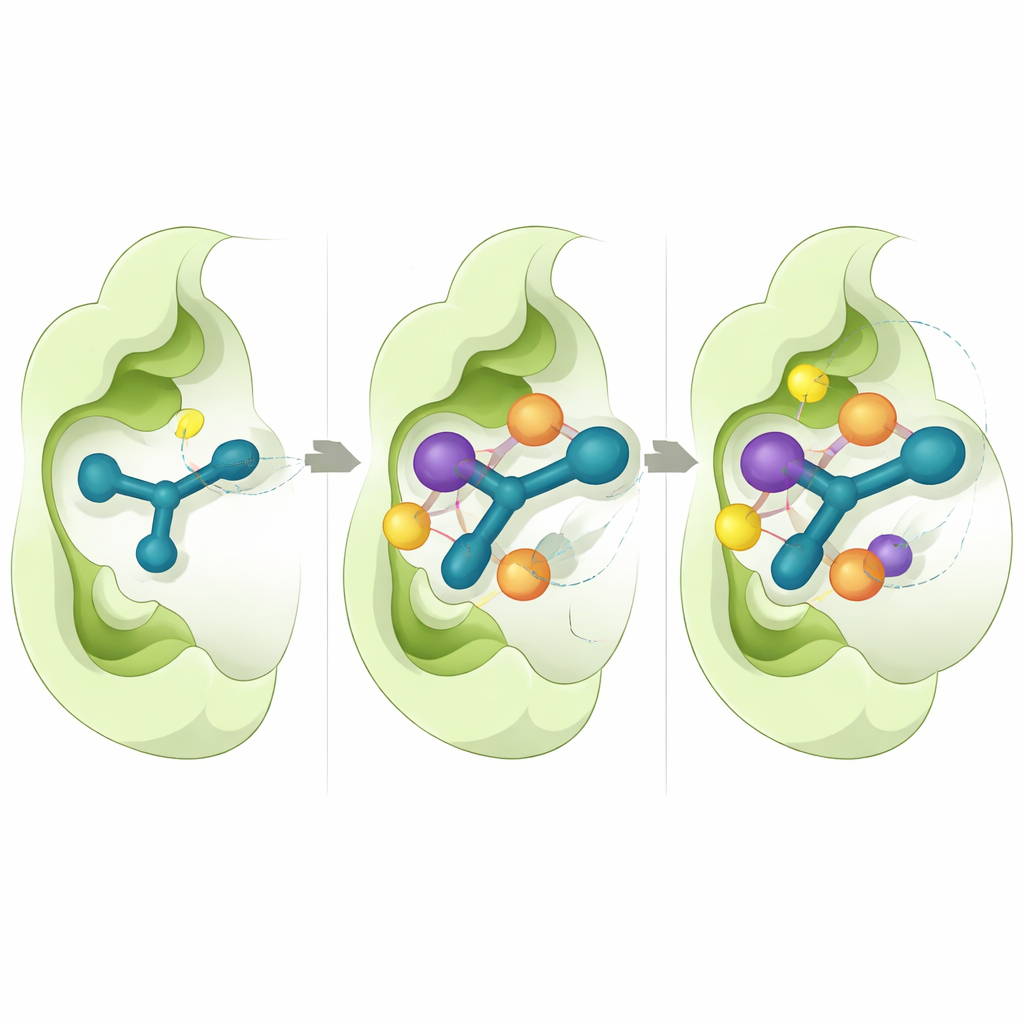
Indícios iniciais de comportamento semelhante a fármacos
Além de atingir seus alvos, candidatos a fármaco devem se comportar adequadamente no corpo. Os autores, portanto, previram propriedades farmacocinéticas como absorção e distribuição in silico. A maioria dos compostos da série, e especialmente 5n e 5o, apresentou um equilíbrio favorável entre tamanho, solubilidade e permeabilidade de membrana, com boa absorção oral prevista e apenas pequenas violações de regras empíricas. Esses dados, combinados com sua inibição enzimática forte e seletiva e a ligação estável nas simulações, apoiam a consideração de 5n e 5o como pontos de partida para otimização adicional em vez de candidatos finais a medicamentos.
O que isso pode significar para os pacientes
Quando tumores utilizam CD39 e CD73 para inundar seu entorno com adenosina, as células imunes ficam lentas e menos capazes de atacar. Este estudo apresenta um novo conjunto de moléculas baseadas em indol que interferem seletivamente nessa via in vitro e mostram comportamento encorajador em modelos computacionais. Embora ainda reste muito trabalho — incluindo testes em células, em animais e, eventualmente, em humanos — os achados sugerem que esse esqueleto químico pode ser moldado em futuros medicamentos que ajudem a remover os “freios” químicos que os tumores colocam sobre o sistema imunológico, potencialmente tornando as terapias atuais contra o câncer mais eficazes.
Citação: Batool, Z., Dutt, S.M., al-Rashida, M. et al. Synthesis, biological evaluation and molecular docking studies of N-propylsulfonyl indole-linked hydrazinecarbothioamides as selective ecto-5′-nucleotidase and NTPDase inhibitors. Sci Rep 16, 14419 (2026). https://doi.org/10.1038/s41598-026-50728-3
Palavras-chave: inibição de ecto-5-nucleotidase, inibidores de NTPDase, sinalização por adenosina, imunoterapia do câncer, tiosemicarbazonas de indol