Clear Sky Science · ar
تخليق وتقييم بيولوجي ودراسات اقتران جزيئي لمشتقات كاربوثيوأميد الهيدرازين المربوطة بالإندول ذات ن‑بروبيل سلفونيل كمثبطات انتقائية لإنزيم ecto‑5′‑nucleotidase وNTPDase
لماذا يهم هذا البحث لعلاجات السرطان المستقبلية
جهازنا المناعي يراقب الخلايا السرطانية باستمرار، لكن الأورام طورت حيلًا ذكية لإيقاف تلك الدفاعات. إحدى تلك الحيل تستخدم مرسلّات كيميائية مشتقة من ATP، نفس الجزيء الذي يمد خلايانا بالطاقة. تصف هذه الورقة عائلة جديدة من الجزيئات الصغيرة المصممة لمقاطعة تلك الخدعة الكيميائية، بهدف بعيد المدى مساعدة الجهاز المناعي على التعرف أفضل على الأورام ومهاجمتها.
المفتاح الكيميائي الذي يهدئ الخلايا المناعية
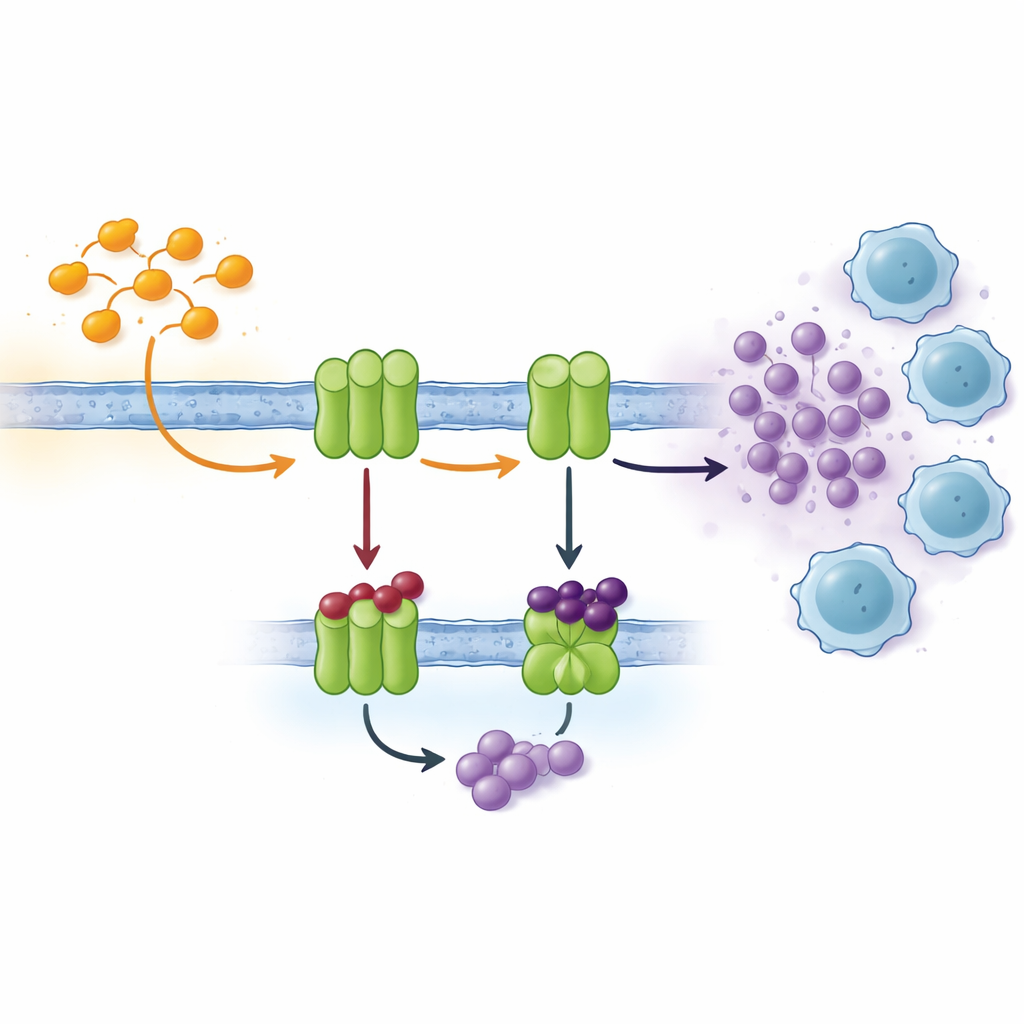
الخلايا تتواصل عبر إشارات متعددة، وإحدى القنوات المهمة تعتمد على النيوكليوتيدات مثل ATP ومنتجه الناتج عن التحلل، الأدينوزين. خارج الخلية، سلسلة من الإنزيمات الموجودة في غشاء الخلية تحوّل ATP بشكل متتابع إلى أدينوزين. يلعب اثنان من هذه الإنزيمات، المعروفتان باسم CD39 وCD73، دورًا بارزًا وغالبًا ما يُفرزان بكميات زائدة في الأنسجة السرطانية منخفضة الأكسجين. هناك، يحولان بسرعة ATP الذي تفرزه الخلايا المتوترة أو المحتضرة إلى أدينوزين، الذي يعمل كمهدئ كيميائي للخلايا المناعية المجاورة. تركيزات الأدينوزين المرتفعة تخفف نشاط الخلايا التائية، وتدعم نمو الأوعية الدموية، وتساعد على انتشار الأورام. لذلك يعد حجب الإنزيمات التي تخلق الأدينوزين استراتيجية جذابة في مناعة السرطان الحديثة.
تصميم مثبطات أذكى باستخدام حلقة ثبتت فعاليتها
غالبًا ما يبدأ مصممو الأدوية بأنظمة حلقية أظهرت قيمة طبية سابقًا. حلقة الإندول، الموجودة في عدة أدوية مضادة للسرطان معتمدة، هي أحد هذه الهياكل. مكوّن مفيد آخر، الثيوسيميكاربازون، يمكنه أن يربط المعادن ويتفاعل بقوة مع أهداف بيولوجية متعددة. في هذا العمل، دمج الباحثون هذين الدافعين في سقالة هجينة واحدة وضبطوها بتوصيل مجموعات كيميائية مختلفة، فأنشأوا مكتبة صغيرة تتألف من 22 مركبًا ذات صلة. غيّروا موقع وحدة الثيوسيميكاربازون على حلقة الإندول وبدّلوا المجموعات الجانبية الملحقة ليروا كيف تؤثر هذه التغييرات على قدرة حجب CD73 وعدد من الإنزيمات المرتبطة المسماة NTPDases.
اختبار أي الجزيئات تستهدف أي إنزيم
أكد الفريق أولًا بنية ونقاء جميع الجزيئات الجديدة باستخدام تقنيات مخبرية قياسية مثل مطيافية الأشعة تحت الحمراء والمطيافية النووية المغناطيسية، والكتلة الطيفية، والكروماتوغرافيا السائلة عالية الأداء. ثم قاسوا مدى قدرة كل مركب على إبطاء خمسة إنزيمات بشرية في تجارب في أنابيب الاختبار: CD73 وأربعة أنواع من NTPDase (1، 2، 3 و8). عدة مركبات من السلسلة أعاقت أهدافها عند تراكيز ميكرومولارية منخفضة، ما يعني أنها كانت أقوى بكثير من المثبطات المرجعية الشائعة الاستخدام. الزينة الكيميائية المختلفة على السقالة وجهت كل مركب نحو أنواع إنزيمية معينة. على سبيل المثال، كان مركب موسوم 5f فعّالًا بشكل خاص ضد NTPDase2 وNTPDase8، بينما فضّل 5i NTPDase1. برزا مركبان مرتبطان، 5n و5o، بسبب تأثيرهما القوي على CD73 وبعض NTPDases المختارة، مما يجعلهما مرشحين رئيسيين واعدين.
التحديق في جيب الربط باستخدام الحاسوب
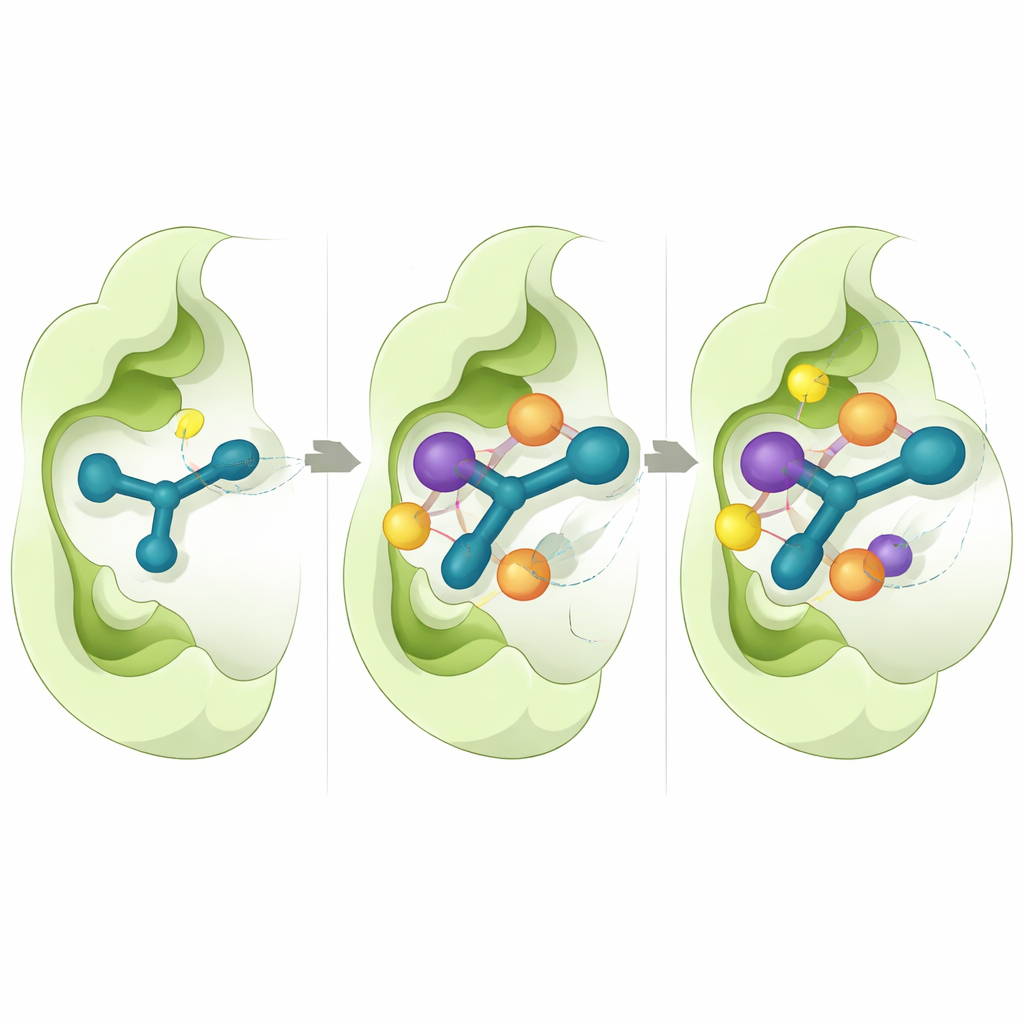
لفهم سبب تفوق بعض الجزيئات على غيرها، استخدم الباحثون محاكاة حاسوبية مفصلة. ركزوا على CD73، لأن هناك بنية ثلاثية الأبعاد عالية الدقة لهذا الإنزيم متاحة. أظهرت تجارب الإقتران الافتراضية أن المركبات النشطة تنزلق إلى الجيب التحفيزي للإنزيم بطريقة متسقة، حيث تتراص حلقة الإندول مقابل أحماض أمينية عطرية وتشكل وحدة الثيوسيميكاربازون روابط هيدروجينية مع بقايا رئيسية. أشارت حسابات طاقة الارتباط إلى أن التلامسات الهيدروفوبية المحكمة وقوى فان دير فالس تساهمان بشكل رئيسي في الارتباط القوي المرصود لـ5n و5o. محاكاة ديناميكا الجزيئات الطويلة، كل منها يحاكي حركة الذرات لنصف ميكروثانية، أشارت إلى أن هذه المعقدات تظل مستقرة مع تقلبات طفيفة في كل من البروتين ومواقع المركب المثبط مع مرور الوقت.
دلالات مبكرة على سلوك شبيه بالدواء
بعيدًا عن مجرد استهدافها للإنزيمات، يجب أن تتحرك الأدوية المحتملة داخل الجسم بشكل مناسب. لذلك توقع المؤلفون خواص الامتصاص والتوزيع وغيرها من الخواص الحرائك الدوائية حسابيًا. أظهر معظم المركبات في السلسلة، وخصوصًا 5n و5o، توازنًا ملائمًا للحجم والذوبانية ونفاذية الغشاء، مع توقع جيد للامتصاص الفموي وانتهاكات طفيفة فقط لقواعد الإبهام العاملة. تدعم هذه البيانات، إلى جانب تثبيطها القوي والانتقائي للإنزيمات والارتباط المستقر في المحاكاة، اعتبار 5n و5o كنقاط انطلاق لمزيد من التحسين بدلاً من اعتبارهما مرشحين دوائيين نهائيين.
ما الذي قد يعنيه هذا للمرضى
عندما تستخدم الأورام CD39 وCD73 لفيض محيطها بالأدينوزين، تصبح الخلايا المناعية بطيئة وأقل قدرة على الهجوم. تقدم هذه الدراسة مجموعة جديدة من الجزيئات القائمة على الإندول التي تتداخل انتقائيًا مع هذا المسار في أنابيب الاختبار وتظهر سلوكًا مشجعًا في النماذج الحاسوبية. بينما لا يزال الكثير من العمل مطلوبًا—بما في ذلك اختبارات في الخلايا والحيوانات وفي نهاية المطاف البشر—تشير النتائج إلى أن هذه السقالة الكيميائية يمكن تشكيلها إلى أدوية مستقبلية تساعد في رفع "مكابح" الأورام الكيميائية على الجهاز المناعي، مما قد يجعل العلاجات الحالية للسرطان أكثر فعالية.
الاستشهاد: Batool, Z., Dutt, S.M., al-Rashida, M. et al. Synthesis, biological evaluation and molecular docking studies of N-propylsulfonyl indole-linked hydrazinecarbothioamides as selective ecto-5′-nucleotidase and NTPDase inhibitors. Sci Rep 16, 14419 (2026). https://doi.org/10.1038/s41598-026-50728-3
الكلمات المفتاحية: مثبط ecto‑5‑nucleotidase, مثبطات NTPDase, إشارة الأدينوزين, المناعة المضادة للسرطان, ثيوسيميكاربازونات الإندول