Clear Sky Science · zh
CircFN1通过miR-19b-3p/PTEN信号轴调控IL-1β诱导的骨关节炎
为何关节酸痛重要
骨关节炎常被归结为“磨损”,但对数以百万计的人来说,它意味着日常的疼痛、僵硬和失去独立生活能力。这项研究深入探查疼痛关节的机理,提出一个及时的问题:为什么有些膝盖和髋关节会如此恶化,我们是否可以通过改变软骨细胞内某些微小RNA分子的行为来减缓这一过程?
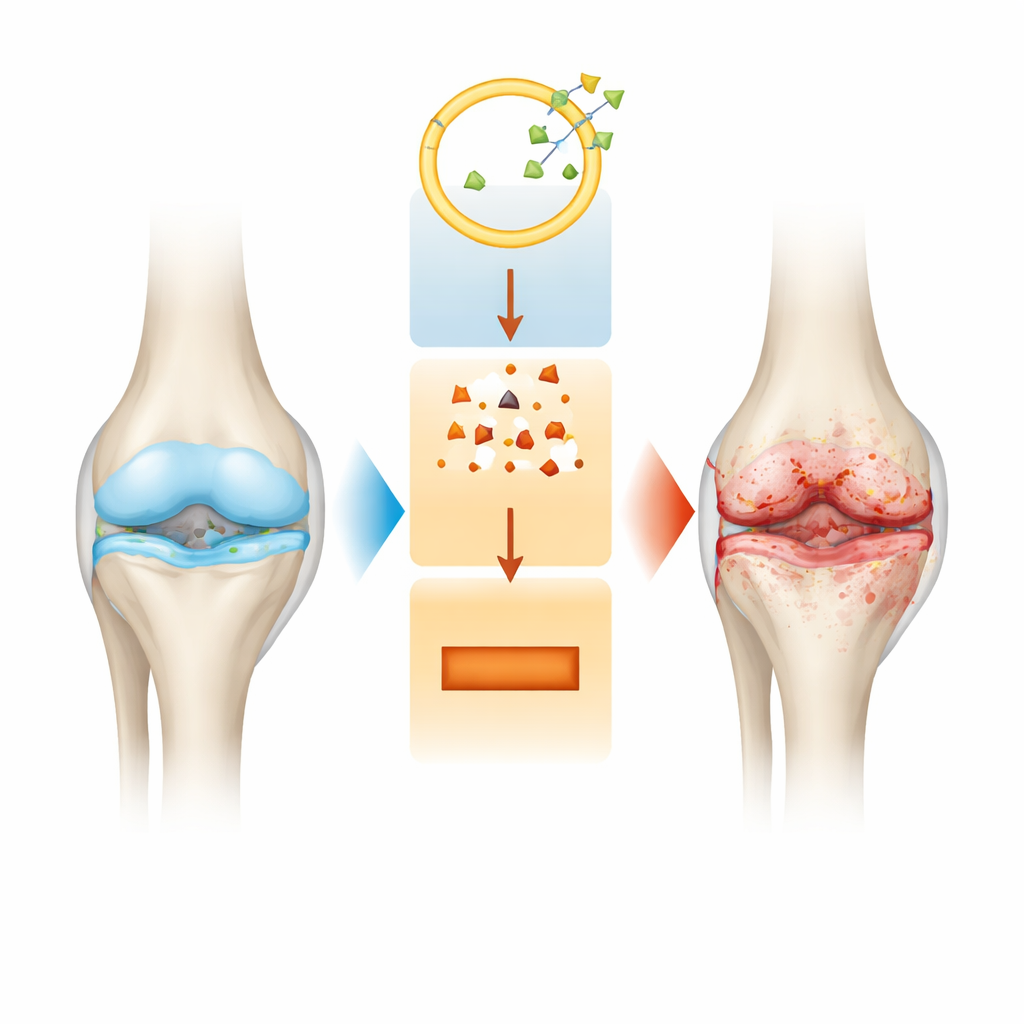
更细致地观察关节破坏
骨关节炎不仅仅是软骨变薄。随着病情进展,整个关节都会发生改变:骨端的光滑缓冲层被侵蚀,关节内膜出现炎症,基底骨以可能加剧疼痛的方式重塑。目前的治疗主要缓解症状,但无法阻止这种缓慢的结构性损伤。因此,研究人员寻找软骨细胞(称为软骨细胞)内的分子开关,试图解释这些细胞为何开始死亡以及为何其周围的支持基质崩解。
环状RNA的隐秘世界
近年来,科学家发现我们基因组中有许多片段并不翻译成蛋白质,但仍然具有强大的调控作用。其中包括环状RNA——形成环状的分子,异常稳定并且在特定组织中常常丰度较高。本文的团队关注其中一种分子circFN1,在暴露于炎症信号IL‑1β的人类软骨细胞中其含量升高。IL‑1β是实验室中常用来模拟骨关节炎的化学刺激。比较正常和IL‑1β处理过的软骨细胞的测序实验显示,circFN1是升高幅度最大的环状RNA之一,使其成为推动关节损伤的主要嫌疑者。
三步分子的角力
研究人员揭示了一条将circFN1与细胞损伤相连的相互作用链。首先,他们表明circFN1能像海绵一样吸附一种小型调控RNA miR‑19b‑3p,将其结合并隔离。通常,miR‑19b‑3p有助于控制PTEN的水平——PTEN是一种影响细胞存活、炎症和基质维护的蛋白。当circFN1水平上升时,更多的miR‑19b‑3p被吸收,进而改变PTEN的活性,扰乱细胞内保护性与有害信号之间的平衡。通过一系列基因“上调与下调”的实验,作者证明了circFN1–miR‑19b‑3p–PTEN这一链条强烈影响软骨细胞对炎性胁迫的响应。
当开关被拨动时会发生什么
为了检验该通路的功能性影响,研究组在IL‑1β处理的软骨细胞中有意降低circFN1。当circFN1被降低时,存活的细胞增多,程序性死亡的细胞减少,软骨的关键构建成分如聚聚蛋白(aggrecan)得以更好地保存。与此同时,分解软骨的分子如MMP‑13下降,周围的炎性物质“汤”例如TNF‑α和IL‑6的强度也减弱。当研究者同时调整miR‑19b‑3p和PTEN时,这些保护性变化按可预测的方式增强或减弱,这进一步支持三者构成一个相互连接的调控回路,而非各自独立作用。
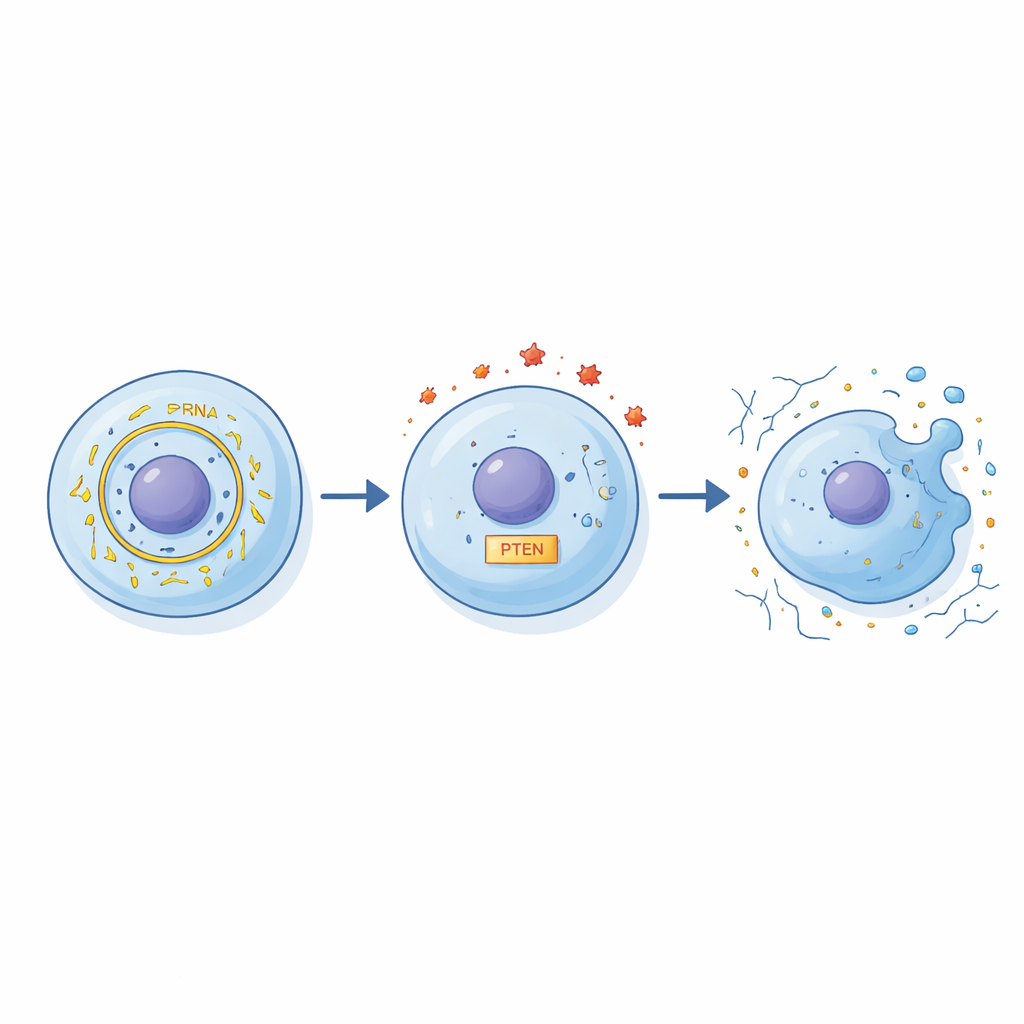
从细胞培养到未来治疗
尽管这些实验是在培养的人类软骨细胞中进行,而非活体关节,但结果指向骨关节炎治疗的一个新的概念性杠杆。该研究表明,升高的circFN1通过重排miR‑19b‑3p与PTEN之间的平衡,放大炎症驱动的软骨损伤。通俗地说,这种环状RNA过剩使软骨细胞对炎性刺激更为脆弱,更容易死亡并丢失其支持基质。如果未来在动物及患者研究中证实这些结果,检测circFN1可能有助于早期发现关节损伤,且旨在阻断circFN1或增强miR‑19b‑3p的疗法或许有望延缓偶发僵硬向慢性致残性骨关节炎的演变。
引用: Jiang, Y., Wang, Q., Yang, X. et al. CircFN1 modulates IL-1β-induced osteoarthritis through the miR-19b-3p/PTEN signaling axis. Sci Rep 16, 10710 (2026). https://doi.org/10.1038/s41598-026-45897-0
关键词: 骨关节炎, 软骨, 非编码RNA, 炎症, 关节退化