Clear Sky Science · pt
CircFN1 modula a osteoartrite induzida por IL-1β através do eixo de sinalização miR-19b-3p/PTEN
Por que as juntas doloridas importam
A osteoartrite é frequentemente descartada como “desgaste”, mas para milhões de pessoas significa dor diária, rigidez e perda de independência. Este estudo investiga em detalhe as articulações doloridas e faz uma pergunta oportuna: por que alguns joelhos e quadris se deterioram tão severamente, e seria possível desacelerar esse processo alterando o comportamento de certas moléculas de RNA minúsculas dentro das células da cartilagem?
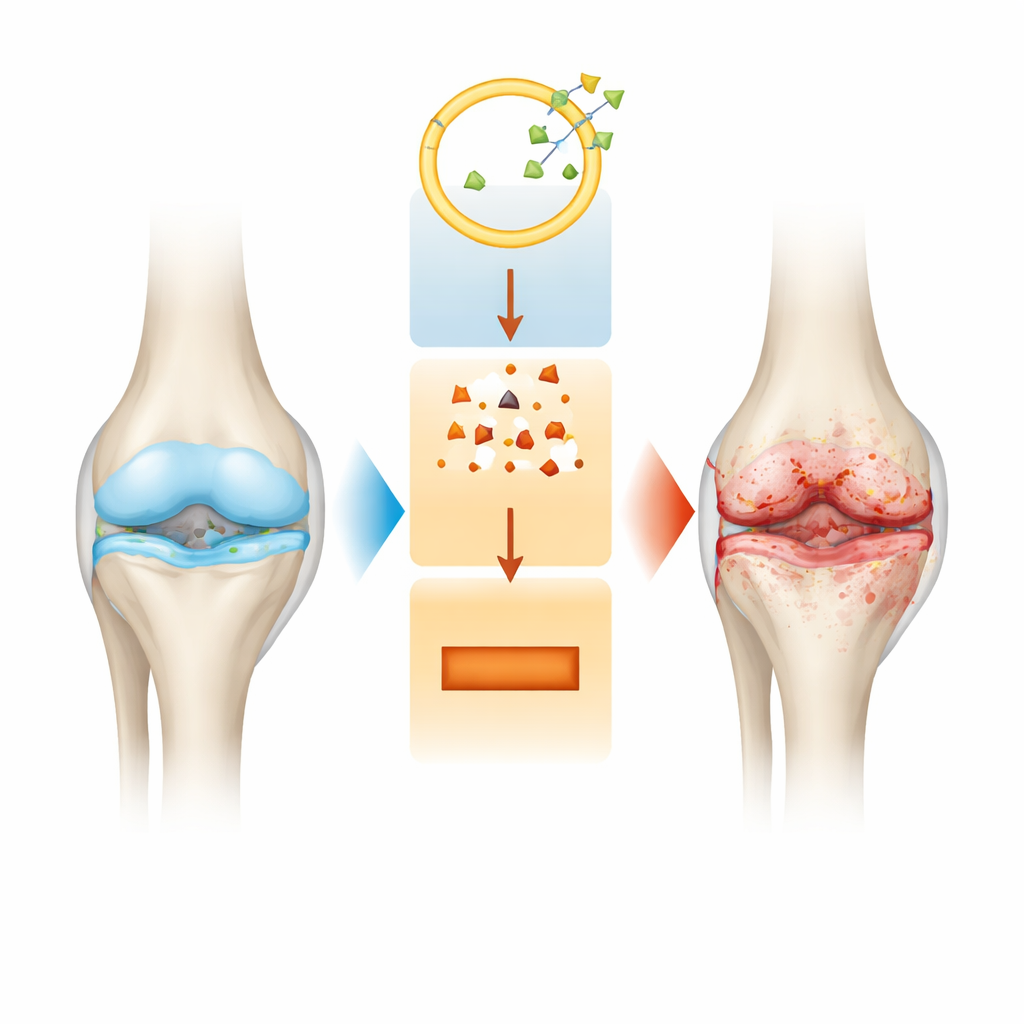
Um olhar mais atento à degradação articular
A osteoartrite é mais do que afinamento da cartilagem. À medida que a doença avança, toda a articulação muda: o amortecedor liso nas extremidades dos ossos se desgasta, o revestimento da articulação fica inflamado e o osso subjacente se remodela de maneiras que podem agravar a dor. Os tratamentos atuais aliviam principalmente os sintomas, mas não interrompem esse dano estrutural lento. Por isso, os pesquisadores procuram interruptores moleculares dentro das células da cartilagem, chamadas condrócitos, que possam explicar por que essas células começam a morrer e por que a matriz de suporte ao redor delas se degrada.
O mundo oculto do RNA circular
Nos últimos anos, os cientistas descobriram que muitas sequências do nosso material genético nunca se tornam proteínas, mas ainda assim exercem papéis regulatórios poderosos. Entre elas estão os RNAs circulares — moléculas em loop que são incomumente estáveis e frequentemente abundantes em tecidos específicos. A equipe por trás deste trabalho concentrou-se em uma dessas moléculas, circFN1, encontrada em níveis mais altos em condrócitos humanos expostos ao sinal inflamatório IL‑1β, um composto comumente usado para mimetizar a osteoartrite em laboratório. Experimentos de sequenciamento comparando condrócitos normais e tratados com IL‑1β mostraram que circFN1 foi um dos RNAs circulares mais fortemente aumentados, tornando-o um suspeito principal em alimentar o dano articular.
Uma disputa molecular em três etapas
Os pesquisadores descobriram uma cadeia de interações que liga circFN1 ao dano celular. Primeiro, demonstraram que circFN1 pode atuar como uma esponja para um pequeno RNA regulatório chamado miR‑19b‑3p, ligando‑se e sequestrando‑o. Normalmente, miR‑19b‑3p ajuda a controlar os níveis de PTEN, uma proteína que influencia sobrevivência celular, inflamação e manutenção da matriz. Quando os níveis de circFN1 aumentam, mais miR‑19b‑3p é absorvido, o que por sua vez altera a atividade de PTEN e perturba o equilíbrio entre sinais protetores e nocivos na célula. Por meio de uma série de experimentos genéticos de “aumentar e diminuir”, os autores demonstraram que essa cadeia circFN1–miR‑19b‑3p–PTEN molda fortemente como os condrócitos respondem ao estresse inflamatório.
O que acontece quando os interruptores são acionados
Para testar o impacto funcional dessa via, a equipe reduziu deliberadamente circFN1 em condrócitos tratados com IL‑1β. Quando circFN1 foi diminuído, mais células sobreviveram, menos passaram por morte programada, e blocos construtivos chave da cartilagem, como a proteína de matriz agrecano, foram melhor preservados. Ao mesmo tempo, moléculas que degradam a cartilagem, como MMP‑13, diminuíram, e a “sopa” circundante de substâncias inflamatórias, como TNF‑α e IL‑6, ficou menos intensa. Quando os pesquisadores também alteraram miR‑19b‑3p e PTEN, essas mudanças protetoras se fortaleceram ou enfraqueceram de maneiras previsíveis, reforçando a ideia de que os três parceiros formam um circuito regulatório conectado em vez de agirem isoladamente.
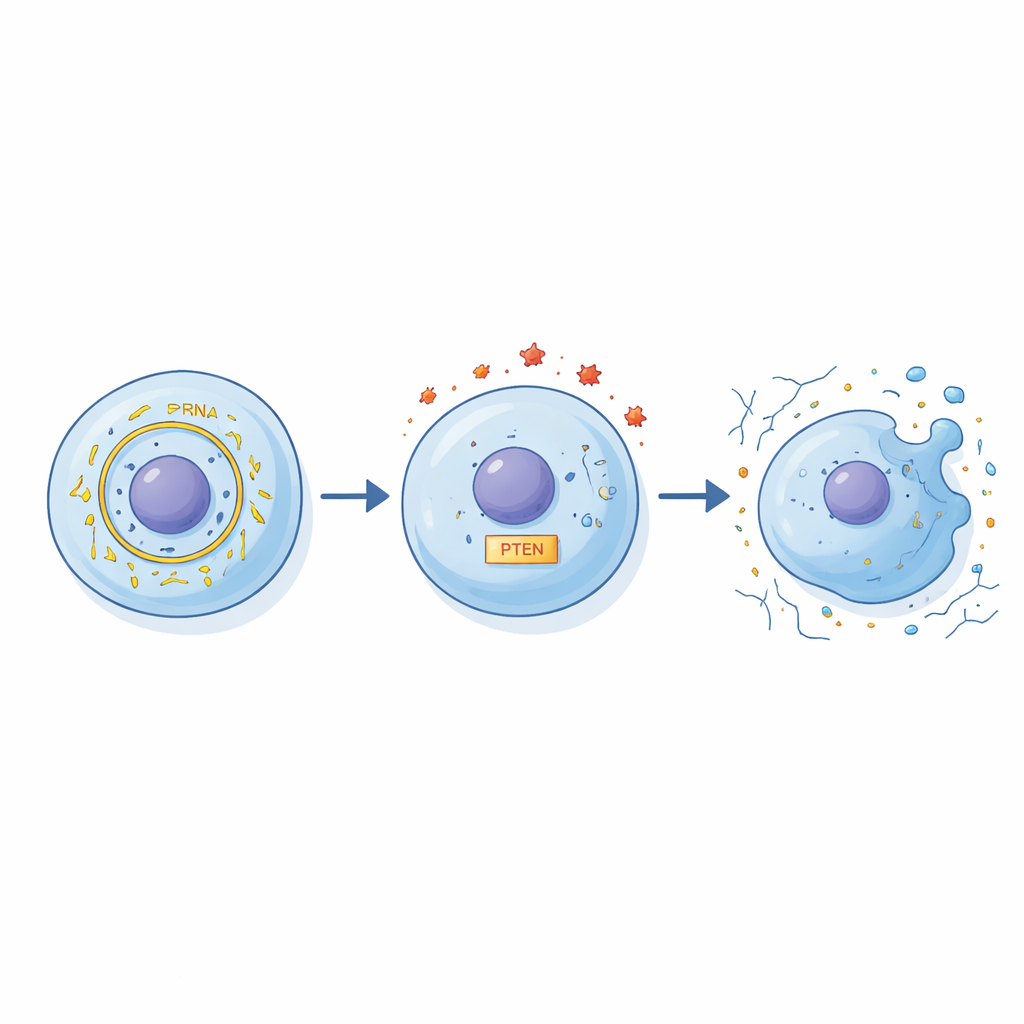
Das placas de Petri a futuras terapias
Embora esses experimentos tenham sido realizados em condrócitos humanos cultivados em vez de articulações vivas, os achados apontam para uma nova alavanca conceitual para o tratamento da osteoartrite. O estudo sugere que o circFN1 elevado amplifica o dano à cartilagem induzido pela inflamação ao rearranjar o equilíbrio entre miR‑19b‑3p e PTEN. Em termos simples, um excesso desse RNA circular torna os condrócitos mais vulneráveis a insultos inflamatórios e mais propensos a morrer e perder sua matriz de suporte. Se trabalhos futuros em animais e pacientes confirmarem esses resultados, medir circFN1 poderia ajudar a detectar danos articulares precoces, e terapias projetadas para bloquear circFN1 ou aumentar miR‑19b‑3p poderiam, um dia, retardar a progressão de rigidez ocasional para osteoartrite crônica e incapacitante.
Citação: Jiang, Y., Wang, Q., Yang, X. et al. CircFN1 modulates IL-1β-induced osteoarthritis through the miR-19b-3p/PTEN signaling axis. Sci Rep 16, 10710 (2026). https://doi.org/10.1038/s41598-026-45897-0
Palavras-chave: osteoartrite, cartilagem, RNA não codificante, inflamação, degeneração articular