Clear Sky Science · ar
يعدِّل CircFN1 الفُصال العظمي المحفَّز بواسطة IL-1β عبر محور إشارات miR-19b-3p/PTEN
لماذا تهم المفاصل المؤلمة
غالبًا ما يُستخف بالفصال العظمي باعتباره "تآكلًا واستهلاكًا"، لكن بالنسبة لملايين الأشخاص يعني ذلك ألمًا يوميًّا وتيبُّسًا وفقدانًا للاستقلالية. تبحث هذه الدراسة تحت السطح عن سبب تدهور بعض الركب والوركين إلى هذا الحد، وتتساءل: هل يمكن أن نبطئ هذه العملية بتغيير سلوك جزيئات RNA الصغيرة داخل خلايا الغضروف؟
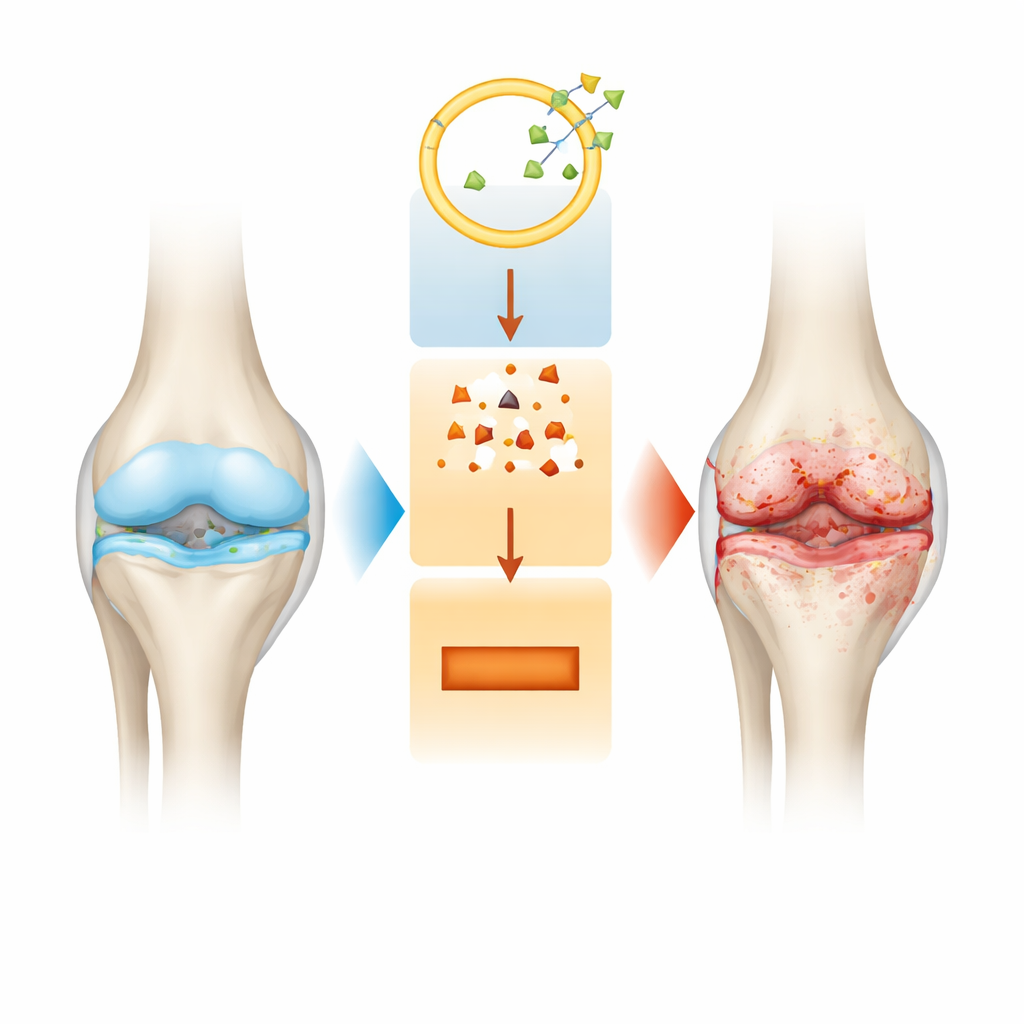
نظرة أقرب على انحلال المفصل
الفصال العظمي هو أكثر من ترقق في الغضروف. مع تقدم المرض، يتغير المفصل بأكمله: تتآكل الوسادة الملساء على أطراف العظام، ويصبح بطانة المفصل ملتهبة، ويعاد تشكيل العظم الأسفل بطرق قد تزيد الألم. العلاجات الحالية تخفف الأعراض في المقام الأول لكنها لا توقف هذا التلف البنيوي البطيء. لذلك يبحث الباحثون عن مفاتيح جزيئية داخل خلايا الغضروف، المسماة الخلايا الغضروفية، قد تفسر لماذا تبدأ هذه الخلايا بالموت ولماذا ينهار المصفوف الداعم حولها.
العالم الخفي للـ RNA الدائري
في السنوات الأخيرة، اكتشف العلماء أن أجزاء كثيرة من مادّتنا الوراثية لا تتحول إلى بروتينات لكنها تؤدي أدوارًا تنظيمية قوية. من بينها RNAs الدائرية—جزيئات حلقيَّة مستقرة بشكل غير عادي وغالبًا وفيرة في أنسجة محددة. ركز الفريق خلف هذه الورقة على جزيء واحد من هذا النوع، circFN1، الذي وُجد بمستويات أعلى في الخلايا الغضروفية البشرية المعرضة للإشارة الالتهابية IL‑1β، وهي مادة كيميائية تُستخدم عادةً لمحاكاة الفصال العظمي في المختبر. أظهرت تجارب التسلسل المقارنة بين الخلايا الغضروفية الطبيعية والمعالجة بـ IL‑1β أن circFN1 كان واحدًا من الـ RNA الدائرية التي زادت بشكل قوي، مما يجعله مشتبهًا رئيسيًّا في تغذية تلف المفصل.
سحب حبل جزيئي مكوَّن من ثلاث خطوات
كشف الباحثون سلسلة تفاعلات تربط circFN1 بإصابة الخلايا. أولًا، بينوا أن circFN1 يمكن أن يعمل كإسفنجة لـ RNA تنظيمي صغير يُدعى miR‑19b‑3p، فيلتصق به ويحتجزه. عادةً يساعد miR‑19b‑3p في ضبط مستويات PTEN، وهو بروتين يؤثر على بقاء الخلية والالتهاب وصيانة المصفوف. عندما ترتفع مستويات circFN1، تُمتصّ المزيد من miR‑19b‑3p، مما يغيّر نشاط PTEN ويعطّل التوازن بين الإشارات الحامية والضارة داخل الخلية. من خلال سلسلة من تجارب "تشغيل وخفض" جينية، أظهر المؤلفون أن سلسلة circFN1–miR‑19b‑3p–PTEN تشكل تأثيرًا قويًا في كيفية استجابة الخلايا الغضروفية للإجهاد الالتهابي.
ماذا يحدث عندما تُقلَب المفاتيح
لاختبار الأثر الوظيفي لهذا المسار، خفّض الفريق عمدًا circFN1 في خلايا غضروفية معالجة بـ IL‑1β. عند انخفاض circFN1، نَجت خلايا أكثر، خضعت نسبة أقل للانتحار المبرمج، وتم الحفاظ على مكونات أساسية للغضروف مثل البروتين المصفوفي أجركان بصورة أفضل. في الوقت نفسه، انخفضت جزيئات متحللة للغضروف مثل MMP‑13، وهدأت "الحساء" المحيط من المواد الالتهابية مثل TNF‑α وIL‑6. عندما عدّل الباحثون أيضًا miR‑19b‑3p وPTEN، تعززت أو ضعفت هذه التغيرات الوقائية بطرق متوقعة، مما يعزز فكرة أن الشركاء الثلاثة يشكلون دائرة تنظيمية مترابطة بدلاً من العمل بشكل معزول.
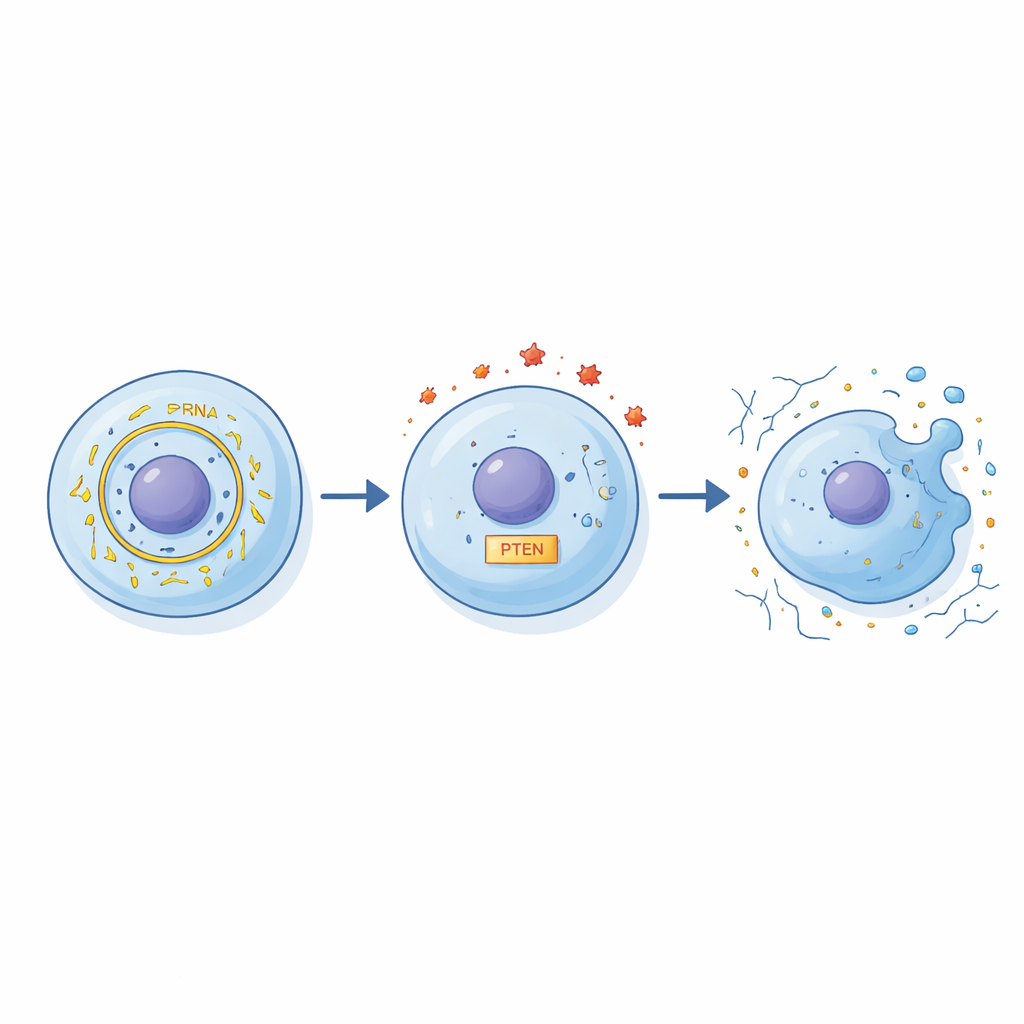
من أطباق الخلايا إلى علاجات مستقبلية
على الرغم من أن هذه التجارب أُجريت في خلايا غضروفية بشرية مزروعة في المختبر وليس في مفاصل حية، تشير النتائج إلى رافعة مفهومية جديدة لعلاج الفصال العظمي. تقترح الدراسة أن ارتفاع circFN1 يضخم الضرر الذي يسببه الالتهاب للغضروف عن طريق إعادة ترتيب التوازن بين miR‑19b‑3p وPTEN. ببساطة، يجعل فائض هذا الـ RNA الدائري خلايا الغضروف أكثر عرضة للهجمات الالتهابية وأكثر ميلاً للموت وفقدان مصفوفها الداعمة. إذا أكدت أعمال مستقبلية في الحيوانات والمرضى هذه النتائج، قد يساعد قياس circFN1 على كشف تلف المفصل المبكر، وقد تؤدي علاجات تهدف إلى حجب circFN1 أو تعزيز miR‑19b‑3p يومًا ما إلى إبطاء الانتقال من تيبّس عرضي إلى فصال عظمي مزمن معوِّق.
الاستشهاد: Jiang, Y., Wang, Q., Yang, X. et al. CircFN1 modulates IL-1β-induced osteoarthritis through the miR-19b-3p/PTEN signaling axis. Sci Rep 16, 10710 (2026). https://doi.org/10.1038/s41598-026-45897-0
الكلمات المفتاحية: الفصال العظمي, الغضروف, RNA غير مشفَّر, الالتهاب, تدهور المفصل