Clear Sky Science · it
CircFN1 modula l'osteoartrite indotta da IL-1β attraverso l'asse di segnalazione miR-19b-3p/PTEN
Perché le articolazioni dolenti contano
L'osteoartrite viene spesso liquidata come “usura”, ma per milioni di persone significa dolore quotidiano, rigidità e perdita di autonomia. Questo studio apre il cofano delle articolazioni doloranti e pone una domanda attuale: perché alcune ginocchia e anche si deteriorano così tanto, e potremmo rallentare questo processo modificando il comportamento di certe piccole molecole di RNA all'interno delle cellule della cartilagine?
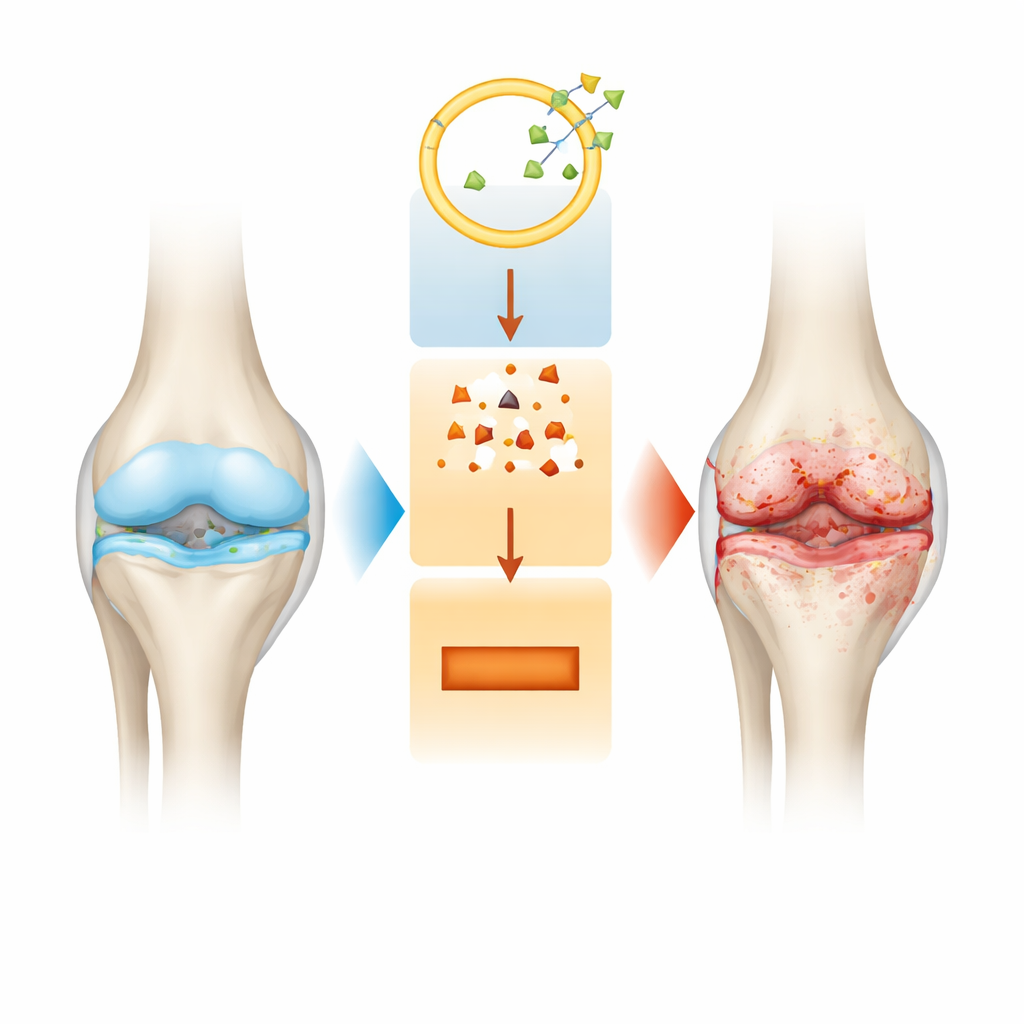
Uno sguardo più da vicino alla degradazione articolare
L'osteoartrite non è solo assottigliamento della cartilagine. Con l'avanzare della malattia, l'intera articolazione cambia: il cuscinetto liscio alle estremità delle ossa si erode, il rivestimento dell'articolazione diventa infiammato e l'osso sottostante si rimodella in modi che possono peggiorare il dolore. I trattamenti attuali alleviano principalmente i sintomi ma non fermano questo lento danno strutturale. I ricercatori cercano quindi interruttori molecolari all'interno dei condrociti, le cellule della cartilagine, che possano spiegare perché queste cellule iniziano a morire e perché la matrice di supporto intorno a loro si disgrega.
Il mondo nascosto degli RNA circolari
Negli ultimi anni gli scienziati hanno scoperto che molte porzioni del nostro materiale genetico non diventano proteine ma svolgono comunque ruoli regolatori potenti. Tra queste ci sono gli RNA circolari—molecole ad anello straordinariamente stabili e spesso abbondanti in tessuti specifici. Il gruppo dietro questo lavoro si è concentrato su una di queste molecole, circFN1, rilevata a livelli più alti nelle cellule cartilaginee umane esposte al segnale infiammatorio IL‑1β, una sostanza usata comunemente in laboratorio per imitare l'osteoartrite. Esperimenti di sequenziamento che confrontavano condrociti normali e trattati con IL‑1β hanno mostrato che circFN1 era una delle RNA circolari maggiormente aumentate, rendendola un principale indiziato nel promuovere il danno articolare.
Una lotta molecolare in tre tappe
I ricercatori hanno scoperto una catena di interazioni che collega circFN1 al danno cellulare. Innanzitutto hanno dimostrato che circFN1 può funzionare come una spugna per un piccolo RNA regolatore chiamato miR‑19b‑3p, legandolo e sequestrandolo. Normalmente miR‑19b‑3p aiuta a controllare i livelli di PTEN, una proteina che influisce sulla sopravvivenza cellulare, l'infiammazione e il mantenimento della matrice. Quando i livelli di circFN1 aumentano, più miR‑19b‑3p viene assorbito, il che a sua volta altera l'attività di PTEN e squilibra il rapporto tra segnali protettivi e dannosi nella cellula. Attraverso una serie di esperimenti genetici di “alza e abbassa” gli autori hanno dimostrato che questa catena circFN1–miR‑19b‑3p–PTEN modella in maniera significativa la risposta dei condrociti allo stress infiammatorio.
Cosa succede quando gli interruttori vengono azionati
Per testare l'impatto funzionale di questa via, il gruppo ha ridotto deliberatamente circFN1 in condrociti trattati con IL‑1β. Quando circFN1 è stato abbassato, più cellule sono sopravvissute, meno hanno subito morte programmata e i principali componenti della cartilagine, come la proteina di matrice aggrecan, sono stati meglio preservati. Allo stesso tempo, le molecole che degradano la cartilagine, come MMP‑13, sono diminuite e il «brodo» di sostanze infiammatorie come TNF‑α e IL‑6 è diventato meno intenso. Quando i ricercatori hanno anche modificato miR‑19b‑3p e PTEN, questi cambiamenti protettivi si sono rafforzati o indeboliti in modi prevedibili, rafforzando l'idea che i tre partner costituiscano un circuito regolatorio connesso anziché agire isolati.
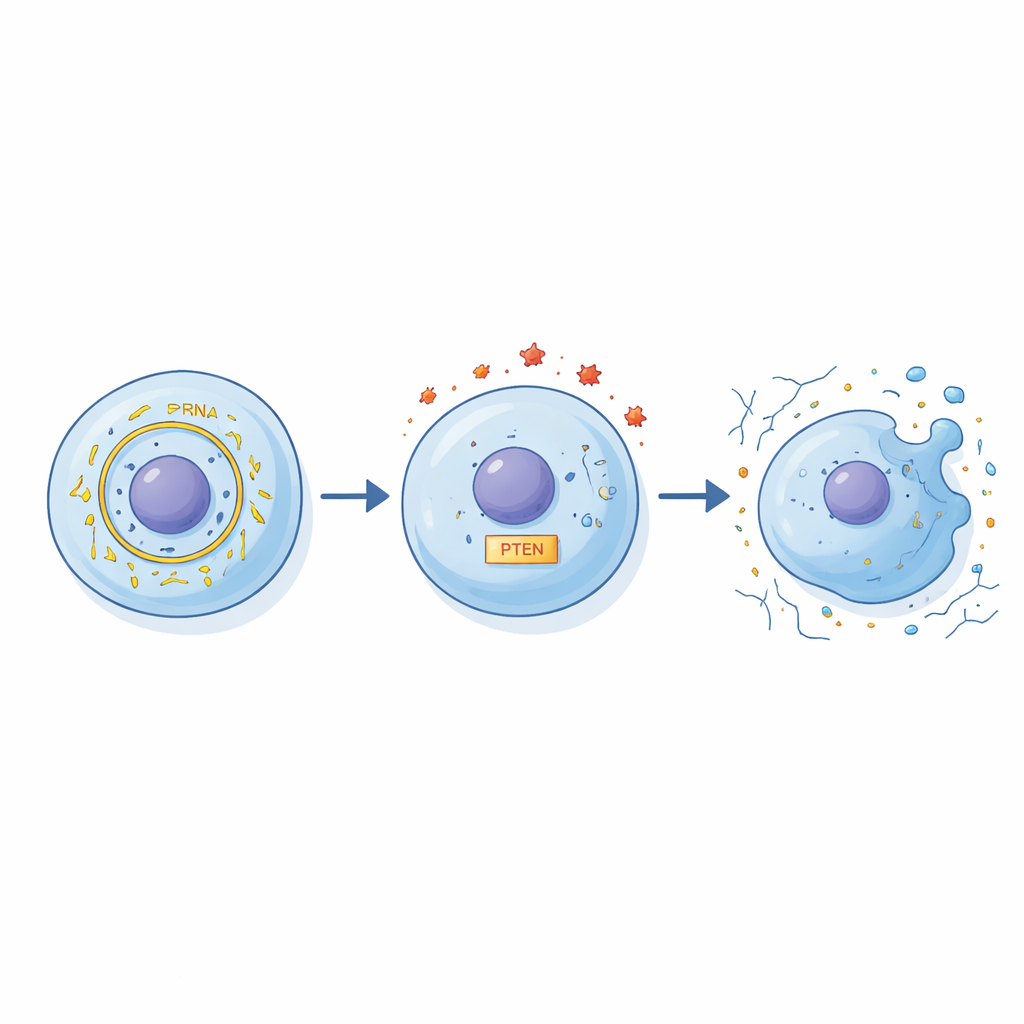
Dalle colture cellulari a future terapie
Sebbene questi esperimenti siano stati eseguiti in colture di cellule cartilaginee umane piuttosto che in articolazioni vive, i risultati indicano una nuova leva concettuale per il trattamento dell'osteoartrite. Lo studio suggerisce che l'aumento di circFN1 amplifica il danno alla cartilagine guidato dall'infiammazione riorganizzando l'equilibrio tra miR‑19b‑3p e PTEN. In termini semplici, un eccesso di questo RNA circolare rende i condrociti più vulnerabili agli insulti infiammatori e più inclini a morire e perdere la loro matrice di supporto. Se lavori futuri su animali e pazienti confermeranno questi risultati, la misurazione di circFN1 potrebbe aiutare a rilevare precocemente il danno articolare, e terapie progettate per bloccare circFN1 o aumentare miR‑19b‑3p potrebbero un giorno rallentare il passaggio da occasionali rigidità a un'osteoartrite cronica e invalidante.
Citazione: Jiang, Y., Wang, Q., Yang, X. et al. CircFN1 modulates IL-1β-induced osteoarthritis through the miR-19b-3p/PTEN signaling axis. Sci Rep 16, 10710 (2026). https://doi.org/10.1038/s41598-026-45897-0
Parole chiave: osteoartrite, cartilagine, RNA non codificante, infiammazione, degenerazione articolare