Clear Sky Science · nl
CircFN1 moduleert IL-1β-geïnduceerde artrose via de miR-19b-3p/PTEN-signaleringsas
Waarom pijnlijke gewrichten ertoe doen
Artrose wordt vaak afgedaan als "slijtage", maar voor miljoenen mensen betekent het dagelijkse pijn, stijfheid en verlies van zelfstandigheid. Deze studie kijkt onder de motorkap van pijnlijke gewrichten en stelt een actuele vraag: waarom verslechteren sommige knieën en heupen zo sterk, en zouden we dat proces kunnen vertragen door het gedrag van bepaalde kleine RNA-moleculen in kraakbeencellen te veranderen?
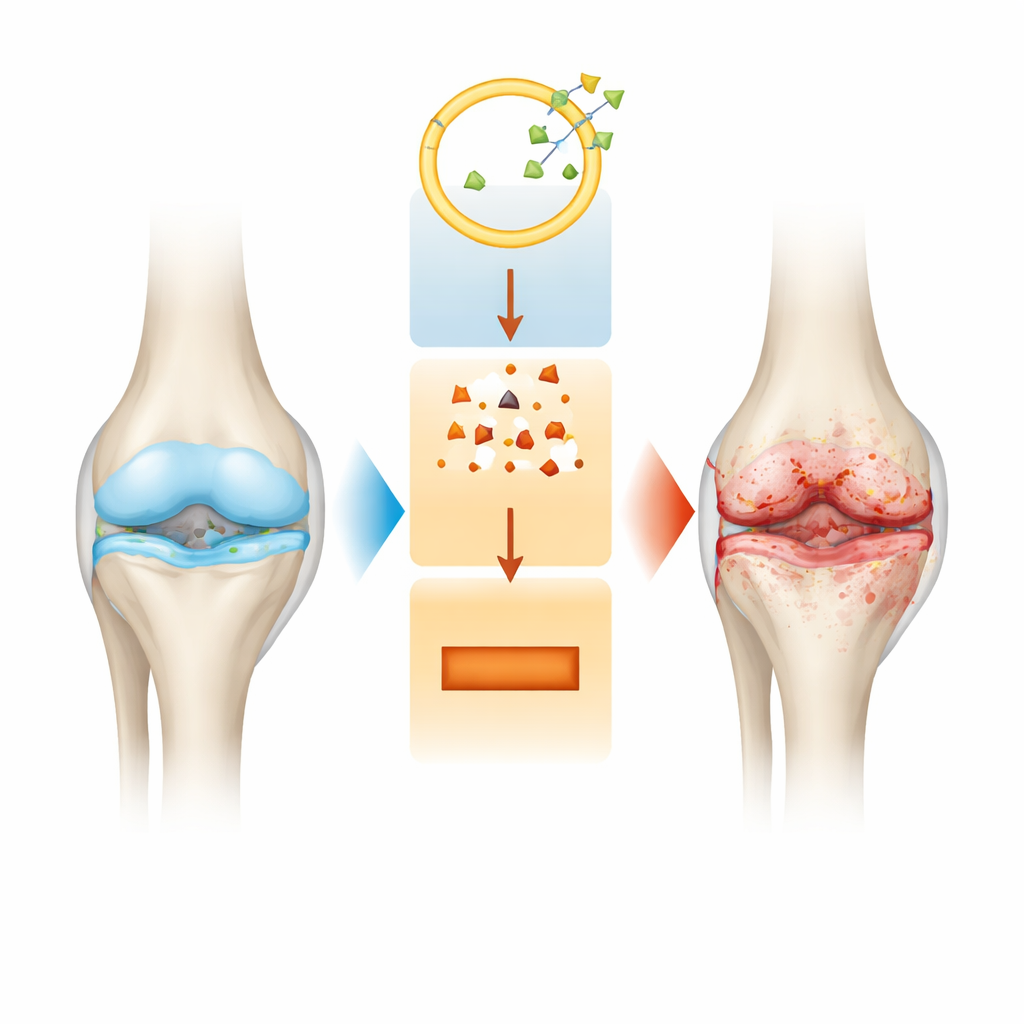
Een nader onderzoek van gewrichtsafbraak
Artrose is meer dan het dunner worden van kraakbeen. Naarmate de ziekte vordert verandert het hele gewricht: het gladde kussentje aan de uiteinden van botten slijt weg, het gewrichtsslijmvlies raakt ontstoken en het onderliggende bot herstructureert zich op manieren die de pijn kunnen verergeren. Huidige behandelingen verlichten vooral symptomen maar stoppen deze langzame structurele schade niet. Onderzoekers zoeken daarom naar moleculaire schakelaars in kraakbeencellen, chondrocyten genoemd, die mogelijk verklaren waarom deze cellen beginnen af te sterven en waarom de ondersteunende matrix rondom hen uiteenvalt.
De verborgen wereld van circulair RNA
In de afgelopen jaren ontdekten wetenschappers dat veel delen van ons genetisch materiaal niet tot eiwitten worden vertaald maar toch krachtige regelgevende rollen vervullen. Daarbij horen circulaire RNA’s—lusvormige moleculen die ongewoon stabiel zijn en vaak in specifieke weefsels overvloedig voorkomen. Het team achter dit artikel richtte zich op één zo’n molecuul, circFN1, dat in hogere niveaus voorkomt in menselijke kraakbeencellen die zijn blootgesteld aan het ontstekingssignaal IL‑1β, een stof die in het laboratorium vaak wordt gebruikt om artrose na te bootsen. Sequencing-experimenten die normale en IL‑1β‑behandelde chondrocyten vergeleken, toonden aan dat circFN1 een van de sterkst verhoogde circulaire RNA’s was, waardoor het een hoofdverdachte werd bij het aanjagen van gewrichtsschade.
Een driefasen moleculaire touwtrekwedstrijd
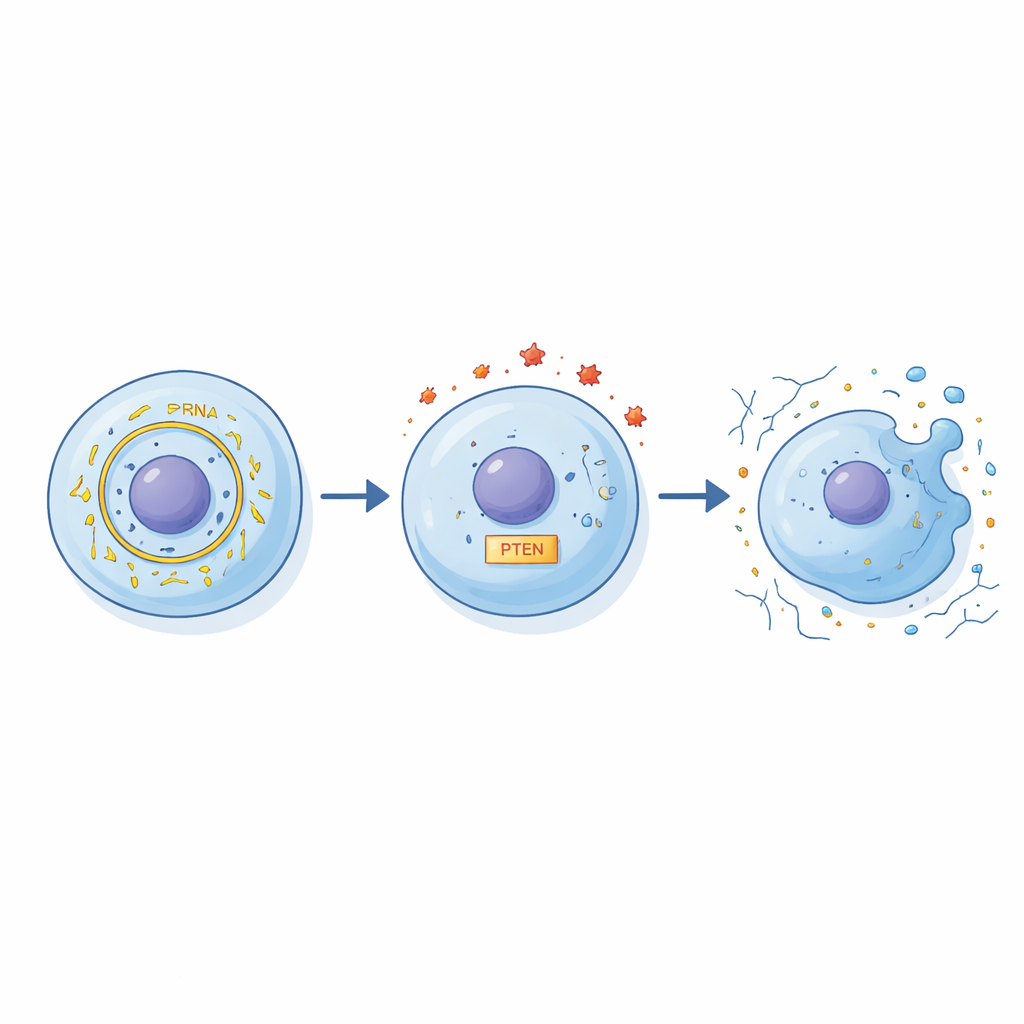
De onderzoekers ontrafelden een keten van interacties die circFN1 aan celschade koppelt. Eerst lieten ze zien dat circFN1 als een spons kan dienen voor een klein regulatorisch RNA genaamd miR‑19b‑3p, door het te binden en weg te houden. Normaal helpt miR‑19b‑3p de niveaus van PTEN te beheersen, een eiwit dat invloed heeft op celdood, ontsteking en het behoud van de matrix. Wanneer circFN1 stijgt, wordt meer miR‑19b‑3p opgeslorpt, wat op zijn beurt de activiteit van PTEN verandert en de balans tussen beschermende en schadelijke signalen in de cel verstoort. Via een reeks genetische "opschroef- en afschroef" experimenten toonden de auteurs aan dat deze circFN1–miR‑19b‑3p–PTEN-keten sterk bepaalt hoe chondrocyten reageren op inflammatoire stress.
Wat er gebeurt als de schakelaars worden omgezet
Om de functionele impact van deze route te testen, verlaagde het team doelbewust circFN1 in IL‑1β‑behandelde chondrocyten. Toen circFN1 werd verlaagd, overleefden meer cellen, ondergingen er minder geprogrammeerde celdood en werden belangrijke bouwstenen van kraakbeen, zoals het matrixeiwit aggrecan, beter behouden. Tegelijkertijd daalden moleculen die kraakbeen afbreken, zoals MMP‑13, en werd de omringende "soep" van ontstekingsstoffen zoals TNF‑α en IL‑6 minder hevig. Toen de onderzoekers ook miR‑19b‑3p en PTEN manipuleerden, werden deze beschermende veranderingen op voorspelbare wijze versterkt of verzwakt, wat het idee versterkt dat alle drie partners een verbonden regelkring vormen in plaats van geïsoleerd te werken.
Van kweekplaatjes naar toekomstige therapieën
Hoewel deze experimenten zijn uitgevoerd in gekweekte menselijke kraakbeencellen en niet in levende gewrichten, wijzen de bevindingen op een nieuw conceptueel aangrijpingspunt voor de behandeling van artrose. De studie suggereert dat verhoogd circFN1 de ontstekingsgedreven kraakbeenschade versterkt door de balans tussen miR‑19b‑3p en PTEN te herschikken. Simpel gezegd maakt een overschot aan dit circulaire RNA kraakbeencellen gevoeliger voor ontstekingsaanvallen en vatbaarder om af te sterven en hun ondersteunende matrix te verliezen. Als toekomstig werk in dieren en patiënten deze resultaten bevestigt, zou het meten van circFN1 kunnen helpen vroege gewrichtsschade te detecteren, en therapieën die circFN1 blokkeren of miR‑19b‑3p versterken, zouden het verval van incidentele stijfheid naar chronische, invaliderende artrose mogelijk kunnen vertragen.
Bronvermelding: Jiang, Y., Wang, Q., Yang, X. et al. CircFN1 modulates IL-1β-induced osteoarthritis through the miR-19b-3p/PTEN signaling axis. Sci Rep 16, 10710 (2026). https://doi.org/10.1038/s41598-026-45897-0
Trefwoorden: artrose, kraakbeen, niet-coderend RNA, ontsteking, gewrichtsdegeneratie