Clear Sky Science · fr
CircFN1 module l’arthrose induite par l’IL-1β via l’axe de signalisation miR-19b-3p/PTEN
Pourquoi les articulations douloureuses comptent
L’arthrose est souvent réduite à un « usure », mais pour des millions de personnes elle rime avec douleur quotidienne, raideur et perte d’autonomie. Cette étude ouvre le capot des articulations endolories et pose une question d’actualité : pourquoi certains genoux et hanches se détériorent-ils autant, et pourrait-on ralentir ce processus en modifiant le comportement de certains petits ARN à l’intérieur des cellules du cartilage ?
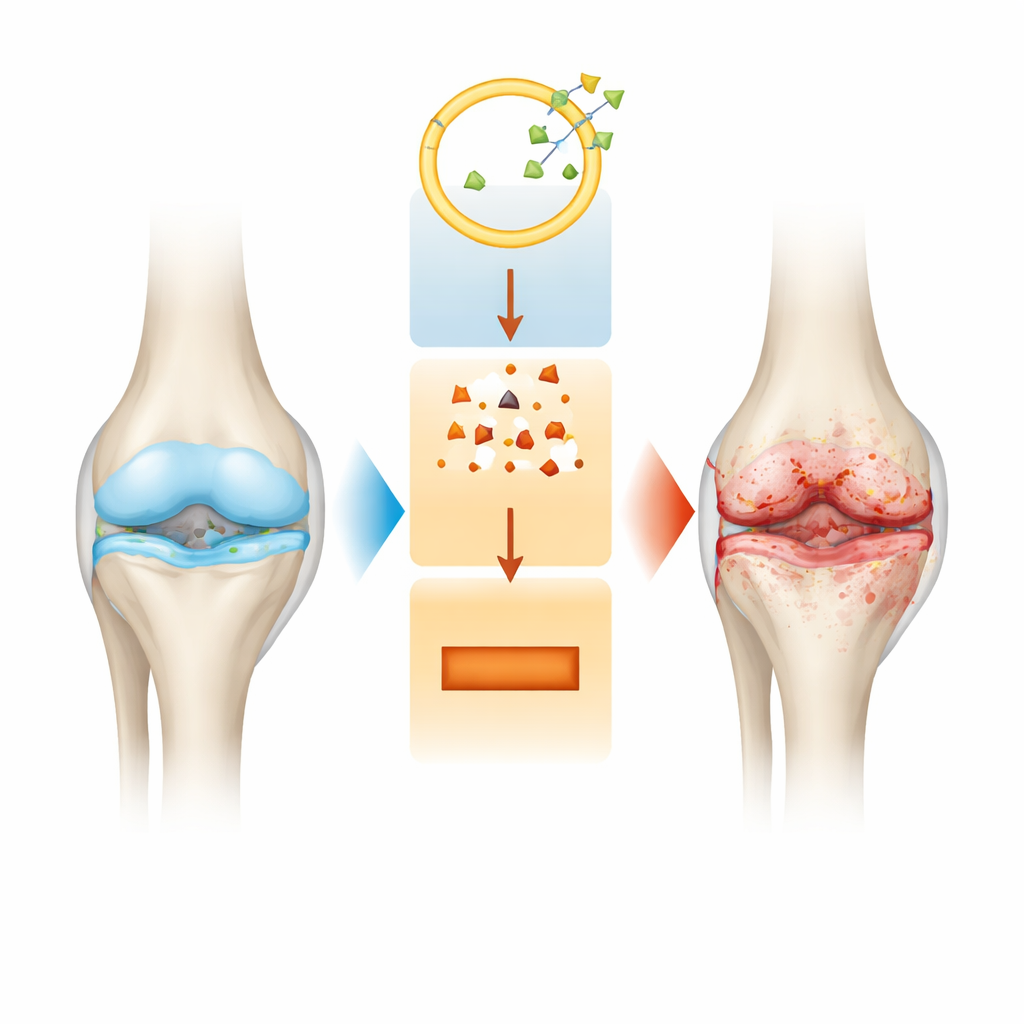
Un regard plus précis sur la dégradation articulaire
L’arthrose n’est pas seulement un amincissement du cartilage. À mesure que la maladie progresse, toute l’articulation se modifie : le coussinet lisse aux extrémités des os s’érode, la membrane articulaire s’enflamme et l’os sous-jacent se remodèle de façons qui peuvent aggraver la douleur. Les traitements actuels soulagent surtout les symptômes mais n’arrêtent pas ces dommages structurels lents. Les chercheurs cherchent donc des interrupteurs moléculaires dans les cellules du cartilage, appelées chondrocytes, qui pourraient expliquer pourquoi ces cellules commencent à mourir et pourquoi la matrice qui les soutient se dégrade.
Le monde caché des ARN circulaires
Ces dernières années, les scientifiques ont découvert que de nombreux segments de notre matériel génétique ne deviennent jamais des protéines mais jouent néanmoins des rôles régulateurs puissants. Parmi eux figurent les ARN circulaires — des molécules en boucle particulièrement stables et souvent abondantes dans des tissus spécifiques. L’équipe de cette étude s’est intéressée à l’une de ces molécules, circFN1, présente à des niveaux plus élevés dans les chondrocytes humains exposés au signal inflammatoire IL‑1β, un agent couramment utilisé pour reproduire l’arthrose en laboratoire. Des expériences de séquençage comparant des chondrocytes normaux et traités par l’IL‑1β ont montré que circFN1 faisait partie des ARN circulaires les plus fortement augmentés, en faisant un suspect majeur dans l’alimentation des lésions articulaires.
Une lutte moléculaire en trois étapes
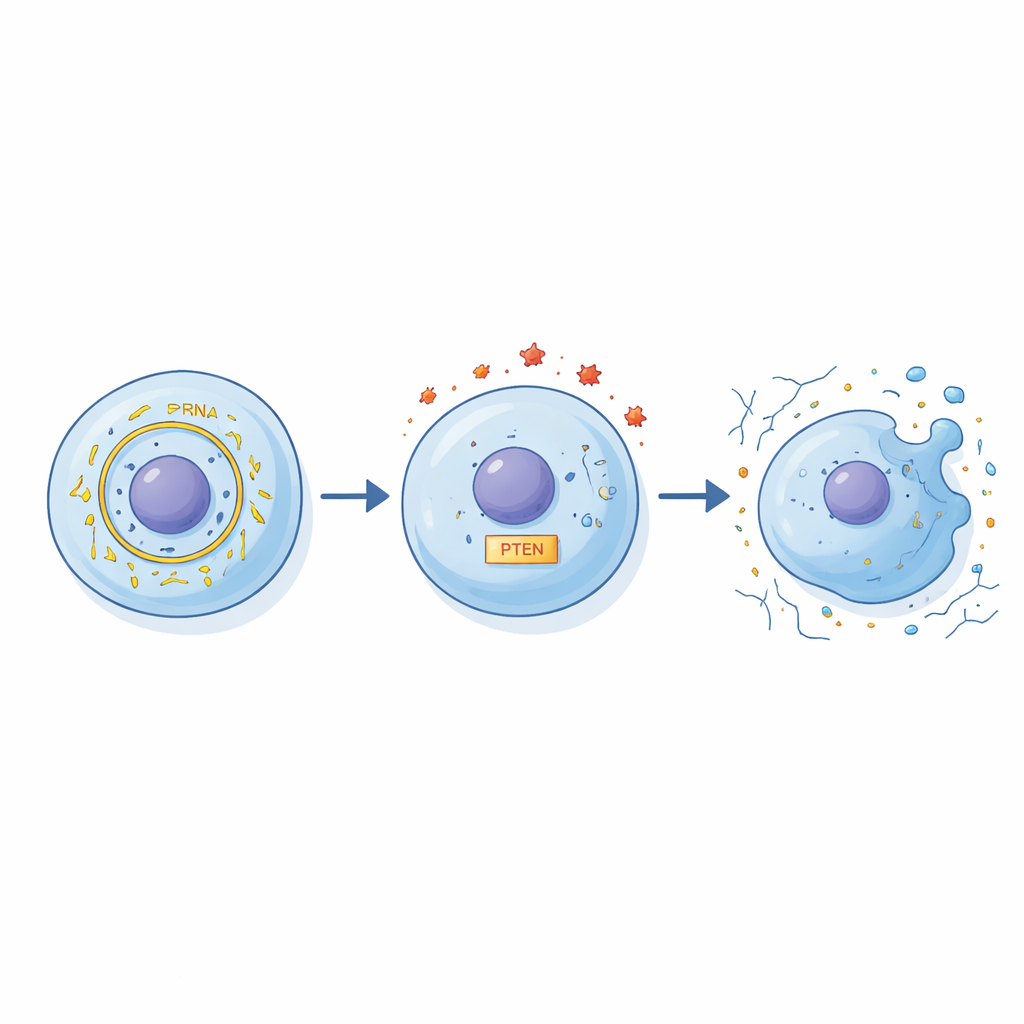
Les chercheurs ont mis au jour une chaîne d’interactions reliant circFN1 à la lésion cellulaire. D’abord, ils ont montré que circFN1 peut agir comme une éponge pour un petit ARN régulateur appelé miR‑19b‑3p, en le liant et le séquestrant. Normalement, miR‑19b‑3p contribue à contrôler les niveaux de PTEN, une protéine qui influence la survie cellulaire, l’inflammation et le maintien de la matrice. Lorsque les niveaux de circFN1 augmentent, plus de miR‑19b‑3p est absorbé, ce qui modifie ensuite l’activité de PTEN et perturbe l’équilibre entre signaux protecteurs et nocifs dans la cellule. À travers une série d’expériences génétiques d’« accentuation et d’atténuation », les auteurs ont démontré que cette chaîne circFN1–miR‑19b‑3p–PTEN influence fortement la réponse des chondrocytes au stress inflammatoire.
Que se passe-t-il lorsque les interrupteurs sont activés ou désactivés
Pour tester l’impact fonctionnel de cette voie, l’équipe a réduit délibérément circFN1 dans des chondrocytes traités par l’IL‑1β. Lorsque circFN1 était abaissé, davantage de cellules survivaient, moins entrelaient la mort programmée, et des éléments clés du cartilage, comme la protéine de matrice aggrécane, étaient mieux préservés. Parallèlement, les molécules qui dégradent le cartilage, telles que MMP‑13, diminuaient, et le « cocktail » de substances inflammatoires environnantes, comme le TNF‑α et l’IL‑6, devenait moins intense. Lorsque les chercheurs ont également modifié miR‑19b‑3p et PTEN, ces changements protecteurs se sont renforcés ou affaiblis de façon prévisible, renforçant l’idée que ces trois partenaires forment un circuit régulateur connecté plutôt qu’agissant isolément.
Des boîtes de culture aux thérapies futures
Bien que ces expériences aient été réalisées sur des cellules de cartilage humain en culture et non dans des articulations vivantes, les résultats pointent vers un nouveau levier conceptuel pour le traitement de l’arthrose. L’étude suggère qu’un niveau élevé de circFN1 amplifie les lésions cartilagineuses induites par l’inflammation en réarrangeant l’équilibre entre miR‑19b‑3p et PTEN. En termes simples, un excès de cet ARN circulaire rend les chondrocytes plus vulnérables aux agressions inflammatoires et plus enclins à mourir et à perdre leur matrice de soutien. Si des travaux futurs chez l’animal et chez l’humain confirment ces résultats, la mesure de circFN1 pourrait aider à détecter les lésions articulaires précoces, et des thérapies visant à bloquer circFN1 ou à renforcer miR‑19b‑3p pourraient un jour ralentir la progression d’une raideur occasionnelle vers une arthrose chronique et invalidante.
Citation: Jiang, Y., Wang, Q., Yang, X. et al. CircFN1 modulates IL-1β-induced osteoarthritis through the miR-19b-3p/PTEN signaling axis. Sci Rep 16, 10710 (2026). https://doi.org/10.1038/s41598-026-45897-0
Mots-clés: arthrose, cartilage, ARN non codant, inflammation, dégénérescence articulaire