Clear Sky Science · he
CircFN1 מווסתת אוסטאוארתריטיס המושר על‑ידי IL-1β דרך ציר האיתות miR-19b-3p/PTEN
מדוע מפרקים כואבים מעניינים
אוסטאוארתריטיס נתפסת לעתים כ"בלאי", אבל עבור מיליוני אנשים היא משמעותה כאב יומי, נוקשות ואובדן עצמאות. המחקר הזה בוחן לעומק מפרקים כואבים ושואל שאלה אקטואלית: מדוע מפרקים כמו ברכיים וירכיים מתדרדרים כל כך, והאם אפשר לשחק תפקיד בתהליך הזה על‑ידי שינוי אופן הפעולה של מולקולות RNA זעירות בתוך תאי הסחוס?
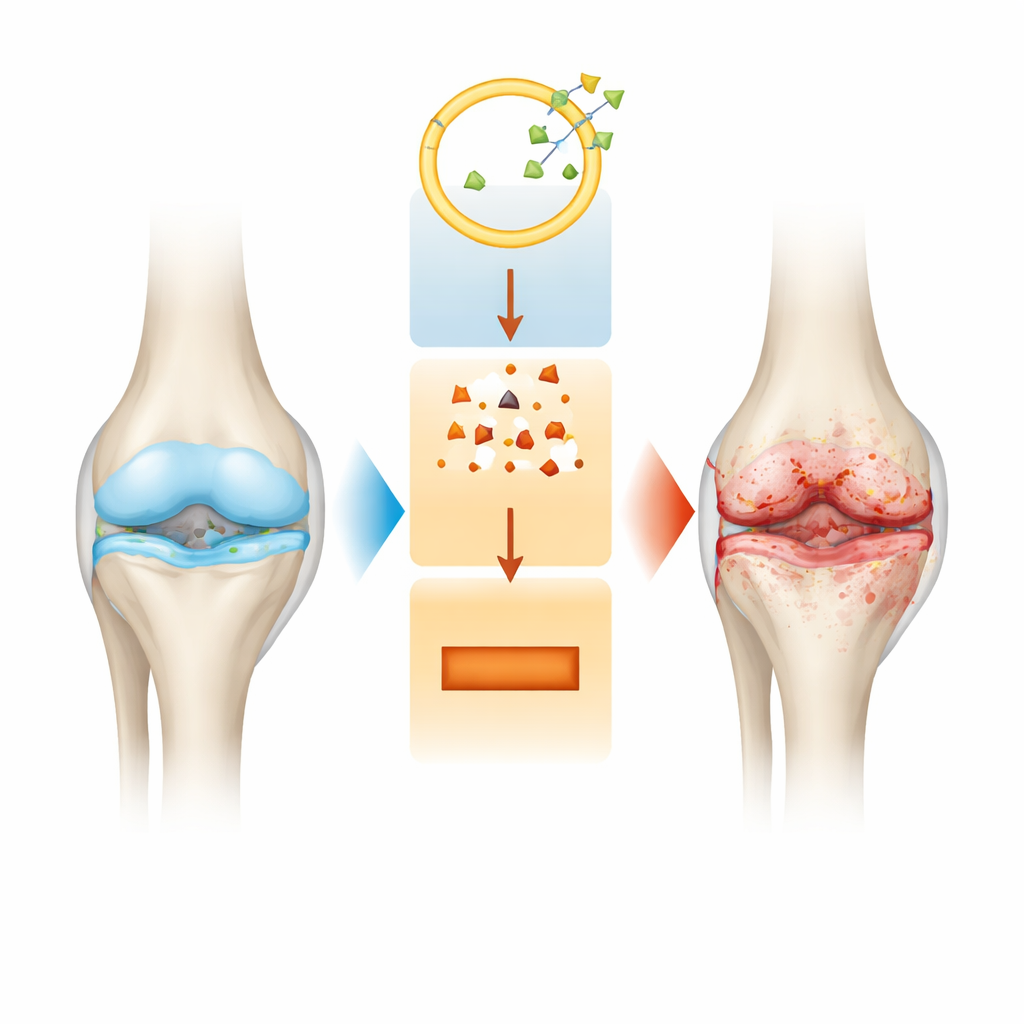
מבט קרוב יותר על התפוררות המפרק
אוסטאוארתריטיס היא יותר מעיבוי או דקיקה של הסחוס. כשהמחלה מתקדמת, כל המפרק משתנה: כרית החלקה בקצות העצמות נשחקת, רירית המפרק נעשית דלקתית, והעצם שמתחת לסחוס משנה את מבנהו באופן שיכול להחמיר את הכאב. הטיפולים הקיימים מקלים בעיקר על התסמינים אך אינם עוצרים את הנזק המבני האיטי הזה. לכן חוקרים מחפשים מתגים מולקולריים בתוך תאי הסחוס, הקרויים כונדרוציטים, שיסבירו מדוע תאים אלה מתחילים להידרדר ומדוע המטריצה התומכת בהם מתפרקת.
עולם מוסתר של RNA מעגלי
בשנים האחרונות גילו מדענים שחלקים רבים מהחומר הגנטי שלנו אינם מומרים לחלבונים אך ממלאים תפקידים רגולטוריים חזקים. בין אלה יש RNAs מעגליים — מולקולות לולאתיות שנחשבות ליציבות במיוחד ולעתים עשירות ברקמות מסוימות. הקבוצה מאחורי מאמר זה התמקדה במולקולה כזו, circFN1, שנמצאה ברמות גבוהות יותר בתאי סחוס אנושיים שנחשפו לאות הדלקתי IL‑1β, חומר שמשמש לעתים קרובות לחקות אוסטאוארתריטיס במעבדה. ניסויי רצף שהשוו כונדרוציטים רגילים לכאלה שטופלו ב‑IL‑1β הראו ש‑circFN1 הוא אחד ה‑circRNA שהוגברו בחוזקה, מה שהפך אותו לחשוד מרכזי בהנעת נזק למפרק.
משחק כוח מולקולרי בשלושה שלבים
החוקרים חשפו שרשרת אינטראקציות שמקשרת בין circFN1 לנזק תאי. ראשית, הראו ש‑circFN1 יכול לשמש כ"ספוג" ל‑miR‑19b‑3p, RNA רגולטורי קטן, בכך שהוא קושר אותו ומסיטו. בדרך רגילה, miR‑19b‑3p מסייע לשלוט ברמות PTEN, חלבון המשפיע על השרידות התאית, דלקת ותחזוקת המטריצה. כאשר רמות circFN1 עולות, יותר miR‑19b‑3p נספג, מה שמשנה את פעילות PTEN ומפר את האיזון בין אותות מגוננים להרסניים בתא. באמצעות סדרת ניסויים של "הגברה והחלשה" גנטית, המחברים הראו כי ציר circFN1–miR‑19b‑3p–PTEN מעצב במידה ניכרת את תגובת הכונדרוציטים ללחץ דלקתי.
מה קורה כשהמפתחים מגלגלים
כדי לבדוק את ההשפעה התפקודית של המסלול הזה, הצוות הפחית בכוונה את circFN1 בכונדרוציטים שטופלו ב‑IL‑1β. כשהורידו את circFN1, יותר תאים שרדו, פחות תאים עברו מוות מתוכנן, ורכיבי מבנה מרכזיים של סחוס, כגון חלבון המטריצה אג'רקאן, נשמרו טוב יותר. במקביל, מולקולות שמפרקות סחוס כמו MMP‑13 ירדו, ו"מרק" החומרים הדלקתיים סביבן כגון TNF‑α ו‑IL‑6 נחלש. כששינו גם את miR‑19b‑3p ו‑PTEN, השינויים המגנים התחזקו או נחלשו באופן צפוי, מה שמחזק את הרעיון ששלושת השותפים הללו מהווים מעגל רגולטורי מקושר ולא פועלים בנפרד.
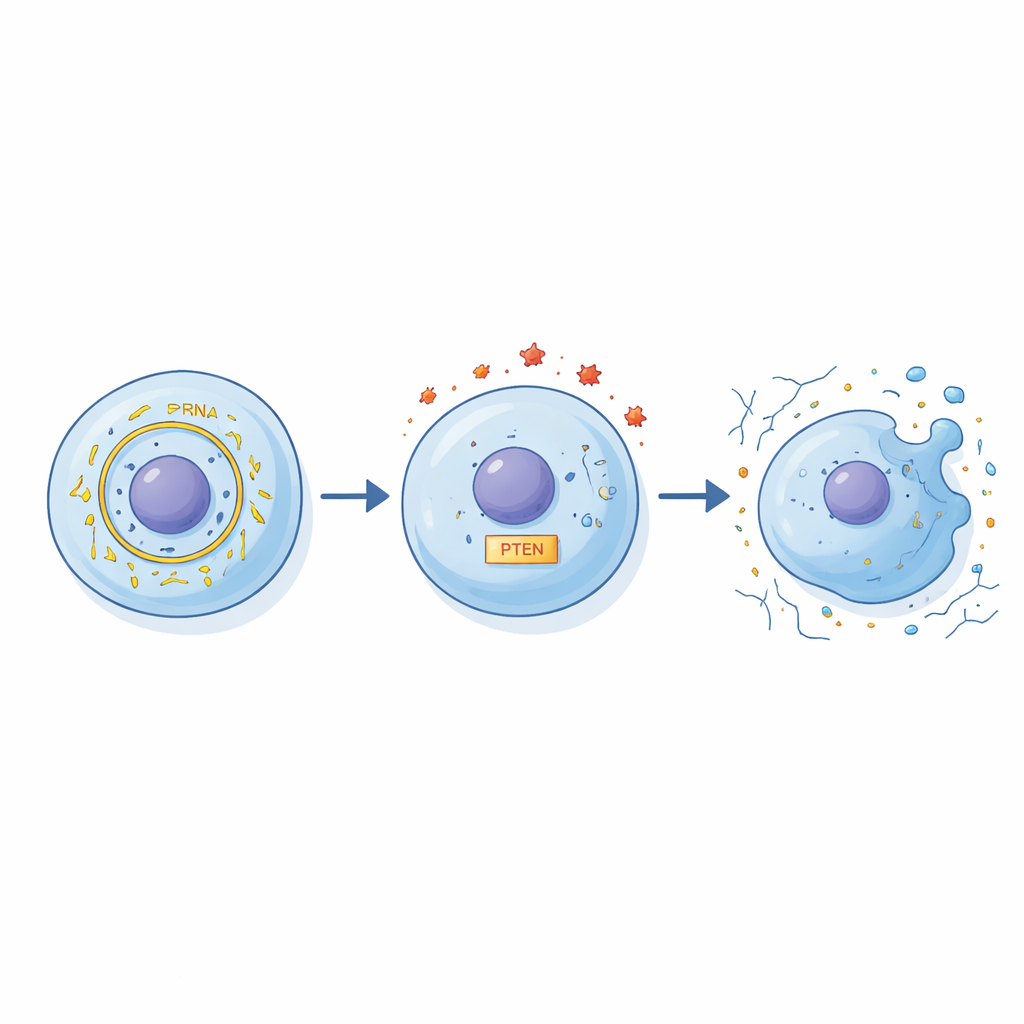
מצלחות תאיות אל טיפולים עתידיים
אמנם הניסויים הללו בוצעו בתאי סחוס אנושיים ממוקרנים ולא במפרקים חיים, אך הממצאים מצביעים על מנוף קונספטואלי חדש לטיפול באוסטאוארתריטיס. המחקר מציע שרמות מוגברות של circFN1 ממחישות ומגבירות את נזק הסחוס המונע על‑ידי דלקת על‑ידי שינוי האיזון בין miR‑19b‑3p ל‑PTEN. בפשטות, עודף RNA מעגלי זה מגדיל את הפגיעות של תאי הסחוס לפגיעות דלקתיות והופך אותם ליותר פגיעים למוות ולשיחור מטריצתם התומכת. אם מחקרים עתידיים בחיות ובחולים יאמתו ממצאים אלה, מדידת circFN1 עשויה לעזור לזהות נזק מוקדם למפרק, וטיפולים שנועדו לחסום את circFN1 או להגביר את miR‑19b‑3p עשויים יום אחד להאט את ההידרדרות מעתקיעות מזדמנת לאוסטאוארתריטיס כרוני ומניעה.
ציטוט: Jiang, Y., Wang, Q., Yang, X. et al. CircFN1 modulates IL-1β-induced osteoarthritis through the miR-19b-3p/PTEN signaling axis. Sci Rep 16, 10710 (2026). https://doi.org/10.1038/s41598-026-45897-0
מילות מפתח: אוסטאוארתריטיס, סחוס, RNA שאינו מקודד, דלקת, ניוון מפרקים