Clear Sky Science · ru
CircFN1 модулирует остеоартрит, индуцированный IL-1β, через сигнальную ось miR-19b-3p/PTEN
Почему болящие суставы важны
Остеоартрит часто сводят к «износу», но для миллионов людей это означает ежедневную боль, скованность и утрату самостоятельности. В этом исследовании заглядывают под капот болезненных суставов и задают своевременный вопрос: почему некоторые колени и бедра так сильно разрушаются и можно ли замедлить этот процесс, изменив поведение некоторых крошечных молекул РНК внутри хондроцитов — клеток хряща?
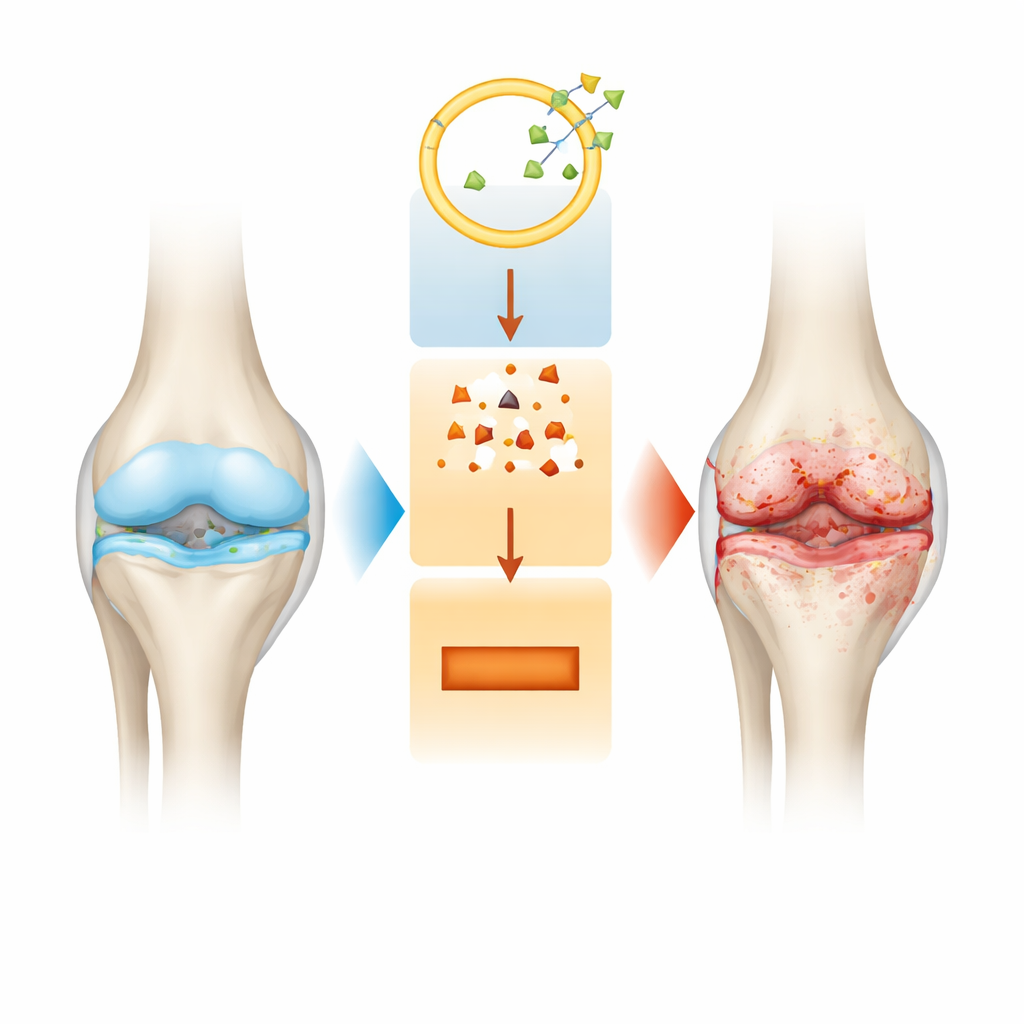
Более пристальный взгляд на разрушение сустава
Остеоартрит — это не только истончение хряща. По мере прогрессирования болезни меняется весь сустав: гладкая подушка на концах костей разрушается, оболочка сустава воспаляется, а подлежащая кость перестраивается так, что это может усиливать боль. Современные методы лечения в основном облегчают симптомы, но не останавливают медленное структурное повреждение. Поэтому исследователи ищут молекулярные переключатели внутри хондроцитов, которые могли бы объяснить, почему эти клетки начинают гибнуть и почему разрушается внеклеточный матрикс вокруг них.
Скрытый мир кольцевых РНК
В последние годы учёные обнаружили, что многие участки нашего генетического материала не превращаются в белки, но при этом выполняют мощные регуляторные функции. Среди них — кольцевые РНК: замкнутые молекулы, обладающие необычной стабильностью и часто обильные в определённых тканях. Авторы статьи сосредоточились на одной такой молекуле — circFN1, уровень которой повышался в человеческих хондроцитах при воздействии провоспалительного сигнала IL‑1β, химического агента, часто используемого в лабораториях для моделирования остеоартрита. Секвенирующие эксперименты, сравнивающие нормальные и обработанные IL‑1β хондроциты, показали, что circFN1 является одной из наиболее сильно увеличенных циркулярных РНК, что делает её главным подозреваемым в продвижении повреждения сустава.
Трёхступенчатая молекулярная перетягивание каната
Исследователи выявили цепочку взаимодействий, связывающую circFN1 с клеточным повреждением. Во-первых, они показали, что circFN1 может действовать как губка для малой регуляторной РНК miR‑19b‑3p, связывая и сеquestрируя её. Как правило, miR‑19b‑3p помогает контролировать уровни белка PTEN, который влияет на выживание клеток, воспаление и поддержание матрикса. Когда уровень circFN1 растёт, больше miR‑19b‑3p поглощается, что, в свою очередь, меняет активность PTEN и нарушает баланс между защитными и вредными сигналами в клетке. Серия генетических экспериментов типа «усилить — ослабить» показала, что цепочка circFN1–miR‑19b‑3p–PTEN существенно формирует реакцию хондроцитов на воспалительный стресс.
Что происходит, когда переключатели меняют положение
Чтобы проверить функциональное влияние этого пути, команда сознательно снизила уровень circFN1 в хондроцитах, обработанных IL‑1β. При уменьшении circFN1 больше клеток выживало, меньше подвергалось программируемой гибели, и ключевые строительные блоки хряща, такие как матричный белок аггрекан, сохранялись лучше. Одновременно снизились молекулы, разрушающие хрящ, например MMP‑13, а вокруг уменьшилась интенсивность «супа» провоспалительных веществ, таких как TNF‑α и IL‑6. Когда исследователи также меняли уровни miR‑19b‑3p и PTEN, эти защитные изменения усиливались или ослабевали предсказуемым образом, что укрепляет идею о том, что все три компонента образуют связанную регуляторную цепь, а не действуют изолированно.
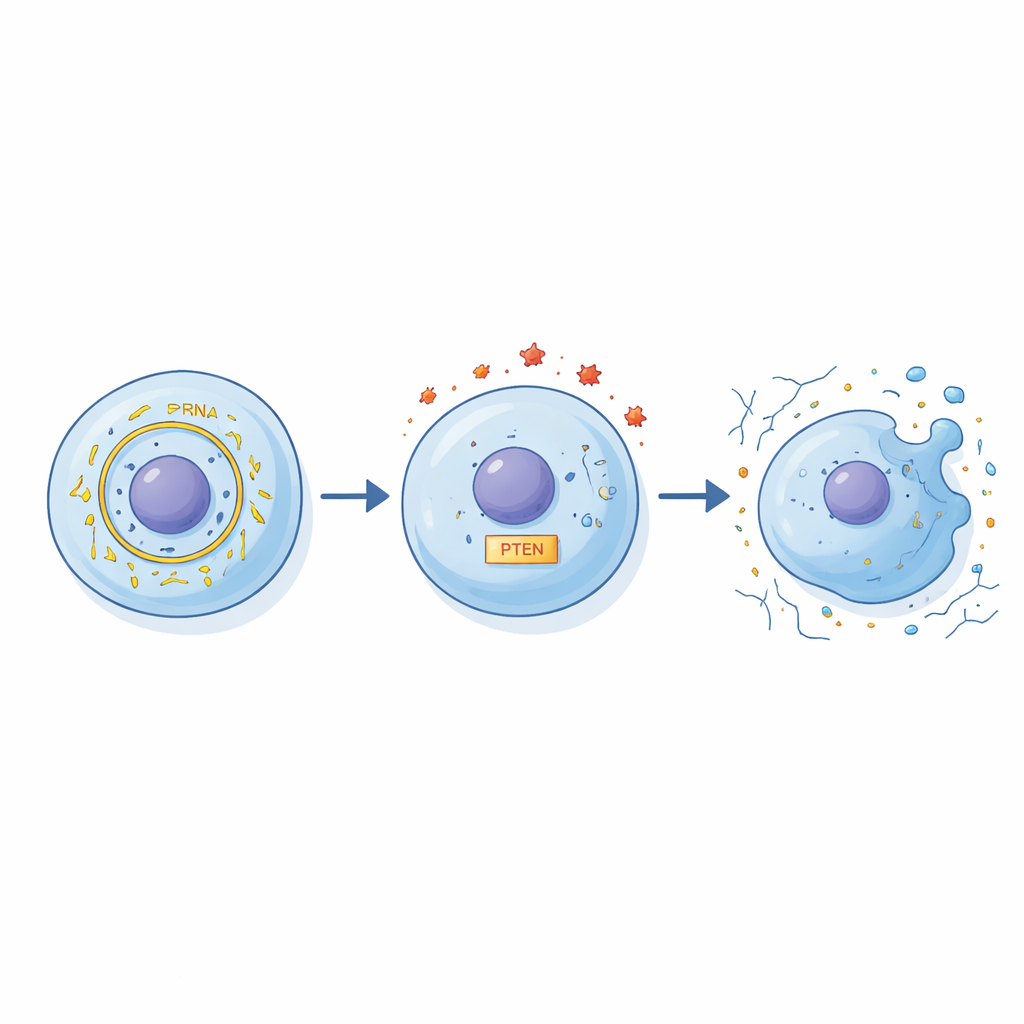
От клеточных чашек к будущим терапиям
Хотя эксперименты проводились в культурах человеческих хондроцитов, а не в живых суставах, результаты указывают на новую концептуальную точку приложения для лечения остеоартрита. Исследование предполагает, что повышенный circFN1 усиливает воспалением‑опосредованное повреждение хряща, перестраивая баланс между miR‑19b‑3p и PTEN. Проще говоря, избыток этой кольцевой РНК делает хондроциты более уязвимыми к воспалительным воздействиям, склонными к гибели и потере поддерживающего матрикса. Если будущие исследования на животных и пациентах подтвердят эти результаты, измерение circFN1 может помочь обнаруживать раннее повреждение сустава, а терапевтические подходы, нацеленные на блокировку circFN1 или повышение miR‑19b‑3p, в перспективе могут замедлить переход от эпизодической скованности к хроническому, инвалидизирующему остеоартриту.
Цитирование: Jiang, Y., Wang, Q., Yang, X. et al. CircFN1 modulates IL-1β-induced osteoarthritis through the miR-19b-3p/PTEN signaling axis. Sci Rep 16, 10710 (2026). https://doi.org/10.1038/s41598-026-45897-0
Ключевые слова: остеоартрит, хрящ, некодирующая РНК, воспаление, дегенерация сустава