Clear Sky Science · sv
CircFN1 påverkar IL-1β‑inducerad artros via miR-19b-3p/PTEN‑signalvägen
Varför värkande leder betyder något
Artros avfärdas ofta som "slitage", men för miljontals människor innebär det daglig smärta, stelhet och förlorad självständighet. Denna studie skruvar upp locket på ömma leder och ställer en aktuell fråga: varför försämras vissa knän och höfter så mycket, och skulle vi kunna bromsa den processen genom att ändra hur vissa små RNA‑molekyler beter sig inne i broskceller?
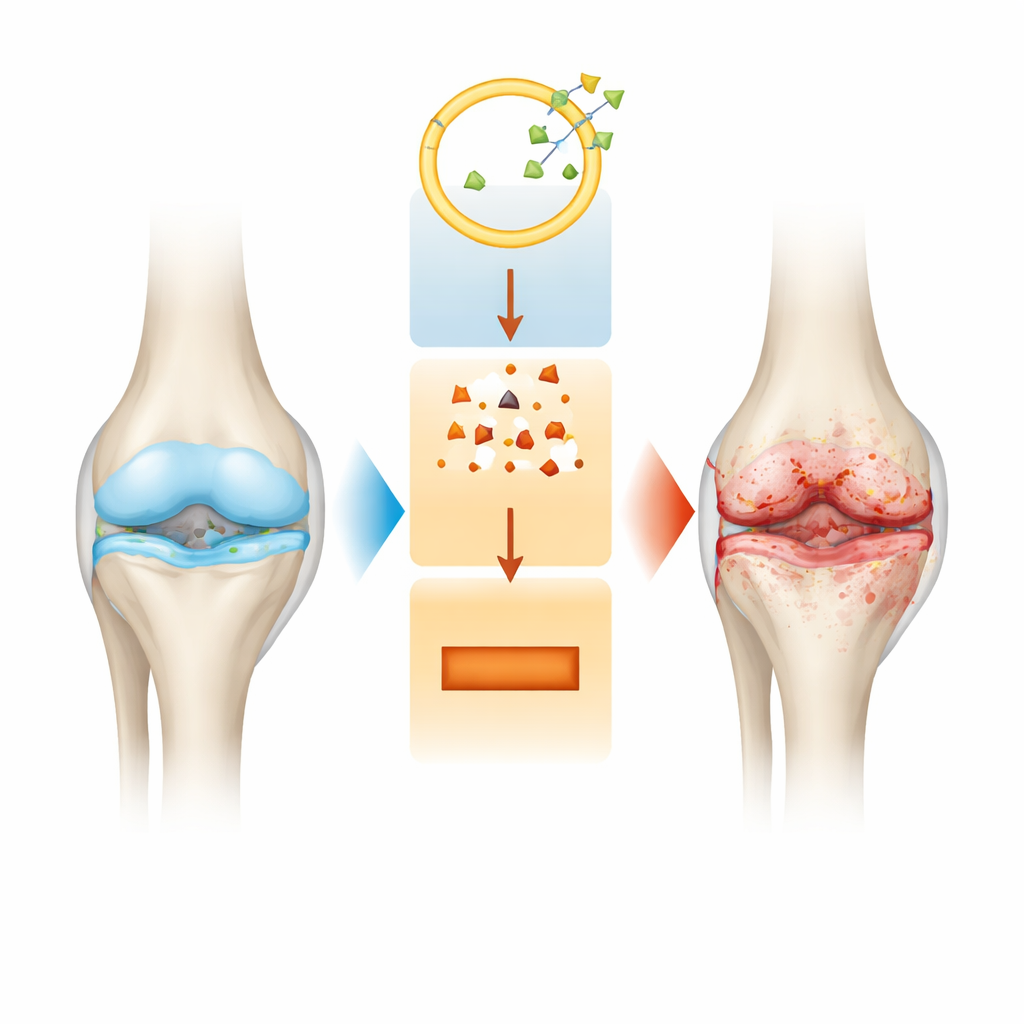
Närmare granskning av lednedbrytning
Artros handlar om mer än tunnare brosk. När sjukdomen framskrider förändras hela leden: den släta dämpningen på benen nöts bort, ledens slemhinna blir inflammerad och underliggande ben ombyggs på sätt som kan förvärra smärtan. Dagens behandlingar lindrar främst symtomen men stoppar inte denna långsamma strukturella skada. Forskare söker därför efter molekylära reglage inne i broskcellerna, så kallade kondrocyter, som kan förklara varför dessa celler börjar dö och varför den omgivande matrisen bryts ned.
Cirkulärt RNA:s dolda värld
Under de senaste åren har forskare upptäckt att många delar av vårt genetiska material aldrig blir proteiner men ändå spelar kraftfulla reglerande roller. Bland dem finns cirkulära RNA — slingformade molekyler som är ovanligt stabila och ofta rikliga i specifika vävnader. Forskargruppen bakom denna artikel fokuserade på en sådan molekyl, circFN1, som förekommer i högre nivåer i mänskliga broskceller exponerade för det inflammatoriska signalämnet IL‑1β, en kemisk signal som ofta används för att efterlikna artros i laboratorium. Sekvenseringsexperiment som jämförde normala och IL‑1β‑behandlade kondrocyter visade att circFN1 var en av de cirkulära RNA som ökade mest, vilket gör den till en huvudmisstänkt i drivandet av ledskador.
En trestegs molekylär dragkamp
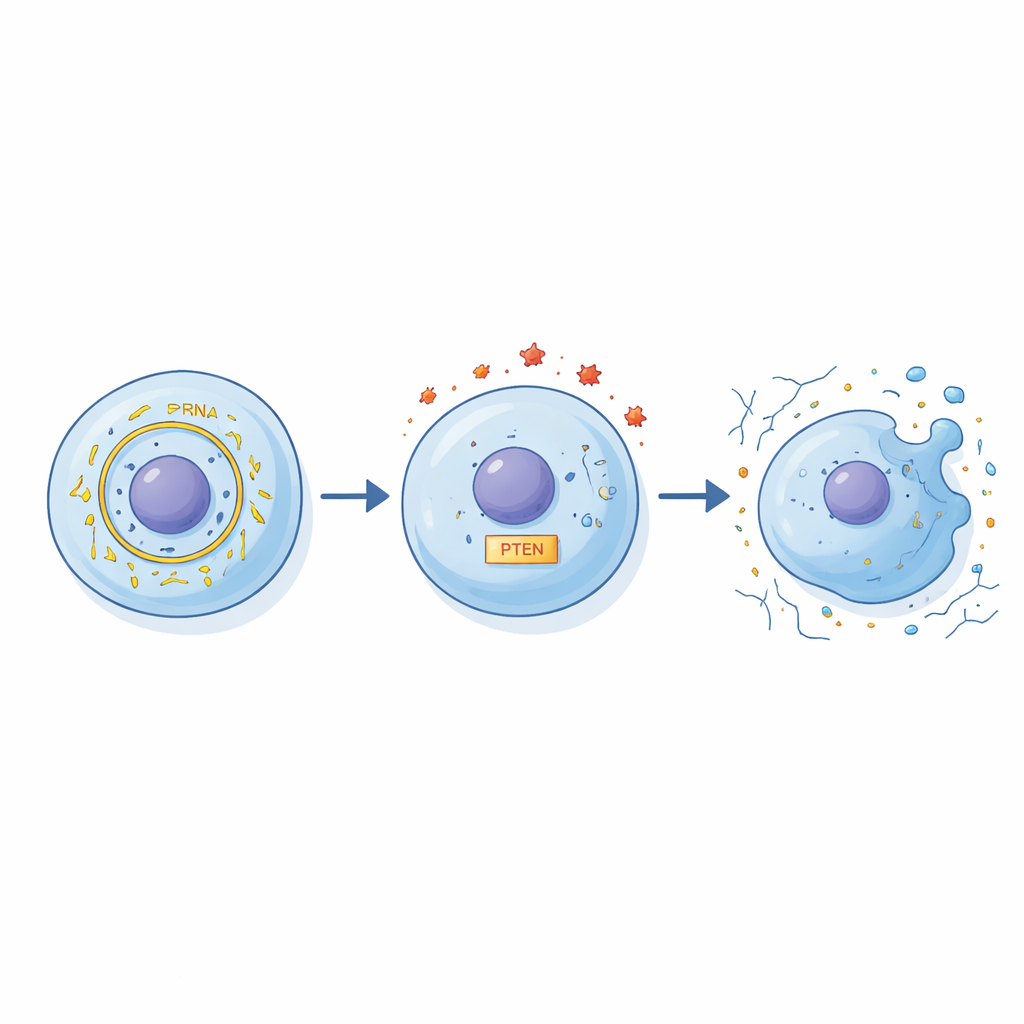
Forskarna avslöjade en kedja av interaktioner som kopplar circFN1 till cellskada. För det första visade de att circFN1 kan fungera som en svamp för ett litet regulatoriskt RNA kallat miR‑19b‑3p, genom att binda upp och inaktivera det. Normalt hjälper miR‑19b‑3p till att reglera nivåerna av PTEN, ett protein som påverkar cellsurvival, inflammation och underhåll av matrisen. När circFN1‑nivåerna stiger binds mer miR‑19b‑3p upp, vilket i sin tur ändrar PTEN:s aktivitet och rubbar balansen mellan skyddande och skadliga signaler i cellen. Genom en serie genetiska ”upp‑ och nedreglerings”‑experiment visade författarna att denna circFN1–miR‑19b‑3p–PTEN‑kedja starkt påverkar hur kondrocyterna svarar på inflammatorisk stress.
Vad som händer när reglagen vrids om
För att testa den funktionella betydelsen av denna väg minskade teamet medvetet circFN1 i IL‑1β‑behandlade kondrocyter. När circFN1 sänktes överlevde fler celler, färre gick in i programmerad celldöd, och viktiga byggstenar i brosket, såsom matrisproteinet aggrekan, bevarades bättre. Samtidigt sjönk nivåerna av molekyler som bryter ned brosk, som MMP‑13, och den omgivande ”soppan” av inflammatoriska substanser som TNF‑α och IL‑6 blev mindre intensiv. När forskarna även förändrade miR‑19b‑3p och PTEN förstärktes eller försvagades dessa skyddande effekter på förutsägbara sätt, vilket stärker idén att de tre aktörerna bildar en sammanlänkad reglerkrets snarare än att verka isolerat.
Från cellskålar till framtida behandlingar
Även om dessa experiment utfördes i odlade mänskliga broskceller snarare än i levande leder pekar resultaten mot ett nytt konceptuellt grepp för behandling av artros. Studien antyder att förhöjd circFN1 förstärker inflammationsdriven brosknedbrytning genom att omfördela balansen mellan miR‑19b‑3p och PTEN. Enkelt uttryckt gör ett överskott av detta cirkulära RNA broskceller mer sårbara för inflammatoriska angrepp och mer benägna att dö och förlora sin stödjande matris. Om framtida arbete i djur och patienter bekräftar dessa fynd, skulle mätning av circFN1 kunna hjälpa till att upptäcka tidiga ledskador, och terapier som blockerar circFN1 eller stärker miR‑19b‑3p skulle en dag kunna bromsa glidningen från sporadisk stelhet till kronisk, invalidiserande artros.
Citering: Jiang, Y., Wang, Q., Yang, X. et al. CircFN1 modulates IL-1β-induced osteoarthritis through the miR-19b-3p/PTEN signaling axis. Sci Rep 16, 10710 (2026). https://doi.org/10.1038/s41598-026-45897-0
Nyckelord: artros, brosk, icke-kodande RNA, inflammation, lednedbrytning