Clear Sky Science · es
CircFN1 modula la osteoartritis inducida por IL-1β a través del eje de señalización miR-19b-3p/PTEN
Por qué importan las articulaciones doloridas
La osteoartritis a menudo se desestima como “desgaste”, pero para millones de personas significa dolor diario, rigidez y pérdida de independencia. Este estudio examina en detalle las articulaciones doloridas y plantea una pregunta oportuna: ¿por qué algunas rodillas y caderas se deterioran tanto, y podríamos ralentizar ese proceso modificando el comportamiento de ciertas moléculas pequeñas de ARN dentro de las células del cartílago?
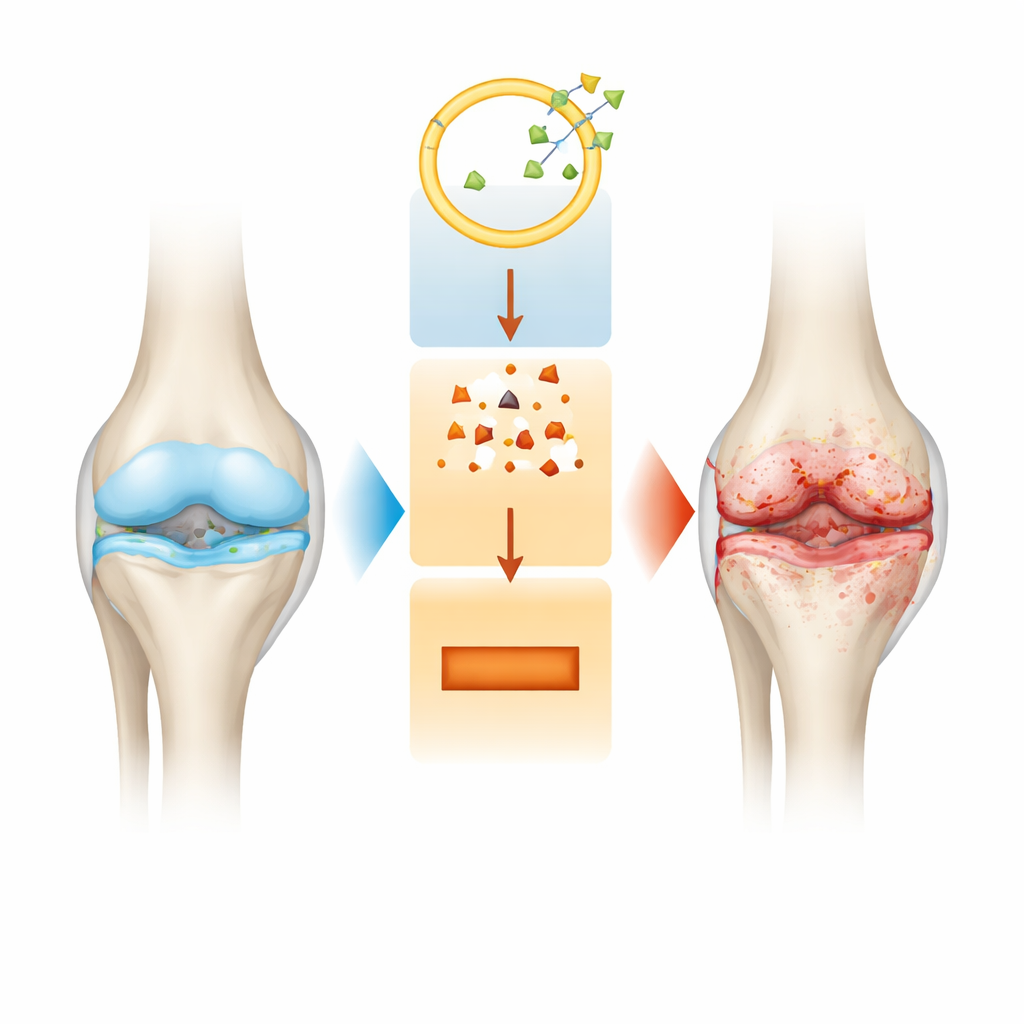
Una mirada más cercana a la degradación articular
La osteoartritis es más que un adelgazamiento del cartílago. A medida que la enfermedad avanza, toda la articulación cambia: la superficie lisa en los extremos de los huesos se erosiona, el revestimiento de la articulación se inflama y el hueso subyacente se remodela de maneras que pueden agravar el dolor. Los tratamientos actuales alivian principalmente los síntomas pero no detienen este lento daño estructural. Por ello, los investigadores buscan interruptores moleculares dentro de las células del cartílago, llamadas condrocitos, que puedan explicar por qué estas células comienzan a morir y por qué la matriz de soporte que las rodea se descompone.
El mundo oculto del ARN circular
En los últimos años, los científicos han descubierto que muchos tramos de nuestro material genético no llegan a convertirse en proteínas, pero aun así desempeñan papeles regulatorios potentes. Entre ellos están los ARN circulares: moléculas en bucle que son inusualmente estables y con frecuencia abundantes en tejidos concretos. El equipo detrás de este trabajo se centró en una de estas moléculas, circFN1, que se encontró en niveles más altos en condrocitos humanos expuestos a la señal inflamatoria IL‑1β, un compuesto comúnmente usado para imitar la osteoartritis en el laboratorio. Experimentos de secuenciación comparando condrocitos normales y tratados con IL‑1β mostraron que circFN1 fue uno de los ARN circulares con mayor aumento, lo que lo convierte en un sospechoso principal en la promoción del daño articular.
Una batalla molecular de tres pasos
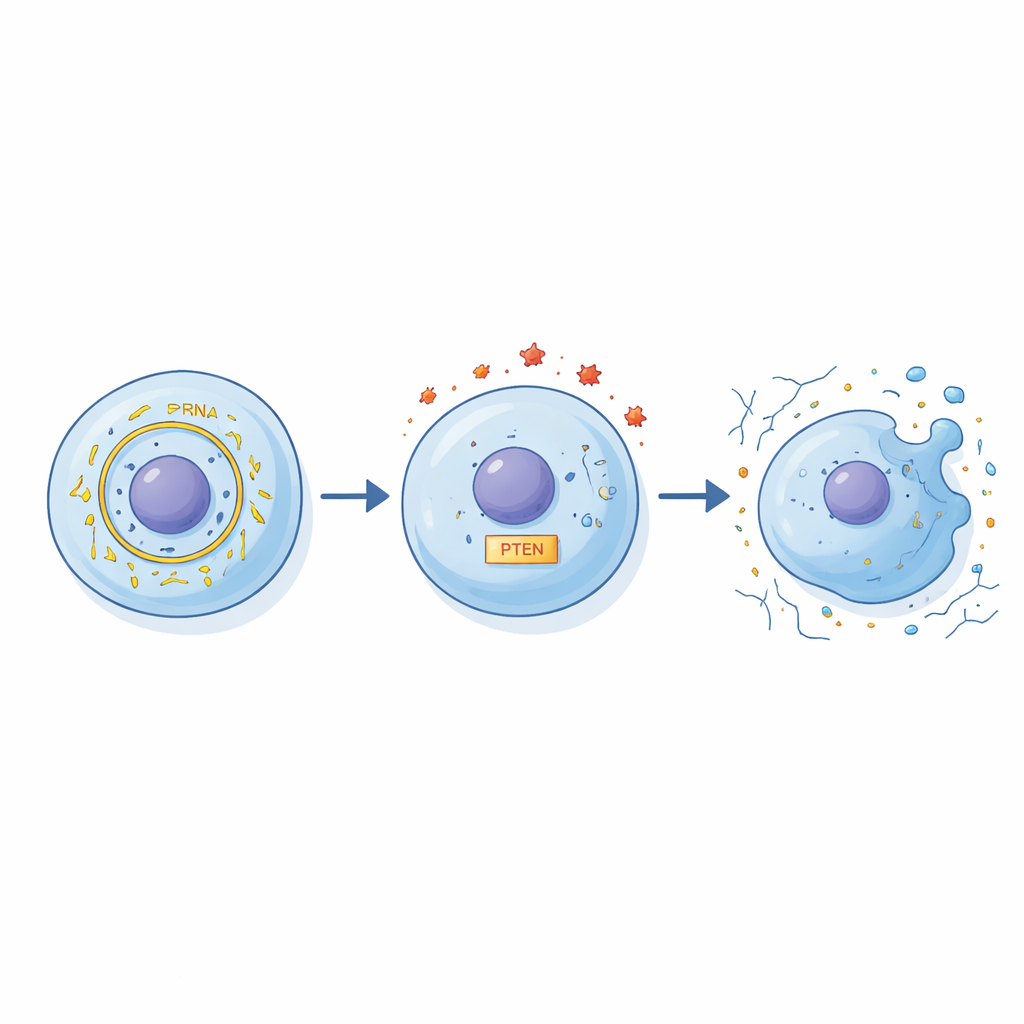
Los investigadores desentrañaron una cadena de interacciones que conecta circFN1 con el daño celular. Primero, demostraron que circFN1 puede actuar como una esponja para un pequeño ARN regulador llamado miR‑19b‑3p, uniéndose a él y secuestrándolo. Normalmente, miR‑19b‑3p ayuda a controlar los niveles de PTEN, una proteína que influye en la supervivencia celular, la inflamación y el mantenimiento de la matriz. Cuando aumentan los niveles de circFN1, se absorbe más miR‑19b‑3p, lo que a su vez altera la actividad de PTEN y desequilibra las señales protectoras y dañinas en la célula. A través de una serie de experimentos genéticos de “subir y bajar” la expresión, los autores demostraron que esta cadena circFN1–miR‑19b‑3p–PTEN condiciona fuertemente la respuesta de los condrocitos al estrés inflamatorio.
Qué ocurre cuando se cambian los interruptores
Para probar el impacto funcional de esta vía, el equipo redujo deliberadamente circFN1 en condrocitos tratados con IL‑1β. Cuando circFN1 se disminuyó, más células sobrevivieron, menos sufrieron muerte programada, y bloques constructivos clave del cartílago, como la proteína de la matriz agrecano, se conservaron mejor. Al mismo tiempo, las moléculas que degradan el cartílago, como MMP‑13, se redujeron, y la “sopa” circundante de sustancias inflamatorias como TNF‑α e IL‑6 se atenuó. Cuando los investigadores también modificaron miR‑19b‑3p y PTEN, estos cambios protectores se reforzaron o debilitaron de maneras predecibles, lo que respalda la idea de que los tres actores forman un circuito regulador conectado en lugar de actuar aisladamente.
De las placas de cultivo a futuras terapias
Aunque estos experimentos se realizaron en condrocitos humanos en cultivo y no en articulaciones vivas, los hallazgos apuntan a una nueva palanca conceptual para el tratamiento de la osteoartritis. El estudio sugiere que el aumento de circFN1 amplifica el daño al cartílago impulsado por la inflamación al reorganizar el equilibrio entre miR‑19b‑3p y PTEN. En términos sencillos, un exceso de este ARN circular hace que los condrocitos sean más vulnerables a los insultos inflamatorios y más propensos a morir y perder su matriz de soporte. Si trabajos futuros en animales y pacientes confirman estos resultados, medir circFN1 podría ayudar a detectar el daño articular temprano, y terapias diseñadas para bloquear circFN1 o aumentar miR‑19b‑3p podrían algún día ralentizar el avance de la rigidez ocasional hacia una osteoartritis crónica y discapacitante.
Cita: Jiang, Y., Wang, Q., Yang, X. et al. CircFN1 modulates IL-1β-induced osteoarthritis through the miR-19b-3p/PTEN signaling axis. Sci Rep 16, 10710 (2026). https://doi.org/10.1038/s41598-026-45897-0
Palabras clave: osteoartritis, cartílago, ARN no codificante, inflamación, degeneración articular