Clear Sky Science · de
CircFN1 moduliert IL-1β-induzierte Arthrose über die miR-19b-3p/PTEN-Signalkaskade
Warum schmerzende Gelenke wichtig sind
Arthrose wird oft als „Verschleiß“ abgetan, aber für Millionen von Menschen bedeutet sie tägliche Schmerzen, Steifheit und den Verlust von Selbstständigkeit. Diese Studie schaut unter die Haube schmerzender Gelenke und stellt eine aktuelle Frage: Warum verschlechtern sich manche Knie und Hüften so stark, und könnten wir diesen Prozess verlangsamen, indem wir das Verhalten bestimmter kleiner RNA-Moleküle in Knorpelzellen verändern?
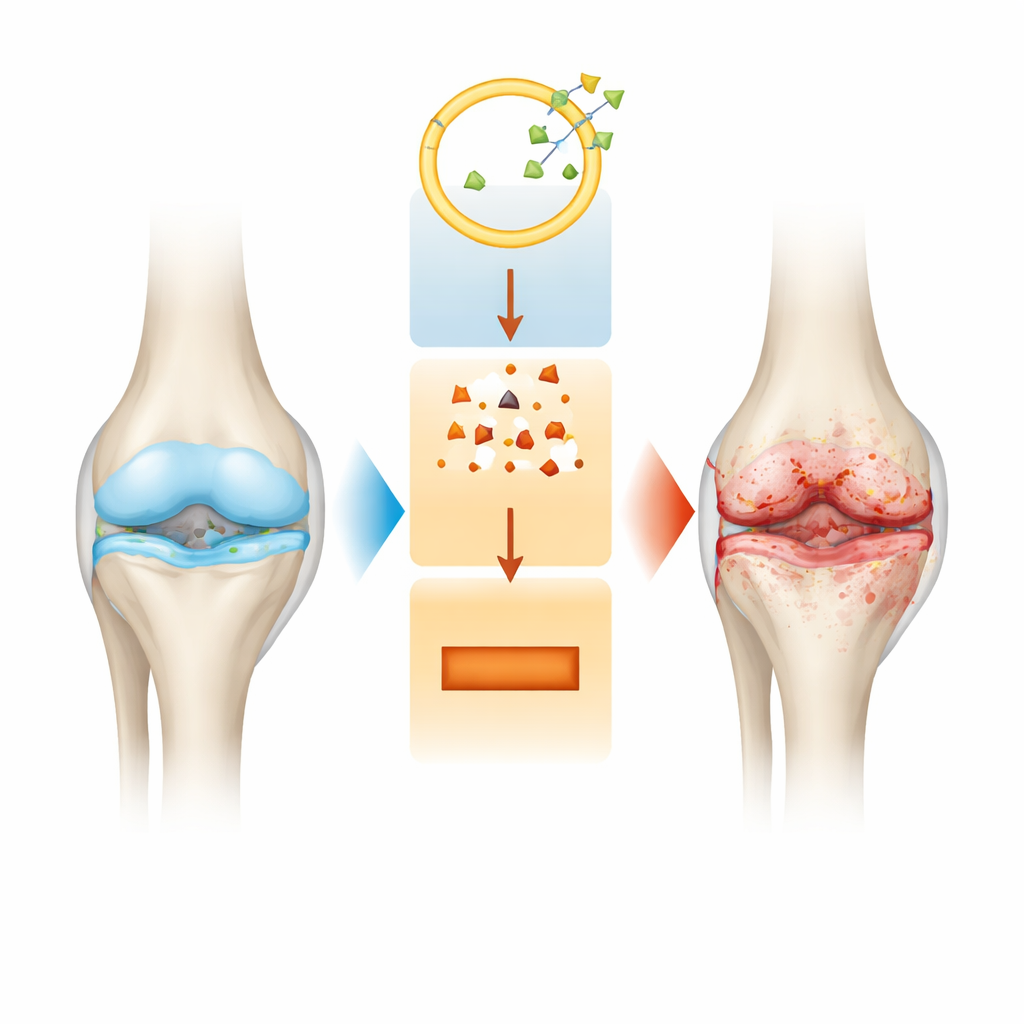
Ein genauerer Blick auf den Gelenkabbau
Arthrose ist mehr als nur dünner werdender Knorpel. Mit Fortschreiten der Erkrankung verändert sich das ganze Gelenk: Das glatte Polster an den Knochenenden erodiert, die Gelenkschleimhaut entzündet sich und der darunterliegende Knochen wird so umgebaut, dass dies Schmerzen verschlimmern kann. Die verfügbaren Behandlungen lindern meist nur die Symptome, stoppen aber nicht den langsamen strukturellen Verfall. Forschende suchen daher nach molekularen Schaltern in Knorpelzellen, den Chondrozyten, die erklären könnten, warum diese Zellen zu sterben beginnen und warum die sie umgebende Matrix zerfällt.
Die verborgene Welt der zirkulären RNA
In jüngerer Zeit haben Wissenschaftler entdeckt, dass viele Abschnitte unseres Erbmaterials nicht zu Proteinen werden, aber dennoch starke regulatorische Rollen übernehmen. Dazu gehören zirkuläre RNAs – geschlossene Moleküle, die ungewöhnlich stabil sind und oft in bestimmten Geweben reichlich vorkommen. Das Team hinter dieser Arbeit konzentrierte sich auf ein solches Molekül, circFN1, das in menschlichen Knorpelzellen nach Exposition gegenüber dem entzündlichen Signal IL‑1β erhöht vorkommt, einem Stoff, der im Labor häufig zur Simulation von Arthrose verwendet wird. Sequenzierungsversuche, die normale und mit IL‑1β behandelte Chondrozyten verglichen, zeigten, dass circFN1 zu den am stärksten erhöhten zirkulären RNAs gehörte und somit ein Hauptverdächtiger für die Verstärkung von Gelenkschäden ist.
Ein dreistufiges molekulares Tauziehen
Die Forschenden legten eine Interaktionskette offen, die circFN1 mit Zellschäden verbindet. Zunächst zeigten sie, dass circFN1 wie ein Schwamm für eine kleine regulatorische RNA namens miR‑19b‑3p wirken kann, indem es sie bindet und sequestriert. Normalerweise reguliert miR‑19b‑3p die Menge von PTEN, einem Protein, das Zellüberleben, Entzündung und Matrixerhalt beeinflusst. Wenn die circFN1-Spiegel steigen, wird mehr miR‑19b‑3p gebunden, was wiederum die PTEN-Aktivität verändert und das Gleichgewicht zwischen schützenden und schädlichen Signalen in der Zelle stört. Durch eine Reihe von genetischen "Aufdreh‑" und "Abdreh‑"Experimenten zeigten die Autorinnen und Autoren, dass diese circFN1–miR‑19b‑3p–PTEN‑Kette stark beeinflusst, wie Chondrozyten auf entzündlichen Stress reagieren.
Was passiert, wenn die Schalter umgelegt werden
Um die funktionellen Folgen dieses Pfads zu testen, reduzierten die Forschenden gezielt circFN1 in IL‑1β‑behandelten Chondrozyten. Bei abgesenktem circFN1 überlebten mehr Zellen, es kam zu weniger programmiertem Zelltod, und zentrale Bausteine des Knorpels wie das Matrixprotein Aggrecan blieben besser erhalten. Gleichzeitig sanken Moleküle, die Knorpel abbauen, wie MMP‑13, und die Konzentration entzündlicher Substanzen wie TNF‑α und IL‑6 nahm ab. Als die Forschenden zudem miR‑19b‑3p und PTEN veränderten, verstärkten oder schwächten sich diese schützenden Effekte in vorhersehbarer Weise ab, was die Vorstellung stützte, dass alle drei Partner einen vernetzten Regulationskreis bilden und nicht isoliert wirken.
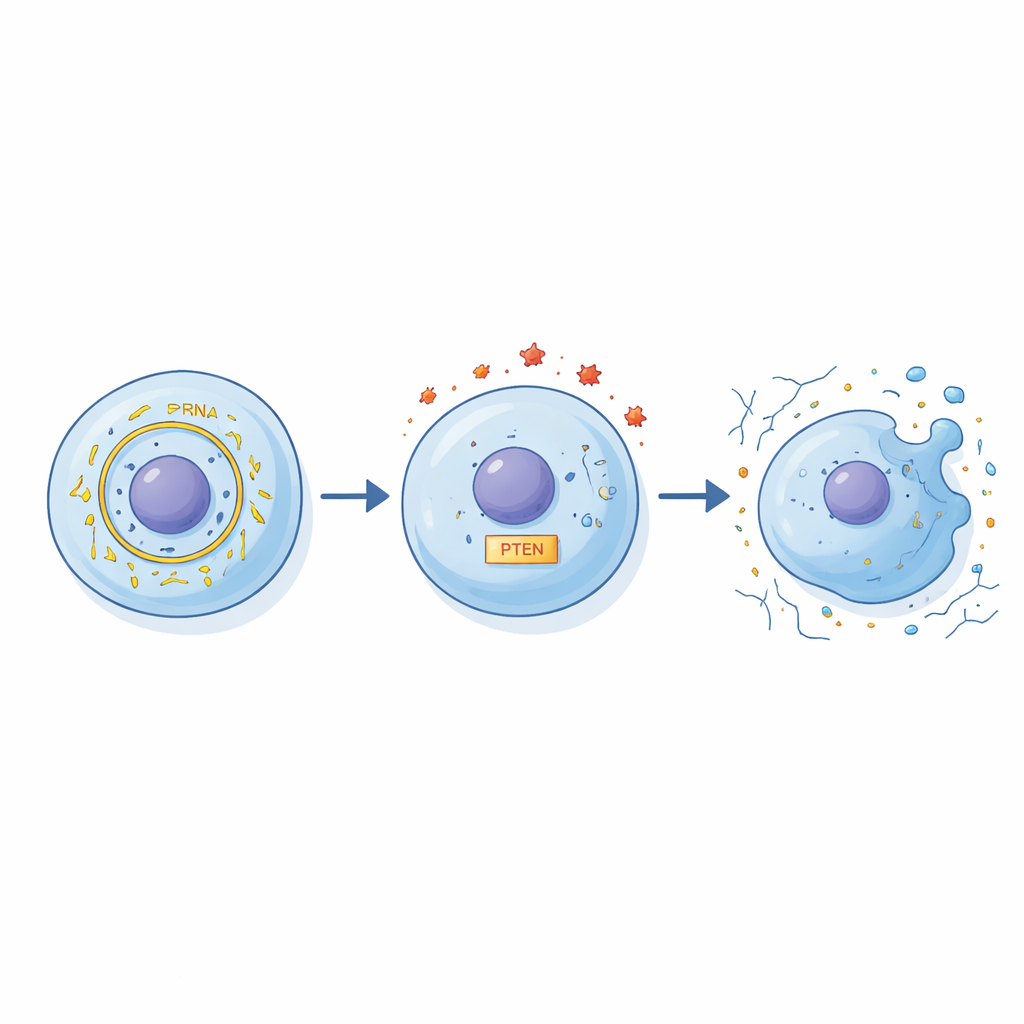
Von Zellkulturen zu künftigen Therapien
Obwohl diese Experimente an kultivierten menschlichen Knorpelzellen und nicht in lebenden Gelenken durchgeführt wurden, weisen die Ergebnisse auf einen neuen Konzepthebel für die Arthrosebehandlung hin. Die Studie legt nahe, dass erhöhtes circFN1 entzündungsgetriebene Knorpelschäden verstärkt, indem es das Gleichgewicht zwischen miR‑19b‑3p und PTEN verschiebt. Einfach gesagt macht ein Überschuss dieser zirkulären RNA Knorpelzellen anfälliger für entzündliche Angriffe und führt dazu, dass sie eher absterben und ihre stützende Matrix verlieren. Wenn zukünftige Arbeiten an Tieren und Menschen diese Befunde bestätigen, könnte die Messung von circFN1 helfen, frühe Gelenkschäden zu erkennen, und Therapien, die circFN1 blockieren oder miR‑19b‑3p steigern, könnten eines Tages das Fortschreiten von gelegentlicher Steifheit zu chronischer, behindernder Arthrose verlangsamen.
Zitation: Jiang, Y., Wang, Q., Yang, X. et al. CircFN1 modulates IL-1β-induced osteoarthritis through the miR-19b-3p/PTEN signaling axis. Sci Rep 16, 10710 (2026). https://doi.org/10.1038/s41598-026-45897-0
Schlüsselwörter: Arthrose, Knorpel, nichtkodierende RNA, Entzündung, Gelenkdegeneration