Clear Sky Science · pl
CircFN1 moduluje osteoartrozę wywołaną przez IL-1β za pośrednictwem osi sygnalizacyjnej miR-19b-3p/PTEN
Dlaczego bolące stawy mają znaczenie
Osteoartroza bywa bagatelizowana jako „zużycie”, ale dla milionów osób oznacza codzienny ból, sztywność i utratę samodzielności. W tym badaniu przyjrzano się mechanizmom bolących stawów i postawiono aktualne pytanie: dlaczego niektóre kolana i biodra tak bardzo się pogarszają i czy możemy spowolnić ten proces przez zmianę działania pewnych drobnych cząsteczek RNA w komórkach chrząstki?
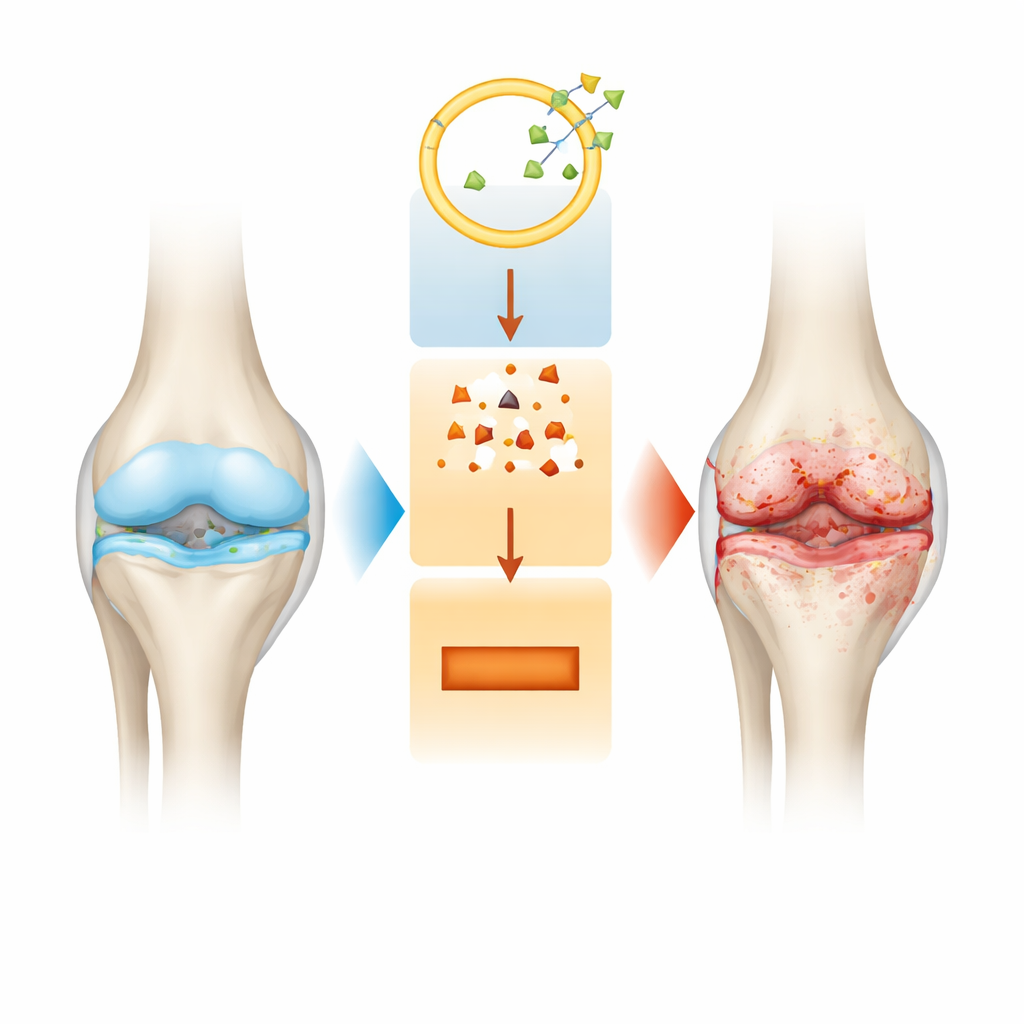
Bliższe spojrzenie na rozpad stawu
Osteoartroza to coś więcej niż przerzedzenie chrząstki. W miarę postępu choroby cały staw się zmienia: gładka warstwa na końcach kości się eroduje, wyściółka stawu ulega zapaleniu, a leżąca pod nią kość przebudowuje się w sposób, który może nasilać ból. Obecne leczenie głównie łagodzi objawy, ale nie zatrzymuje powolnych zmian strukturalnych. Naukowcy zatem poszukują molekularnych przełączników w komórkach chrząstki, zwanych chondrocytami, które mogłyby wyjaśnić, dlaczego te komórki zaczynają umierać i dlaczego otaczająca je macierz ulega degradacji.
Ukryty świat RNA cyrkularnego
W ostatnich latach odkryto, że wiele fragmentów naszego materiału genetycznego nigdy nie przekształca się w białka, a mimo to pełni silne funkcje regulacyjne. Wśród nich znajdują się RNA cyrkularne — zamknięte cząsteczki, które są wyjątkowo trwałe i często obficie występują w określonych tkankach. Zespół autorów skupił się na jednej z takich cząsteczek, circFN1, wykrytej w wyższych stężeniach w ludzkich komórkach chrząstki po ekspozycji na sygnał zapalny IL‑1β, chemiczny czynnik powszechnie używany w modelach osteoartrozy in vitro. Eksperymenty sekwencjonowania porównujące chondrocyty kontrolne i traktowane IL‑1β wykazały, że circFN1 był jednym z najsilniej podwyższonych RNA cyrkularnych, co czyni go głównym podejrzanym o napędzanie uszkodzeń stawu.
Trzystopniowa molekularna gra przeciągania
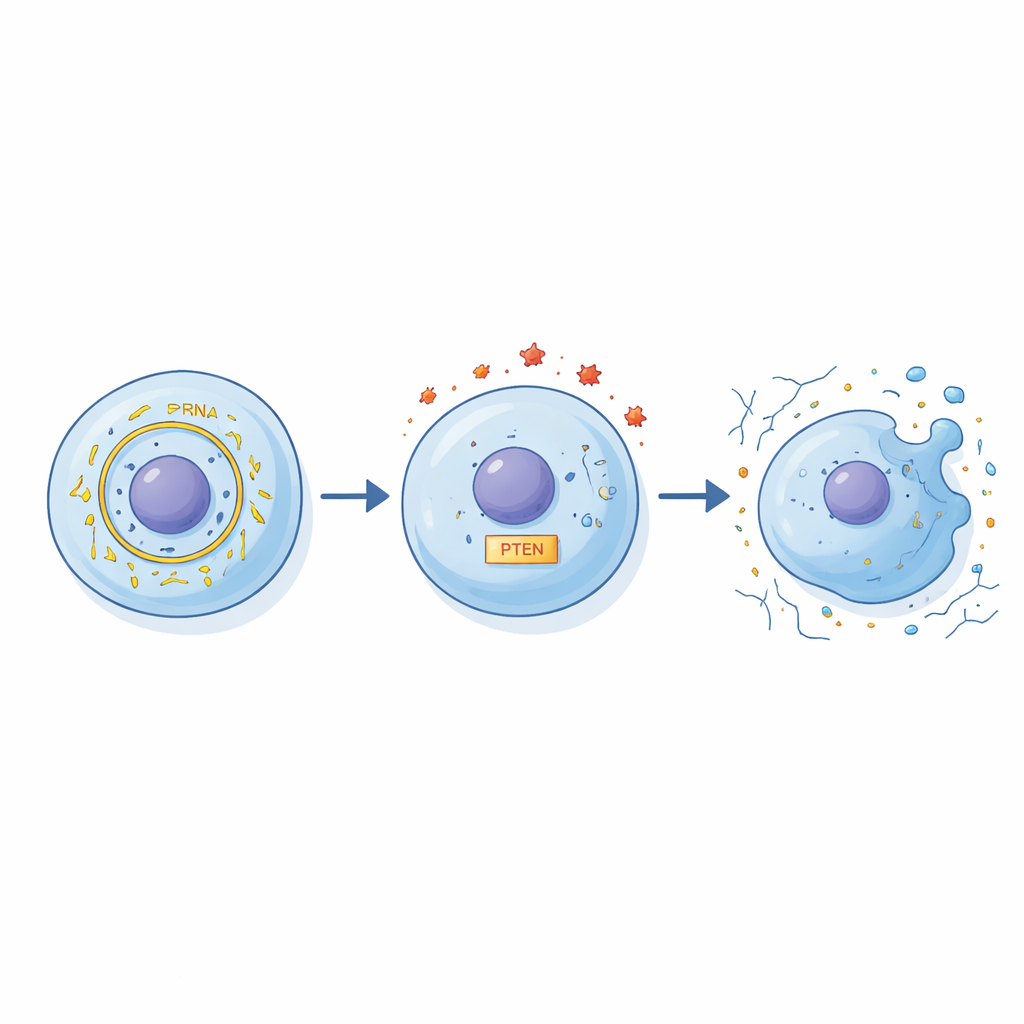
Naukowcy odkryli łańcuch interakcji łączący circFN1 z uszkodzeniem komórek. Najpierw pokazali, że circFN1 może działać jak gąbka dla małej regulacyjnej cząsteczki RNA o nazwie miR‑19b‑3p, wiążąc ją i sekwestrując. Normalnie miR‑19b‑3p pomaga kontrolować poziomy PTEN, białka wpływającego na przeżycie komórek, zapalenie i utrzymanie macierzy. Gdy poziom circFN1 rośnie, więcej miR‑19b‑3p zostaje „wchłonięte”, co z kolei zmienia aktywność PTEN i zaburza równowagę między sygnałami ochronnymi a szkodliwymi w komórce. Poprzez serię eksperymentów genetycznego „podkręcania i przyciszania” autorzy wykazali, że łańcuch circFN1–miR‑19b‑3p–PTEN silnie kształtuje reakcję chondrocytów na stres zapalny.
Co się dzieje, gdy przełączniki zostaną przestawione
Aby sprawdzić funkcjonalny wpływ tej ścieżki, zespół celowo obniżył poziom circFN1 w chondrocytach traktowanych IL‑1β. Gdy circFN1 został zmniejszony, więcej komórek przeżyło, mniej uległo programowanej śmierci, a kluczowe składniki budulcowe chrząstki, takie jak białko macierzy agrekan, były lepiej zachowane. Jednocześnie spadły poziomy enzymów niszczących chrząstkę, takich jak MMP‑13, a otaczające „soup” substancji zapalnych, takich jak TNF‑α i IL‑6, było mniej nasilone. Gdy badacze także modyfikowali miR‑19b‑3p i PTEN, obserwowane zmiany ochronne wzmacniały się lub osłabiały w przewidywalny sposób, co wzmacniało przekonanie, że wszystkie trzy elementy tworzą połączony obwód regulacyjny, a nie działają w izolacji.
Od hodowli komórek do przyszłych terapii
Chociaż eksperymenty przeprowadzono w hodowanych ludzkich komórkach chrząstki, a nie w żywych stawach, wyniki wskazują na nowy koncepcyjny dźwignię w leczeniu osteoartrozy. Badanie sugeruje, że podwyższone poziomy circFN1 wzmacniają zapalnie napędzane uszkodzenie chrząstki przez przestawienie równowagi między miR‑19b‑3p a PTEN. Mówiąc prościej, nadmiar tego RNA cyrkularnego czyni komórki chrząstki bardziej podatnymi na urazy zapalne, bardziej skłonnymi do obumierania i do utraty macierzy podporowej. Jeśli przyszłe badania na zwierzętach i u pacjentów potwierdzą te wyniki, pomiar circFN1 mógłby pomóc wykryć wczesne uszkodzenia stawu, a terapie mające na celu zablokowanie circFN1 lub zwiększenie miR‑19b‑3p mogłyby pewnego dnia spowolnić przejście od sporadycznej sztywności do przewlekłej, wyniszczającej osteoartrozy.
Cytowanie: Jiang, Y., Wang, Q., Yang, X. et al. CircFN1 modulates IL-1β-induced osteoarthritis through the miR-19b-3p/PTEN signaling axis. Sci Rep 16, 10710 (2026). https://doi.org/10.1038/s41598-026-45897-0
Słowa kluczowe: choroba zwyrodnieniowa stawów, chrząstka, RNA niekodujące, zapalanie, degradacja stawu