Clear Sky Science · zh
Limosilactobacillus reuteri 代谢产物在 5‑氟尿嘧啶暴露后调节免疫通路并促进肠道屏障修复
为何在癌症治疗期间保护肠道至关重要
化疗能挽救生命,但常常损伤口腔和肠道黏膜,导致疼痛、腹泻和感染,进而可能中断或削弱治疗。这项研究探讨了无害细菌,或更确切地说它们释放的分子,是否能在常用抗癌药物损伤后帮助肠壁自我修复。研究聚焦于一种知名益生菌菌株 Limosilactobacillus reuteri DSM 17938,问题是:其分泌的糖类和微小颗粒能否在不向脆弱患者给予活菌的情况下,支持愈合?
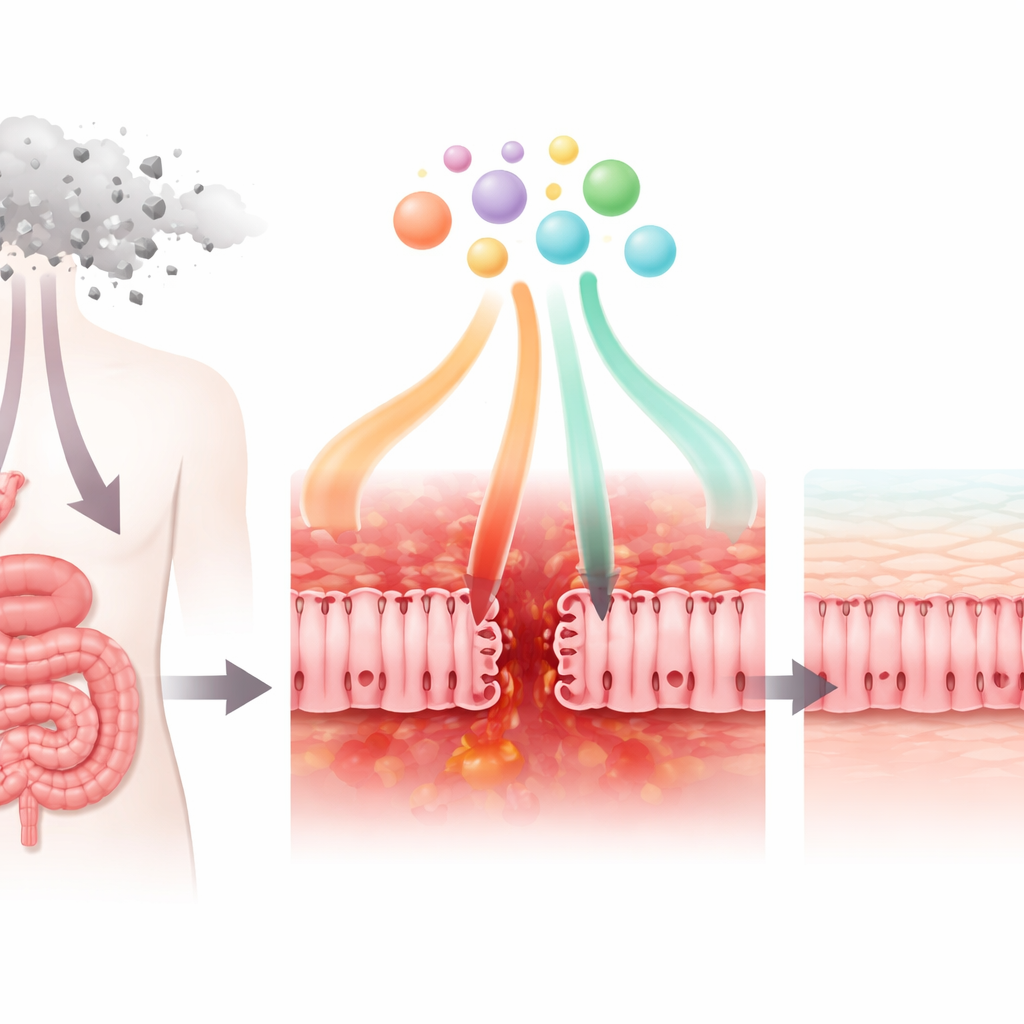
一种常用抗癌药如何损害肠壁
研究者首先检查了广泛用于乳腺癌、胃癌和结直肠癌的化疗药物 5‑氟尿嘧啶(5‑FU)对类小肠上皮细胞的影响。在培养皿中,5‑FU 降低了这些细胞的存活率和正常代谢功能。它还削弱了将相邻细胞紧密连接在一起的“紧密连接”,使细胞层更易渗漏。显微镜下可见关键的连接蛋白失去了原有整齐的网状排列并变得紊乱。与此同时,细胞开始分泌更多的炎性信号,如趋化因子 CXCL8,而调节因子 TGF‑β1 的产生减少。这些变化总体上与患者肠道屏障受损、炎症和对微生物屏蔽能力下降时的情况相吻合。
来自益生菌的有益糖类
研究团队随后转向 L. reuteri DSM 17938 产生的产物:不含细胞的上清液(含多种分泌分子)、纯化的胞外多糖(EPS,长链糖)和微小膜囊泡。这些产物在化疗药物洗去后才加入,模拟的是一种支持性治疗而非事先保护。在类肠上皮细胞系和来自供体的人来源小肠原代细胞中,EPS 明显改善了屏障功能。细胞层的电阻上升,荧光示踪物穿透减少,表明封闭性增强。有趣的是,EPS 和其他细菌产物还在肠腔侧促使 CXCL8 和另一个趋化因子 CCL20 的释放增加。因此,同样的处理既增强了屏障,又激发了通常与炎症相关的信号。
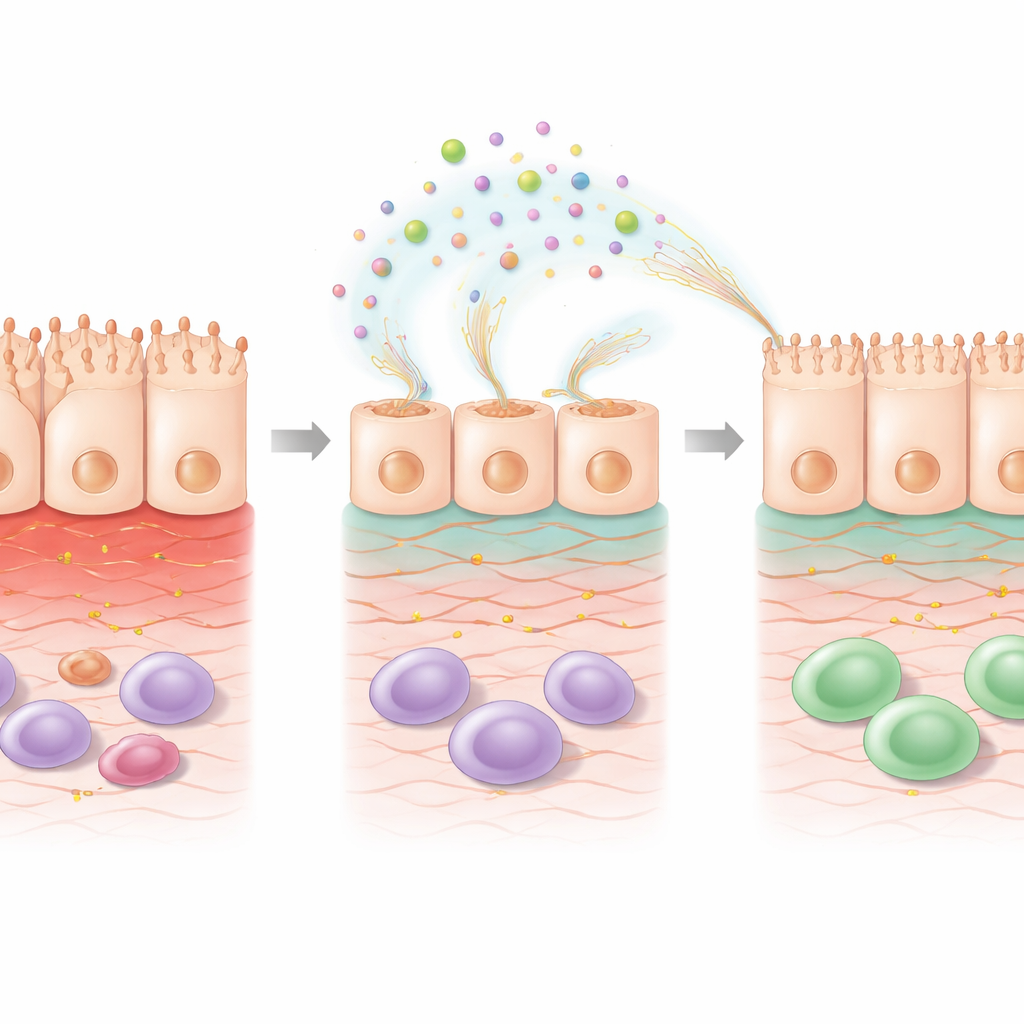
细胞内部:修复程序被激活
为了弄清细胞内部发生了什么变化,科学家们分析了在有无 EPS 条件下 5‑FU 处理后的全基因表达。单独的化疗改变了许多与细胞存活、应激处理和免疫信号相关的基因。将 EPS 加到 5‑FU 之上进一步改变了基因模式,指向修复方向。与组织外基质(支持细胞的支架)重塑相关的基因以及与视黄酸(维生素 A 衍生分子,已知有利于肠道屏障健康)相关的通路被上调。帮助解毒氧化应激有害副产物的基因被激活,而一些与应激诱导损伤相关的基因被下调。这些变化表明 EPS 不仅仅是覆盖在表面;它们主动重新编程受损细胞,使其重建结构并恢复功能。
愈合过程中的免疫细胞对话
因为肠道屏障并非孤立愈合,团队进一步探讨这些上皮变化如何影响免疫细胞。他们将来自 5‑FU 损伤并经细菌产物刺激的上皮培养物的培养液用于将人单核细胞分化为巨噬细胞。来自 EPS 处理细胞的条件培养基促使巨噬细胞趋向 M1‑样表型,这通常与早期炎性反应和组织清理相关。相比之下,来自不含细胞的上清液处理的培养基更倾向于促成 M2‑样表型,通常与抑制炎症和组织重塑相关,而膜囊泡则产生混合模式。值得注意的是,即便表面标志显示 M1‑样倾向,典型的强烈炎性细胞因子如 IL‑1β 和 TNF‑α 并未增加,暗示这是一种更为平衡、以修复为中心的激活而非失控的炎症反应。
这对未来癌症护理可能意味着什么
这项工作表明,一种益生菌所释放的特定分子——尤其是其胞外多糖——能够在体外帮助肠细胞从化疗引起的损伤中恢复。EPS 强化了屏障、启动了内部修复程序,并以与有序组织愈合一致的方式影响免疫细胞行为。尽管该研究在细胞培养体系中完成,需要在动物和患者中进一步验证,但它指向了一个可能的未来:通过使用明确定义的细菌产物而不是活微生物,作为化疗的辅助以减少痛苦的肠道副作用,帮助患者维持救命治疗。
引用: Lasaviciute, G., López Plana, M., Sundberg Örtegren, S. et al. Limosilactobacillus reuteri metabolites modulate immune pathways and intestinal barrier repair after 5 fluorouracil exposure. Sci Rep 16, 11376 (2026). https://doi.org/10.1038/s41598-026-45524-y
关键词: 化疗黏膜炎, 肠道屏障修复, 益生菌代谢产物, Limosilactobacillus reuteri, 胞外多糖