Clear Sky Science · ar
مستقلبات Limosilactobacillus reuteri تعدّل مسارات المناعة وإصلاح حاجز الأمعاء بعد التعرض للفلوئورويوراسيل 5
لماذا حماية الأمعاء أثناء علاج السرطان مهمة
العلاج الكيميائي ينقذ الأرواح، لكنه كثيرًا ما يؤذي بطانة الفم والأمعاء، مسببًا ألمًا وإسهالًا وعدوى قد تقطع أو تضعف العلاج. تستقصي هذه الدراسة ما إذا كانت البكتيريا غير الضارة، أو بدقة أكبر الجزيئات التي تفرزها، قادرة على مساعدة جدار الأمعاء على الإصلاح بعد أن يتعرض لإصابة بواسطة دواء شائع للسرطان. يركز العمل على سلالة بروبيوتيك معروفة، Limosilactobacillus reuteri DSM 17938، ويتساءل: هل يمكن للسكريات والبِقع الصغيرة التي تفرزها أن تدعم الشفاء دون الحاجة إلى إعطاء بكتيريا حية للمرضى الضعفاء؟
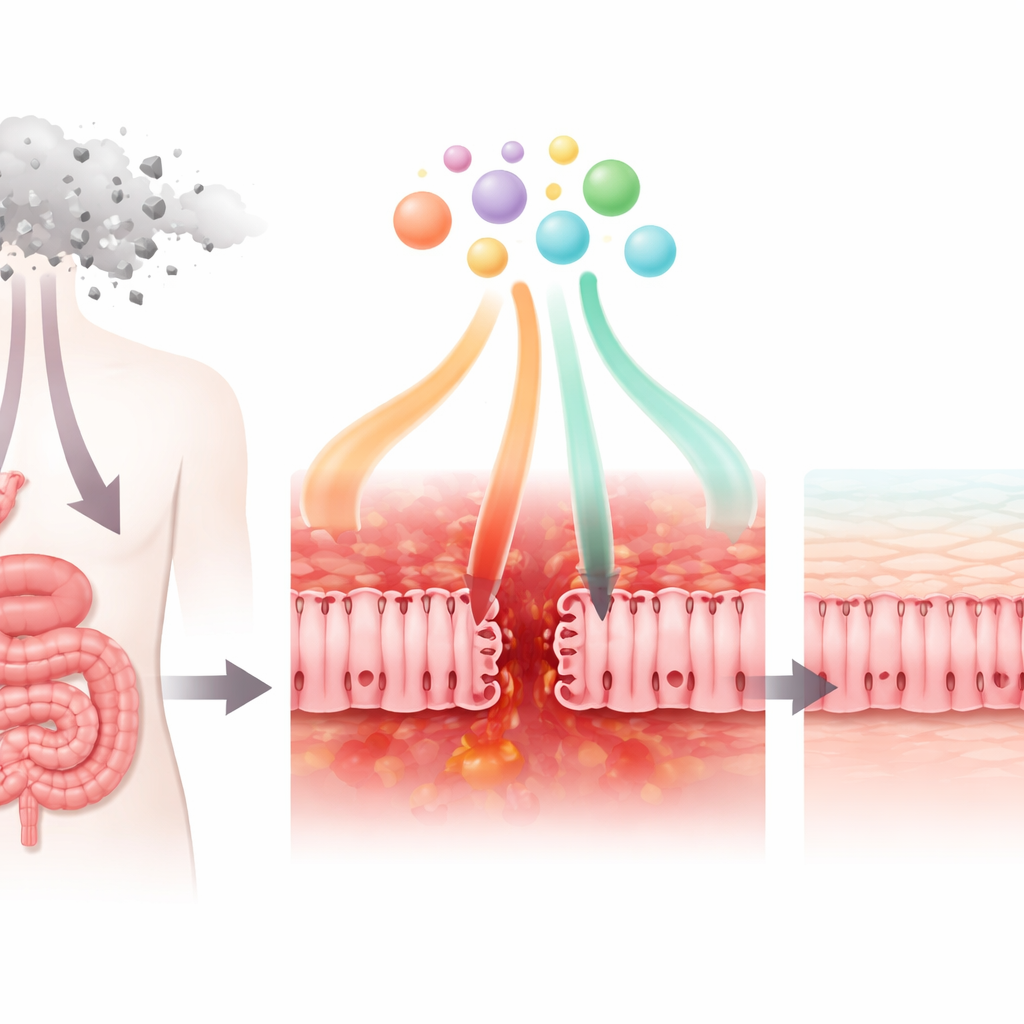
كيف يضر دواء السرطان الشائع بجدار الأمعاء
بدأ الباحثون بفحص كيفية تأثير دواء العلاج الكيميائي 5‑فلورويوراسيل (5‑FU)، المستخدم على نطاق واسع ضد سرطانات الثدي والمعدة والقولون، على خلايا تشبه خلايا بطانة الأمعاء الدقيقة. في أطباق المختبر، خفّض 5‑FU بقاء هذه الخلايا وكفاءتها الأيضية الطبيعية. كما أضعف "الالتصاقات المحكمة" التي تربط الخلايا المجاورة ببعضها، مما جعل طبقة الخلايا أكثر تسربًا. أظهرت الميكروسكوبية أن بروتينات الوصل الرئيسية فقدت ترتيبها الشبكي المعتاد وأصبحت غير منظمة. في الوقت نفسه، بدأت الخلايا في إفراز مستويات أعلى من الإشارات الالتهابية، مثل الكيمياء الموجهة CXCL8، بينما أنتجت كميات أقل من العامل التنظيمي TGF‑β1. معًا تعكس هذه التغيرات ما يحدث لدى المرضى عندما يتضرر حاجز الأمعاء ويشتعل ويصبح أقل قدرة على صد الميكروبات.
السكريات المفيدة من بكتيريا صديقة
ثم اتجه الفريق إلى منتجات L. reuteri DSM 17938: مصل خالٍ من الخلايا يحتوي على العديد من الجزيئات المفرزة، وبوليسكاريدات خارِجية (EPS، سلاسل سكرية طويلة) منقاة، وحويصلات غشائية دقيقة. أضيفت هذه فقط بعد غسل دواء العلاج الكيميائي بعيدًا، محاكاةً لعلاج داعم بدلاً من درع وقائي يُعطى مسبقًا. في كلٍ من سطر الخلايا الشبيه بالأمعاء والخلايا الأولية لبطانة الأمعاء الدقيقة البشرية من متبرع، حسّنت EPS بوضوح وظيفة الحاجز. ارتفعت المقاومة الكهربائية عبر طبقة الخلايا، وانخفض مرور متتبع فلوري عبر الحاجز، ما يشير إلى إغلاق أقوى. ومن المثير للاهتمام أن EPS والمنتجات البكتيرية الأخرى عززت أيضًا إطلاق CXCL8 وكيميوكين آخر، CCL20، خاصةً على الجانب المواجه لمجرى الأمعاء. بذلك، نفس المعالجة التي قَوت الحاجز أثارت أيضًا إشارات مرتبطة عادةً بالالتهاب.
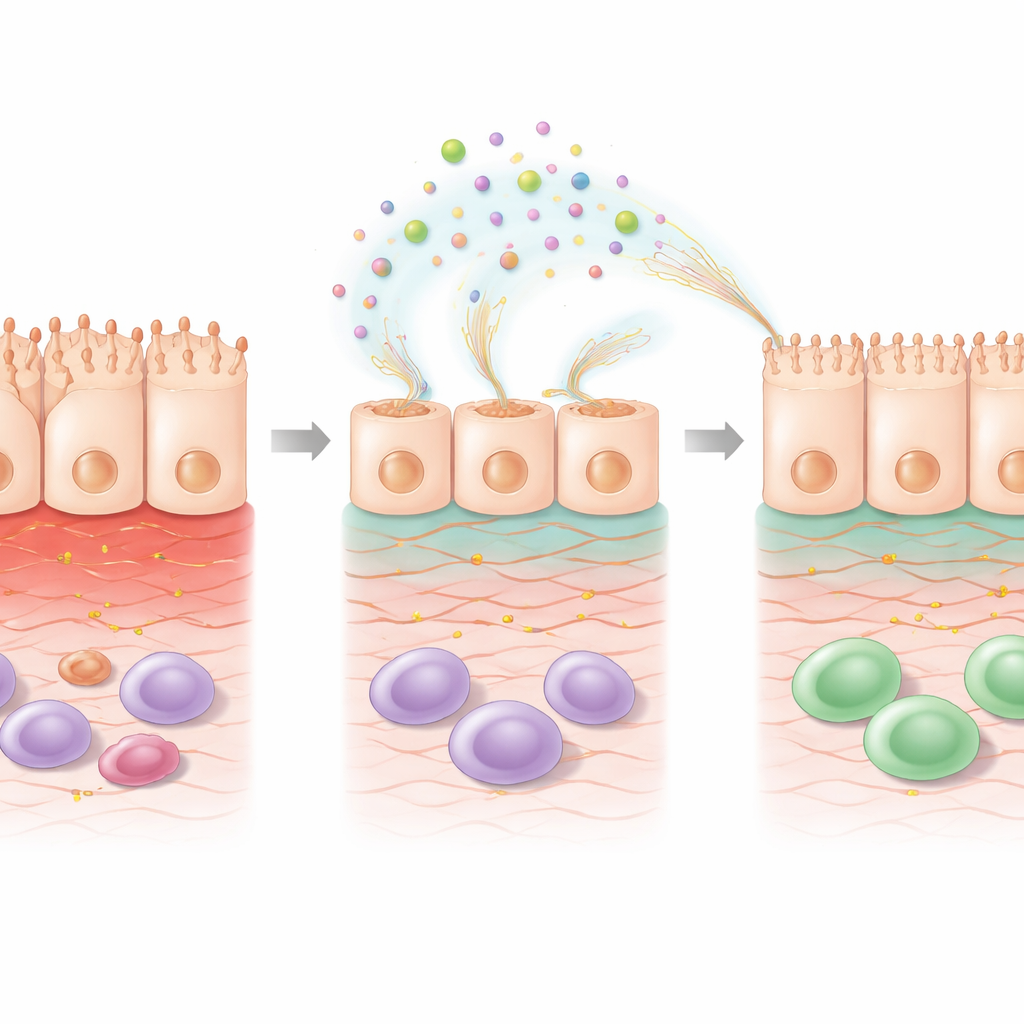
داخل الخلية: برامج الإصلاح تنطلق
لفهم ما الذي تغير داخل الخلايا، حلّل العلماء نشاط الجينات العام بعد علاج 5‑FU مع أو بدون EPS. غير العلاج الكيميائي وحده العديد من الجينات المتعلقة ببقاء الخلايا، والتعامل مع الإجهاد، وإشارات المناعة. إضافة EPS فوق 5‑FU بدّلت النمط أكثر، بطريقة أظهرت ميلًا نحو الإصلاح. ارتفعت مستويات جينات تشارك في تنظيم المصفوفة خارج الخلوية—الهيكل الداعم للخلايا—وفي مسارات مرتبطة بحمض الريتينويك، الجزيء المشتق من فيتامين A المعروف بتعزيز صحة حاجز الأمعاء. كما أُشغلت جينات أخرى تساعد على إزالة السموم الناتجة عن الإجهاد التأكسدي، بينما خُفّضت بعض الجينات المرتبطة بالضرر الناتج عن الإجهاد. تشير هذه التغيرات إلى أن EPS لا تكتفي بتغليف السطح؛ بل تعيد برمجة الخلايا المصابة بنشاط لإعادة بناء بنيتها واستعادة وظائفها.
تواصل مع خلايا المناعة أثناء الشفاء
لأن حاجز الأمعاء لا يلتئم بمعزل عن المحيط، سأل الفريق كيف يمكن أن تؤثر هذه التغيرات الظاهرية على خلايا المناعة. أخذوا السائل من مزاريب ظهارية تضررت بـ5‑FU وتم تحفيزها بمنتجات بكتيرية واستخدموه لتنمية الخلايا الوحيدة البشرية إلى البلاعم. دفعت الوسائط المخصصة من الخلايا المعالجة بـEPS البلاعم نحو نمط شبيه بـM1، وهي حالة عادةً ما ترتبط بالاستجابات الالتهابية المبكرة وتنظيف الأنسجة. في المقابل، ميّزت الوسائط من المزاريب المعالجة بالمصل الخالي من الخلايا الميل نحو نمط شبيه بـM2، المرتبط عادةً بتهدئة الالتهاب وإعادة تشكيل الأنسجة، بينما أنتجت الحويصلات الغشائية نمطًا مختلطًا. ومن الجدير بالذكر أنه حتى عندما اقترحت علامات سطحية انحرافًا شبيهًا بـM1، لم تزدَّ السيتوكينات الالتهابية الكلاسيكية العدوانية مثل IL‑1β وTNF‑α، مما يلمّح إلى تفعيل أكثر توازنًا وموجهًا نحو الإصلاح بدلًا من التهاب جامح.
ما الذي قد يعنيه هذا لرعاية السرطان المستقبلية
تُظهر هذه الدراسة أن جزيئات محددة يُفرزها بكتيرٍيا بروبيوتيك—وخاصة البوليسكاريدات الخارِجية—يمكن أن تساعد خلايا الأمعاء على التعافي من إصابات ناتجة عن العلاج الكيميائي في المختبر. قوّت EPS الحاجز، وشغّلت برامج إصلاح داخلية، وشكّلت سلوك خلايا المناعة بطرق تتوافق مع شفاء منظم للأنسجة. وعلى الرغم من أن الدراسة أُجريت في مزاريب خلوية وتحتاج إلى تأكيد في حيوانات ومرضى، إلا أنها تشير إلى مستقبل قد تُستخدم فيه منتجات بكتيرية محددة بعناية، بدلًا من الكائنات الحية نفسها، جنبًا إلى جنب مع العلاج الكيميائي لتقليل آثار الأمعاء المؤلمة ومساعدة المرضى على الاستمرار في العلاجات المنقذة للحياة.
الاستشهاد: Lasaviciute, G., López Plana, M., Sundberg Örtegren, S. et al. Limosilactobacillus reuteri metabolites modulate immune pathways and intestinal barrier repair after 5 fluorouracil exposure. Sci Rep 16, 11376 (2026). https://doi.org/10.1038/s41598-026-45524-y
الكلمات المفتاحية: التهاب الغشاء المخاطي الناتج عن العلاج الكيميائي, إصلاح حاجز الأمعاء, مستقلبات البروبيوتيك, Limosilactobacillus reuteri, البوليسكاريدات الخارجية