Clear Sky Science · nl
Metabolieten van Limosilactobacillus reuteri moduleren immuunroutes en herstel van de darmbarrière na blootstelling aan 5-fluorouracil
Waarom het beschermen van de darm tijdens kankerbehandeling belangrijk is
Chemotherapie redt levens, maar beschadigt vaak het slijmvlies van mond en darm, wat pijn, diarree en infecties veroorzaakt en de behandeling kan onderbreken of verzwakken. Deze studie onderzoekt of onschadelijke bacteriën, of specifieker de door hen uitgescheiden moleculen, de darmwand kunnen helpen herstellen nadat deze beschadigd is door een veelgebruikt kankermedicijn. Het werk richt zich op een bekende probiotische stam, Limosilactobacillus reuteri DSM 17938, en stelt de vraag: kunnen de uitgescheiden suikers en kleine deeltjes het herstel ondersteunen zonder levende bacteriën aan kwetsbare patiënten te hoeven toedienen?
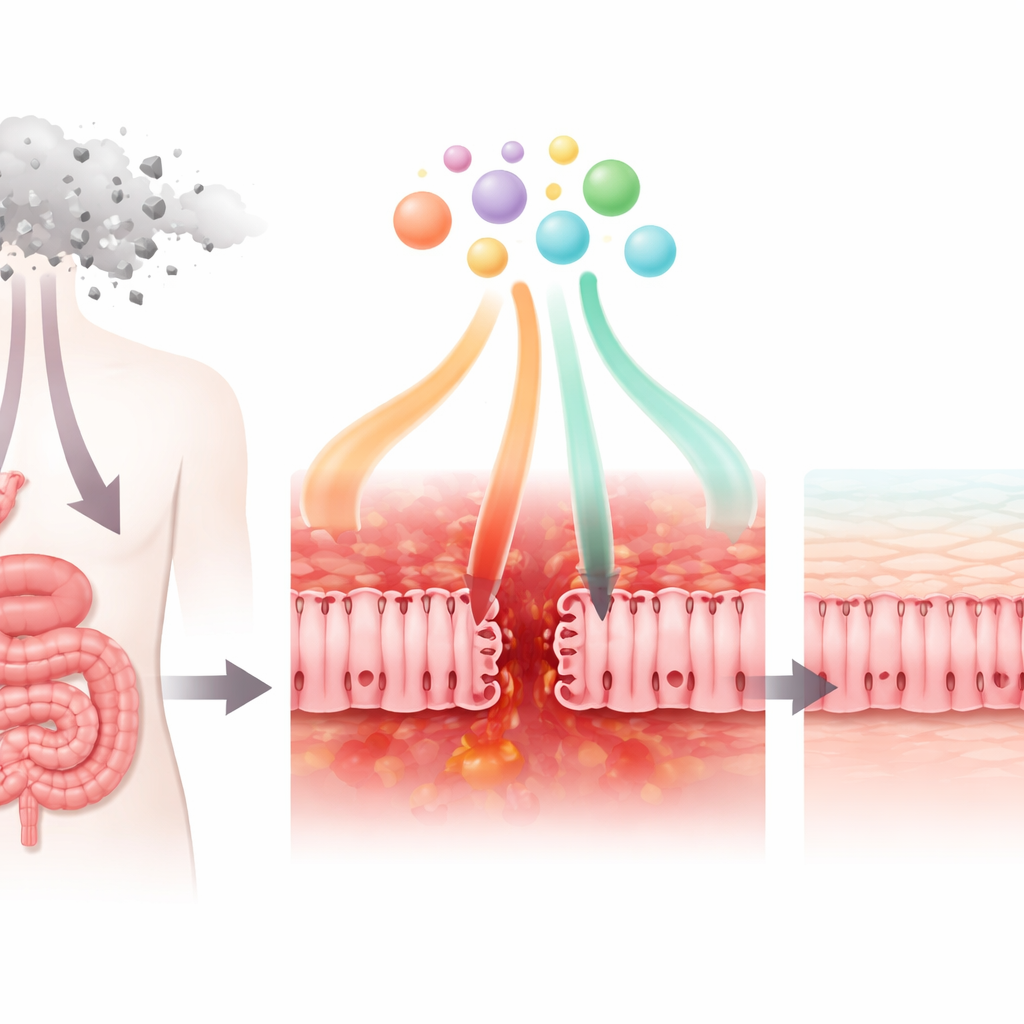
Hoe een veelgebruikt kankermedicijn de darmwand schaadt
De onderzoekers onderzochten eerst hoe het chemotherapiemedicijn 5-fluorouracil (5-FU), veel gebruikt tegen borst-, maag- en darmkanker, cellen beïnvloedt die lijken op de bekleding van de dunne darm. In laboratoriumschalen verminderde 5-FU het overleven en de normale stofwisseling van deze cellen. Het verzwakte ook de "tight junctions" die aangrenzende cellen bij elkaar houden, waardoor de cellaag lekker werd. Microscopen lieten zien dat sleutelproteïnen van de verbindingen hun gebruikelijke nette, webachtige rangschikking verloren en gedesorganiseerd raakten. Tegelijkertijd begonnen de cellen hogere niveaus van ontstekingssignalen af te geven, zoals de chemokine CXCL8, terwijl de productie van de regulatorische factor TGF-β1 afnam. Samen weerspiegelen deze veranderingen wat er gebeurt bij patiënten wanneer de darmbarrière beschadigd, ontstoken is en minder goed in staat is om microben buiten te houden.
Helende suikers van vriendelijke bacteriën
Het team wendde zich vervolgens tot producten gemaakt door L. reuteri DSM 17938: een cell-vrije supernatant met vele uitgescheiden moleculen, gezuiverde exopolysacchariden (EPS, lange suikerketens) en kleine membraanvasjes. Deze werden pas toegevoegd nadat het chemotherapiemedicijn was weggespoeld, wat een ondersteunende behandeling nabootst in plaats van een beschermende toediening vooraf. Zowel in de darmachtige kankercellijn als in primaire humane dunne darmcellen van een donor verbeterde EPS duidelijk de barrièrefunctie. De elektrische weerstand over de cellaag nam toe en de doorgang van een fluorescerende tracer door de barrière nam af, wat op betere afdichting wijst. Interessant was dat EPS en de andere bacteriële producten ook de afgifte van CXCL8 en een andere chemokine, CCL20, verhoogden, vooral aan de zijde gericht naar het darmlumen. Zo riep dezelfde behandeling die de barrière versterkte ook signalen op die typisch met ontsteking geassocieerd worden.
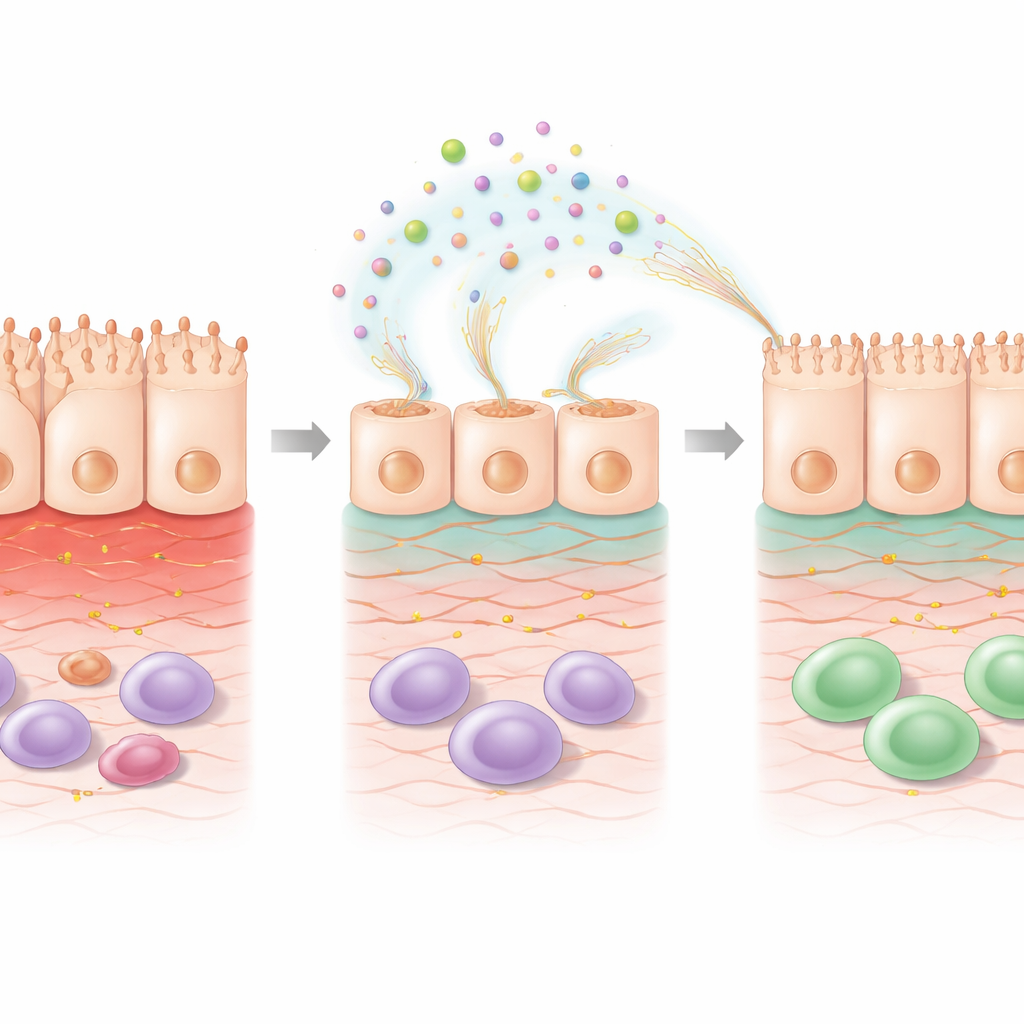
Binnenin de cel: herstelprogramma's schakelen in
Om te begrijpen wat er binnenin de cellen veranderde, analyseerden de wetenschappers de globale genactiviteit na behandeling met 5-FU met of zonder EPS. Chemotherapie alleen veranderde vele genen die verband houden met celoverleving, stressrespons en immuunsignalering. Het toevoegen van EPS bovenop 5-FU verschuifde het patroon verder in een richting die op herstel wijst. Genen die betrokken zijn bij de organisatie van de extracellulaire matrix — het geraamte dat cellen ondersteunt — en in routes gekoppeld aan retinoïnezuur, een uit vitamine A afgeleid molecuul dat de gezondheid van de darmbarrière bevordert, werden omhooggereguleerd. Andere genen die helpen bij het ontgiften van schadelijke bijproducten van oxidatieve stress werden aangezet, terwijl sommige genen geassocieerd met stress-geïnduceerde schade juist geremd werden. Deze veranderingen suggereren dat EPS niet simpelweg het oppervlak bedekken; ze herprogrammeren de beschadigde cellen actief om hun structuur te herbouwen en functie te herstellen.
Communicatie met immuuncellen tijdens herstel
Aangezien de darmbarrière niet geïsoleerd geneest, vroegen de onderzoekers hoe deze epitheliale veranderingen immuuncellen zouden kunnen beïnvloeden. Ze namen het medium van 5-FU-beschadigde, met bacterieproducten gestimuleerde epitheelculturen en gebruikten het om menselijke monocyten tot macrofagen te differentiëren. Geprepareerd medium van EPS-behandelde cellen dreef macrofagen naar een M1-achtig profiel, een toestand die typisch geassocieerd wordt met vroege ontstekingsreacties en opruiming van weefsels. Daarentegen neigde medium van culturen behandeld met de cell-vrije supernatant naar een M2-achtig profiel, vaak geassocieerd met het kalmeren van ontsteking en weefselremodellering, terwijl membraanvasjes een gemengd patroon gaven. Opmerkelijk was dat, zelfs wanneer oppervlaktemarkers een M1-achtige verschuiving suggereerden, klassieke agressieve ontstekingscytokines zoals IL‑1β en TNF‑α niet verhoogd waren, wat wijst op een meer gebalanceerde, op herstel gerichte activatie in plaats van uit de hand lopende ontsteking.
Wat dit kan betekenen voor toekomstige kankerzorg
Dit werk toont aan dat specifieke moleculen uitgescheiden door een probiotische bacterie — met name haar exopolysacchariden — darmcellen in het laboratorium kunnen helpen herstellen van door chemotherapie veroorzaakte schade. EPS verstevigden de barrière, zetten interne herstelprogramma's aan en beïnvloedden het gedrag van immuuncellen op manieren die passen bij georkestreerd weefselherstel. Hoewel de studie in celkweken werd uitgevoerd en bevestiging in diermodellen en patiënten nodig heeft, wijst het op een toekomst waarin zorgvuldig gedefinieerde bacteriële producten, in plaats van levende microben, naast chemotherapie gebruikt zouden kunnen worden om pijnlijke darmbijwerkingen te verminderen en patiënten op levensreddende behandelingen te houden.
Bronvermelding: Lasaviciute, G., López Plana, M., Sundberg Örtegren, S. et al. Limosilactobacillus reuteri metabolites modulate immune pathways and intestinal barrier repair after 5 fluorouracil exposure. Sci Rep 16, 11376 (2026). https://doi.org/10.1038/s41598-026-45524-y
Trefwoorden: chemotherapie mukositis, herstel van de darmbarrière, probiotische metabolieten, Limosilactobacillus reuteri, exopolysacchariden