Clear Sky Science · pl
Metabolity Limosilactobacillus reuteri modulują szlaki odpornościowe i naprawę bariery jelitowej po ekspozycji na 5‑fluorouracyl
Dlaczego ważna jest ochrona jelit podczas leczenia nowotworów
Chemoterapia ratuje życie, ale często uszkadza wyściółkę jamy ustnej i przewodu pokarmowego, powodując ból, biegunkę i infekcje, które mogą przerwać lub osłabić terapię. W tym badaniu sprawdzono, czy nieszkodliwe bakterie, a dokładniej cząsteczki, które wydzielają, mogą pomóc ścianie jelita w naprawie po uszkodzeniu wywołanym powszechnym lekiem przeciwnowotworowym. Praca koncentruje się na znanym szczepie probiotycznym Limosilactobacillus reuteri DSM 17938 i zadaje pytanie: czy jego wydzielane cukry i drobne cząsteczki mogą wspierać gojenie bez podawania żywych bakterii pacjentom z obniżoną odpornością?
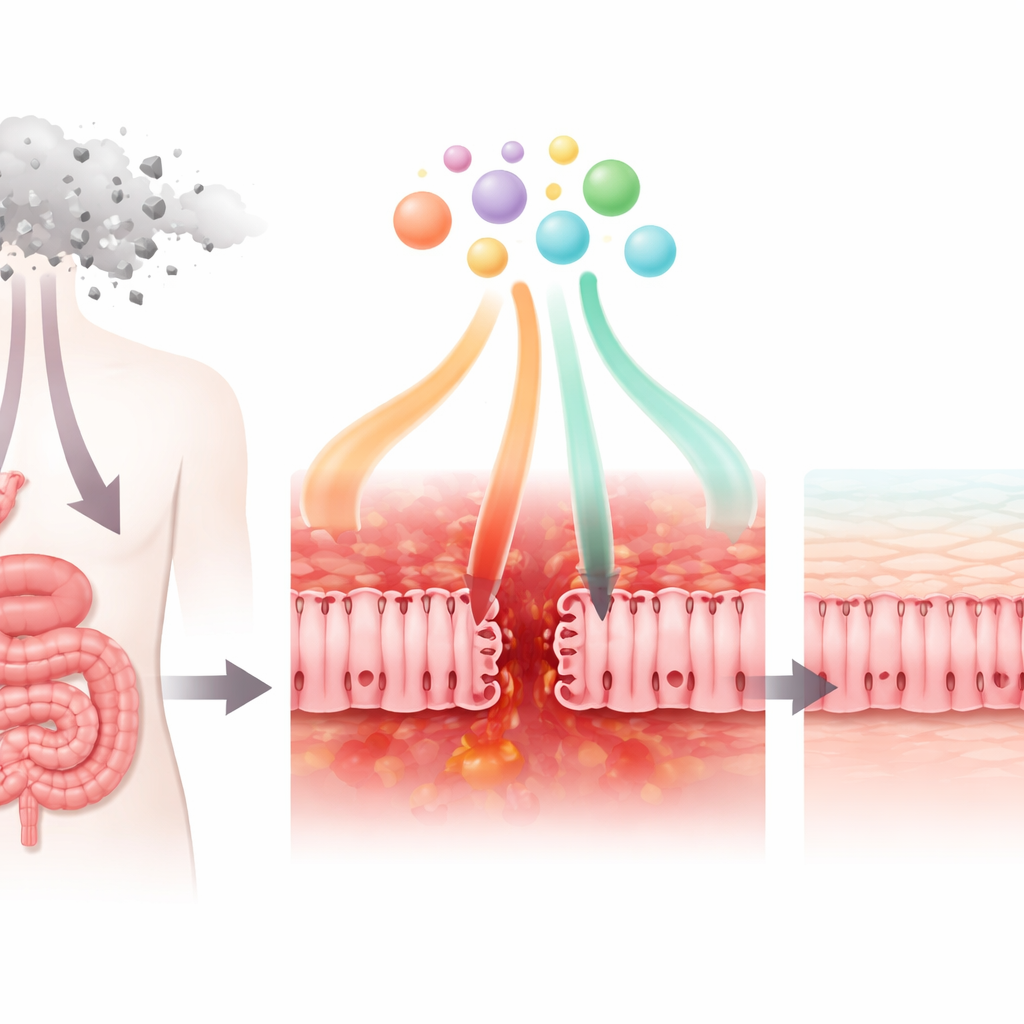
Jak powszechny lek przeciwnowotworowy uszkadza ścianę jelita
Naukowcy najpierw zbadali, jak lek chemioterapeutyczny 5‑fluorouracyl (5‑FU), szeroko stosowany w leczeniu raka piersi, żołądka i jelita grubego, wpływa na komórki przypominające nabłonek jelita cienkiego. W hodowlach in vitro 5‑FU obniżał przeżywalność tych komórek i ich normalny metabolizm. Osłabił również „zamki szczelne” (tight junctions), które łączą sąsiednie komórki, zwiększając przepuszczalność warstwy komórkowej. Mikroskopia wykazała, że kluczowe białka połączeń straciły zwyczajową uporządkowaną, sieciową aranżację i stały się zdezorganizowane. Jednocześnie komórki zaczęły wydzielać wyższe poziomy sygnałów zapalnych, takich jak chemokina CXCL8, przy jednoczesnym spadku produkcji regulatorowego czynnika TGF‑β1. Te zmiany odzwierciedlają to, co dzieje się u pacjentów, gdy bariera jelitowa jest uszkodzona, zaogniona i mniej zdolna do blokowania drobnoustrojów.
Pomocne cukry od przyjaznych bakterii
Zespół zwrócił się następnie ku produktom wytwarzanym przez L. reuteri DSM 17938: pozbawionemu komórek supernatantowi zawierającemu liczne wydzielone cząsteczki, oczyszczonym egzopolisacharydom (EPS, długie łańcuchy cukrowe) oraz drobnym pęcherzykom błonowym. Dodano je dopiero po wypłukaniu leku chemioterapeutycznego, naśladując leczenie wspomagające, a nie ochronę podaną wcześniej. Zarówno w linii komórkowej przypominającej nabłonek jelita, jak i w pierwotnych ludzkich komórkach jelita cienkiego od dawcy, EPS wyraźnie poprawiły funkcję bariery. Opór elektryczny przez warstwę komórek wzrósł, a przepływ fluorescencyjnego znacznika przez barierę zmalał, co wskazuje na szczelniejsze zamknięcie. Co ciekawe, EPS i inne produkty bakteryjne zwiększyły także wydzielanie CXCL8 i innej chemokiny, CCL20, szczególnie po stronie zwróconej do światła jelita. Zatem to samo leczenie, które wzmacniało barierę, jednocześnie pobudzało sygnały zwykle związane z zapaleniem.
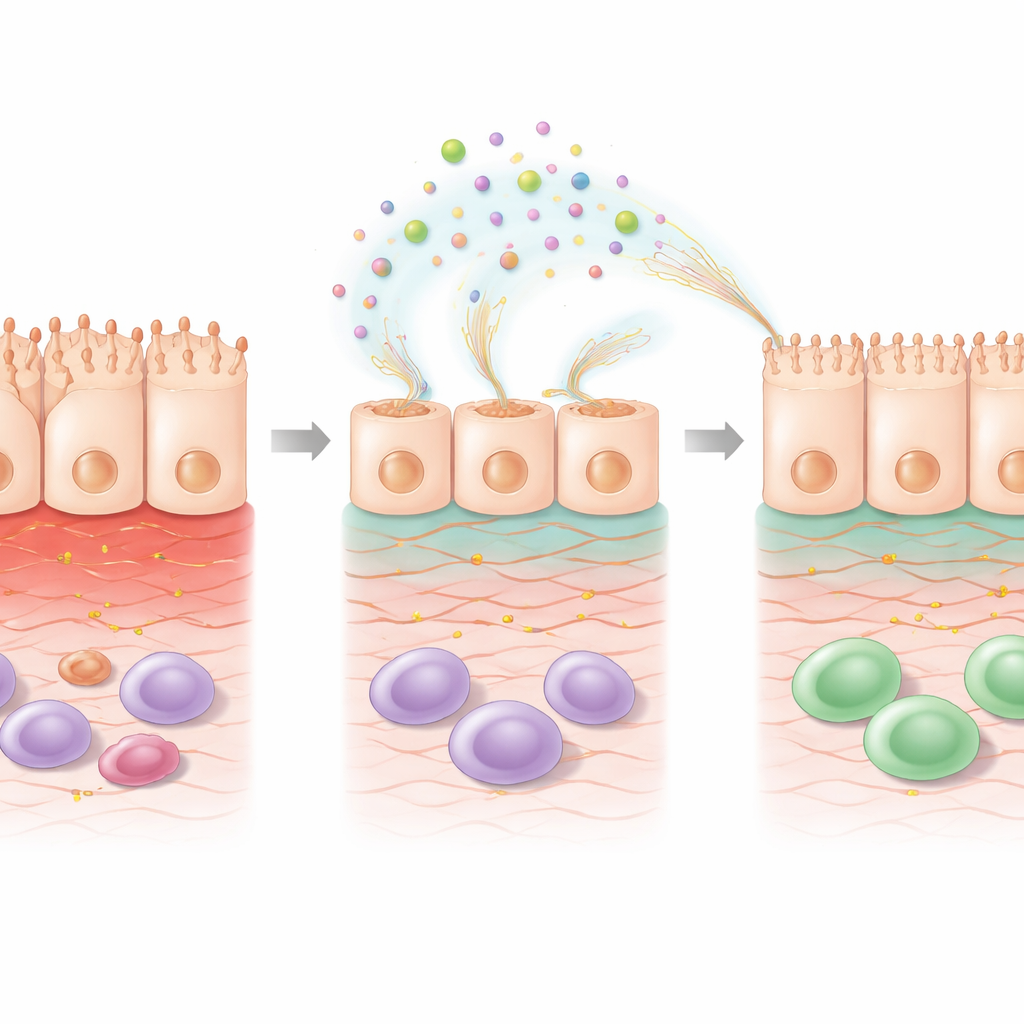
Wewnątrz komórki: uruchamianie programów naprawczych
Aby zrozumieć, co zmieniało się wewnątrz komórek, badacze przeanalizowali globalną aktywność genów po leczeniu 5‑FU z EPS lub bez niego. Sama chemioterapia zmieniała wiele genów związanych z przeżyciem komórek, radzeniem sobie ze stresem i sygnalizacją immunologiczną. Dodanie EPS na tle 5‑FU przesunęło wzorzec dalej, w kierunku wskazującym na naprawę. Uaktywniono geny zaangażowane w organizację macierzy pozakomórkowej — rusztowania wspierającego komórki — oraz szlaki powiązane z kwasem retinowym, pochodną witaminy A znaną z promowania zdrowia bariery jelitowej. Włączono także geny pomagające detoksykować szkodliwe produkty stresu oksydacyjnego, podczas gdy niektóre geny powiązane z uszkodzeniami wywołanymi stresem zostały wyciszone. Te zmiany sugerują, że EPS nie tylko powlekają powierzchnię; aktywnie przeprogramowują uszkodzone komórki, by odbudowały strukturę i przywróciły funkcję.
Rozmowa z komórkami odpornościowymi podczas gojenia
Ponieważ bariera jelitowa nie goi się w izolacji, zespół zbadał, jak zmiany w nabłonku mogą wpływać na komórki odpornościowe. Pobierali płyn z kultur nabłonkowych uszkodzonych 5‑FU i stymulowanych produktami bakteryjnymi, a następnie stosowali go do różnicowania ludzkich monocytów w makrofagi. Medium uwarunkowane przez komórki traktowane EPS kierowało makrofagi ku profilowi podobnemu do M1, stanowi zwykle związany z wczesną odpowiedzią zapalną i sprzątaniem tkanek. Natomiast medium z kultur traktowanych pozbawionym komórek supernatantem skłaniało raczej ku profilowi M2, często związanym z łagodzeniem zapalenia i przebudową tkanek, podczas gdy pęcherzyki błonowe wywoływały mieszany wzorzec. Co ważne, choć markery powierzchniowe sugerowały nachylenie ku M1, klasyczne agresywne cytokiny zapalne, takie jak IL‑1β i TNF‑α, nie były zwiększone, co sugeruje bardziej zrównoważoną, nastawioną na naprawę aktywację, a nie niekontrolowane zapalenie.
Co to może znaczyć dla przyszłej opieki onkologicznej
Praca pokazuje, że określone cząsteczki wydzielane przez bakterię probiotyczną — szczególnie jej egzopolisacharydy — mogą pomagać komórkom jelitowym w odzyskiwaniu sprawności po uszkodzeniu wywołanym chemioterapią w warunkach laboratoryjnych. EPS uszczelniały barierę, uruchamiały wewnątrzkomórkowe programy naprawcze i kształtowały zachowanie komórek odpornościowych w sposób zgodny z uporządkowanym gojeniem tkanek. Chociaż badanie przeprowadzono na hodowlach komórkowych i wymaga potwierdzenia u zwierząt i pacjentów, wskazuje na perspektywę, w której starannie zdefiniowane produkty bakteryjne, zamiast żywych mikroorganizmów, mogłyby być stosowane obok chemioterapii, aby zmniejszyć bolesne skutki uboczne w przewodzie pokarmowym i pomóc pacjentom kontynuować ratujące życie leczenie.
Cytowanie: Lasaviciute, G., López Plana, M., Sundberg Örtegren, S. et al. Limosilactobacillus reuteri metabolites modulate immune pathways and intestinal barrier repair after 5 fluorouracil exposure. Sci Rep 16, 11376 (2026). https://doi.org/10.1038/s41598-026-45524-y
Słowa kluczowe: chemoterapia zapalenie błony śluzowej, naprawa bariery jelitowej, metabolity probiotyczne, Limosilactobacillus reuteri, egzopolisacharydy