Clear Sky Science · he
מטבוליטים של Limosilactobacillus reuteri מווסתים מסלולים חיסוניים ותיקון מחסום המעי לאחר חשיפה ל-5 פלואורואורציל
מדוע חשוב להגן על המעי במהלך טיפול בסרטן
כימותרפיה מצילה חיים, אך לעיתים קרובות פוגעת ברירית הפה והמעי, וגורמת לכאב, לשלשול ולזיהומים היכולים להפריע או להחליש את הטיפול. במחקר זה נבדק האם חיידקים בלתי מזיקים, ובאופן מדויק יותר המולקולות שהם משחררים, יכולים לעזור לדופן המעי לתקן את עצמה לאחר שנפגעה מתרופה סרטנית נפוצה. העבודה מתמקדת בזן פרוביוטי מוכר, Limosilactobacillus reuteri DSM 17938, ושואלת: האם הסוכרים המופרשים והחלקיקים הזעירים שלו יכולים לתמוך בריפוי ללא מתן חיידקים חיים לחולים פגיעים?
כיצד תרופה נפוצה לפגיעה בסיכון המעי
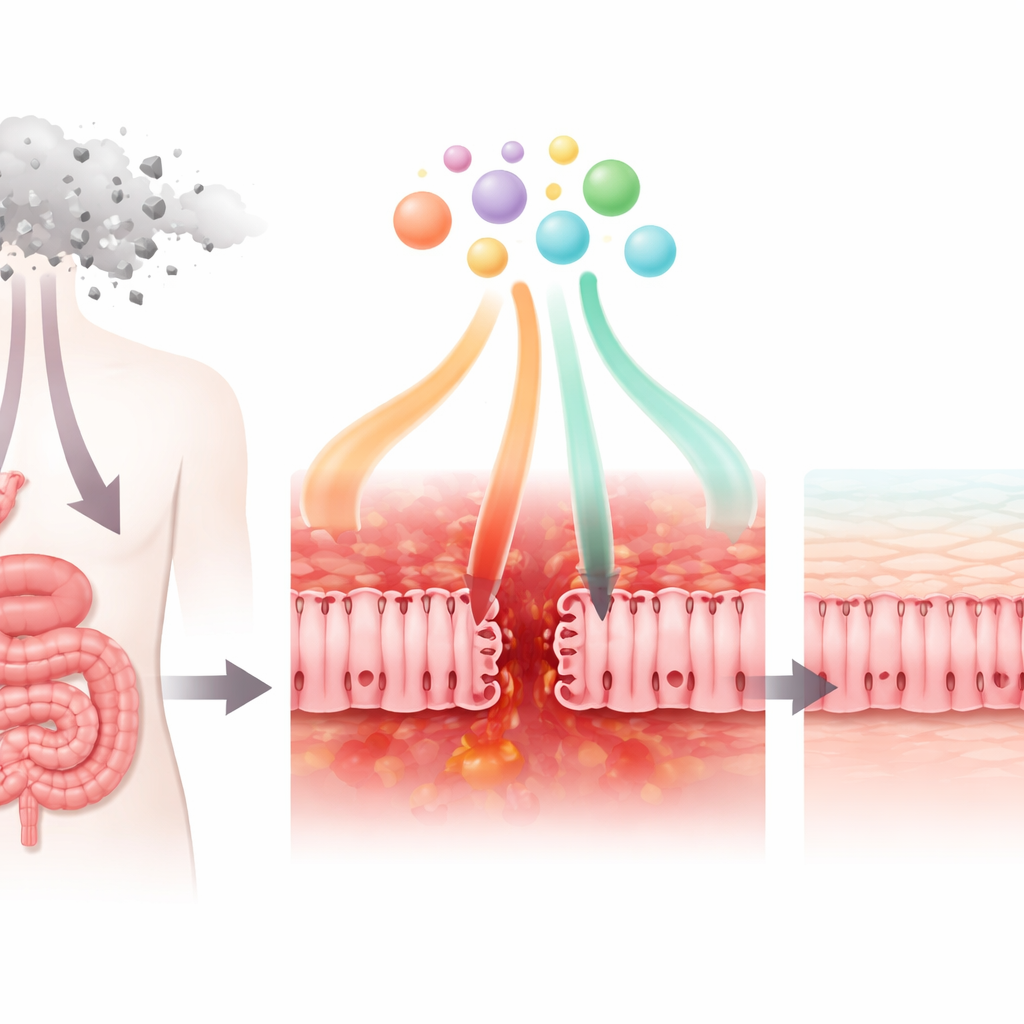
החוקרים בחנו תחילה כיצד תרופת הכימותרפיה 5-פלואורואורציל (5-FU), המשמשת נרחב נגד סרטן השד, הקיבה והמעי הגס, משפיעה על תאים המדמים את התאים המצפים את המעי הדק. בצלחות מעבדה, 5-FU הפחיתה את הישרדות התאים ואת הפעילות המטבולית שלהם. היא גם החלישה את ה"חיבורים הצפופים" שמחזיקים תאים שכנים יחד, והפכה את שכבת התאים לדליפה יותר. במיקרוסקופ נצפה כי חלבוני החיבור החיוניים איבדו את הסידור המסודר והנטו להתפורר. במקביל, התאים החלו להפריש רמות גבוהות יותר של איתותים דלקתיים, כגון הכימוקין CXCL8, בעוד שהפיקו פחות מהגורם הרגולטורי TGF-β1. שינויים אלו משקפים יחד את מה שקורה בחולים כאשר מחסום המעי נפגע, מתנפח ופחות מסוגל למנוע חדירת מיקרובים.
סוכרים מועילים מחיידקים ידידותיים
בהמשך פנו החוקרים לתוצרים שמייצר L. reuteri DSM 17938: תת-עירור חסר-תאים המכיל מולקולות מופרשות רבות, אקסופוליסכרידים מזוקקים (EPS, שרשרות סוכר ארוכות) ושלפוחיות ממברנה זעירות. אלה נוספו רק לאחר שטופל הכימותרפיה ונשטף, בדומה לטיפול תומך ולא למגן שניתן מראש. הן בקו תאי סרטני המדמה אפיתל מעי והן בתאים ראשוניים של המעי הדק האנושי מתורם, ה-EPS שיפרו באופן ברור את תפקוד המחסום. ההתנגדות החשמלית בחוצץ התאי עלתה, ומעבר של חומר פלואורסצנטי דרך המחסום פחת, מה שמעיד על איטום הדוק יותר. מעניין כי ה-EPS ומוצרי החיידק האחרים גם הגבירו את שחרור ה-CXCL8 וכימוקין נוסף, CCL20, במיוחד בצד הפונה ללומן המעי. לפיכך, אותו טיפול שהחיש את המחסום גם עורר איתותים שבדרך כלל מקושרים לדלקת.
בתוך התא: תוכניות תיקון נדלקות
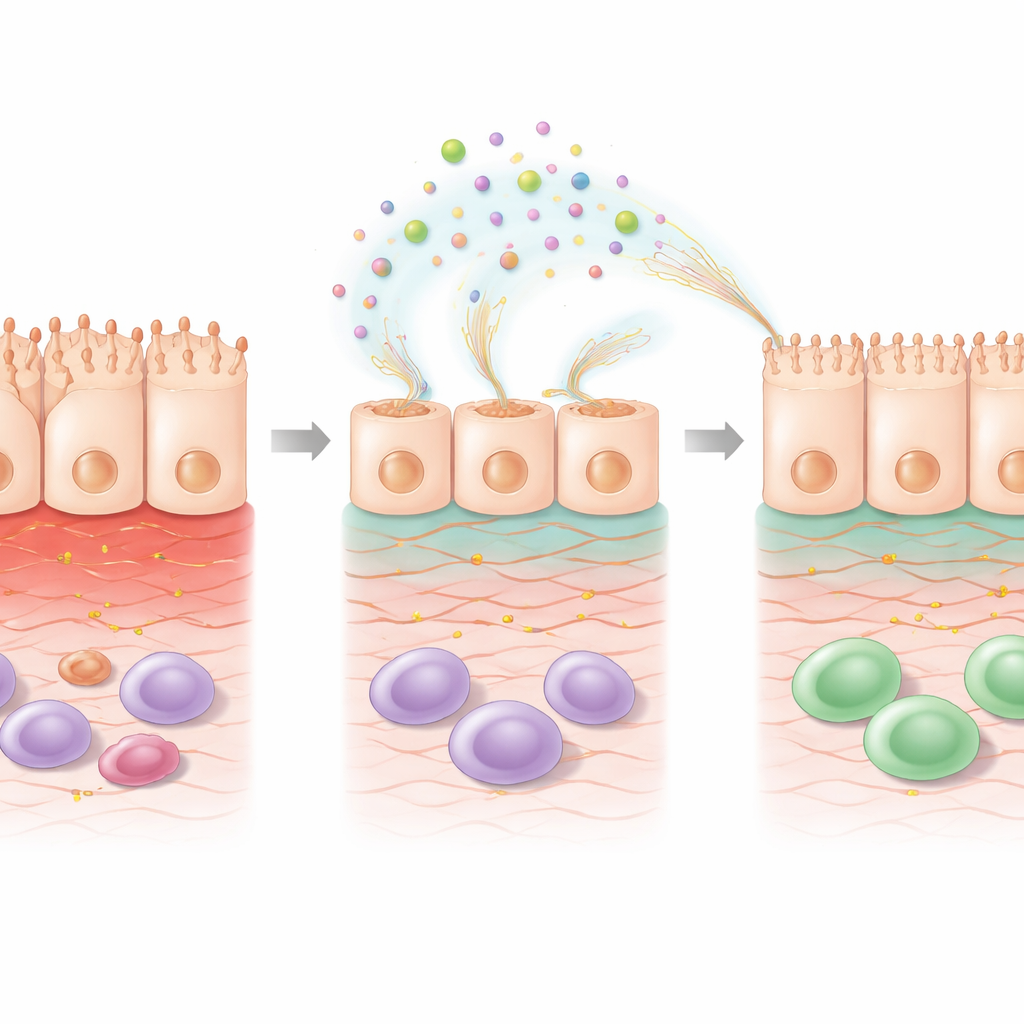
כדי להבין מה משתנה בתוך התאים, המדענים ניתחו פעילות גנים גלובלית לאחר טיפול ב-5-FU עם או בלי EPS. הכימותרפיה לבדה שינתה ביטוי של גנים רבים הקשורים בהישרדות התאים, בהתמודדות עם לחץ ובאיתות חיסוני. הוספת EPS על 5-FU הסיטה את התבנית עוד יותר, בכיוון שמצביע על תיקון. גנים המעורבים בארגון המטריצה החוץ-תאית—השלד התומך בתאים—ובדרכי אותות הקשורות לחומצה רטינואית, מולקולה נגזרת ויטמין A הידועה בקידום בריאות מחסום המעי, הועלו. גנים אחרים המסייעים לנטרול תוצרי לוואי מזיקים של מתח חמצוני הופעלו, בעוד שחלק מהגנים המקושרים לנזק המושרה על ידי סטרס הוקלו. שינויים אלה מרמזים כי ה-EPS אינם פשוט מצפים את המשטח; הם מתכנתים באופן פעיל את התאים הנפגעים לשקם את המבנה ולשחזר תפקוד.
שיח צולב עם תאי חיסון במהלך הריפוי
מכיוון שמחסום המעי אינו מתחבר בבדידות, הצוות בדק כיצד השינויים האפיתליאלים האלה עשויים להשפיע על תאי חיסון. הם לקחו את הנוזל מתוך תרביות אפיתל שנפגעו ב-5-FU וגורמו לתגובה על-ידי מוצרי חיידק, והשתמשו בו כדי לגרום למונוציטים אנושיים להתמיינות למקרופאגים. המדיה המותנית מתאים שטופלו ב-EPS דחפה את המקרופאגים לפרופיל דמוי M1, מצב המקושר בדרך כלל לתגובות דלקתיות מוקדמות וניקוי רקמות. לעומת זאת, מדיה מתרביות שטופלו בתת-עירור חסר-תאים נטתה לתמוך בפרופיל דמוי M2, לעתים קרובות מקושר להרגעת הדלקת ושחזור רקמה, בעוד שלפחותת הממברנה יצרו דפוס מעורב. ראוי לציין שגם כאשר סימני שטח הרמזו על הסטיה לכיוון M1, ציטוקינים דלקתיים אגרסיביים קלאסיים כגון IL‑1β ו-TNF‑α לא הוגברו, דבר שמרמז על הפעלה מאוזנת ומוקדמת יותר המיועדת לתיקון ולא לדלקת יוצאת משליטה.
מה משמעות הדבר לטיפול בסרטן בעתיד
העבודה מצביעה על כך שמולקולות ספציפיות המופרשות על ידי חיידק פרוביוטי—בפרט האקסופוליסכרידים שלו—יכולות לסייע לתאי מעי להתאושש מפגיעה שנגרמה על ידי כימותרפיה בתנאי מעבדה. ה-EPS חיזקו את המחסום, הפעילו תוכניות תיקון פנימיות וצביעו את התנהגות תאי החיסון באופן התואם לריפוי מתואם של רקמות. למרות שהמחקר בוצע בתרביות תאים וצריך אישור בניסויים בחיות ובחולים, הוא מצביע לכיוון עתיד שבו תוצרים חיידקיים מוגדרים בקפידה, במקום מיקרובים חיים, עשויים להינתן לצד כימותרפיה להפחתת תופעות הלוואי הקשות במעי ולעזור לחולים להמשיך טיפול מציל חיים.
ציטוט: Lasaviciute, G., López Plana, M., Sundberg Örtegren, S. et al. Limosilactobacillus reuteri metabolites modulate immune pathways and intestinal barrier repair after 5 fluorouracil exposure. Sci Rep 16, 11376 (2026). https://doi.org/10.1038/s41598-026-45524-y
מילות מפתח: מוקוסיטיס כימותרפיה, תיקון מחסום מעי, מטבוליטים פרוביוטיים, Limosilactobacillus reuteri, אקסופוליסכרידים