Clear Sky Science · tr
Limosilactobacillus reuteri metabolitleri, 5-florourasil maruziyetinden sonra bağışıklık yollarını ve bağırsak bariyerinin onarımını modüle ediyor
Neden kanser tedavisi sırasında bağırsak koruması önemli
Kemoterapi hayat kurtarıyor, ancak ağız ve bağırsak yüzeyini sıklıkla zedeleyerek ağrı, ishal ve enfeksiyonlara yol açar; bu durum tedavinin kesilmesine veya etkinliğinin azalmasına neden olabilir. Bu çalışma, zararsız bakterilerin —daha doğrusu onların salgıladığı moleküllerin— yaygın bir kanser ilacı tarafından hasar görmüş bağırsak duvarının onarımına yardımcı olup olamayacağını araştırıyor. Çalışma, iyi bilinen bir probiyotik suşu olan Limosilactobacillus reuteri DSM 17938’e odaklanıyor ve şu soruyu soruyor: Canlı bakteri vermeye gerek kalmadan, bu bakterinin salgıladığı şekerler ve küçük parçacıklar iyileşmeyi destekleyebilir mi?
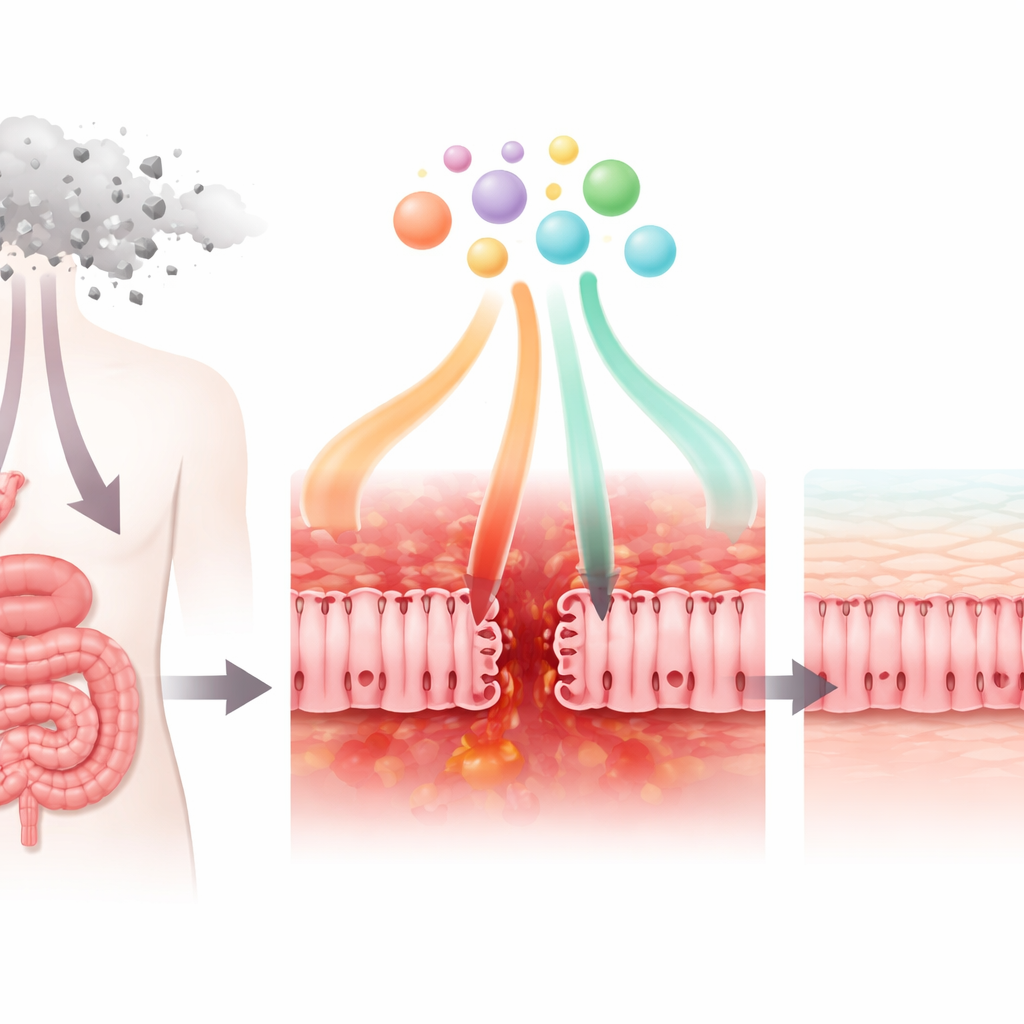
Yaygın bir kanser ilacının bağırsak duvarına nasıl zarar verdiği
Araştırmacılar önce, meme, mide ve kolon kanserlerine karşı yaygın olarak kullanılan kemoterapi ilacı 5-florourasil’in (5-FU) ince bağırsak yüzeyine benzer hücreleri nasıl etkilediğini incelediler. Laboratuvar ortamında 5-FU, bu hücrelerin hayatta kalma ve normal metabolik işlevlerini sürdürme yeteneğini azalttı. Ayrıca komşu hücreleri bir arada tutan “sıkı bağlantıları” zayıflatarak hücre tabakasının daha geçirgen hale gelmesine yol açtı. Mikroskopik inceleme, önemli bağlantı proteinlerinin olağan düzenli, ağ benzeri yapılarını kaybedip dağınık hale geldiğini gösterdi. Aynı zamanda hücreler, kemokin CXCL8 gibi inflamatuvar sinyallerin salgılanmasını artırdı ve düzenleyici faktör TGF-β1 üretimini azalttı. Bu değişiklikler birlikte, bağırsak bariyerinin hasarlandığında, iltihaplandığında ve mikropları dışarıda tutmakta daha az etkin olduğunda hastalarda görülen durumu yansıtıyor.
Dost bakterilerden gelen yararlı şekerler
Ekip daha sonra L. reuteri DSM 17938 tarafından üretilen ürünlere yöneldi: birçok salgılanmış molekül içeren hücresiz süpernatant, saflaştırılmış egzopolisakkaritler (EPS, uzun şeker zincirleri) ve küçük zar vezikülleri. Bunlar, kemoterapi ilacı yıkandıktan sonra —koruyucu bir önlem yerine destek tedavisini taklit ederek— yalnızca sonrasında eklendi. Hem bağırsak benzeri kanser hücre hattında hem de bir donörden alınmış insan ince bağırsak primer hücrelerinde, EPS bariyer fonksiyonunu belirgin şekilde iyileştirdi. Hücre tabakası boyunca elektriksel direnç arttı ve bariyer üzerinden floresan izleyicinin geçişi azaldı; bu da daha sıkı bir sızdırmazlığa işaret ediyor. İlginç olarak, EPS ve diğer bakteriyel ürünler ayrıca CXCL8 ve bir başka kemokin olan CCL20 salınımını özellikle bağırsak lümenine bakan tarafta artırdı. Böylece bariyeri güçlendiren aynı tedavi, tipik olarak inflamasyonla ilişkilendirilen sinyalleri de harekete geçirdi.
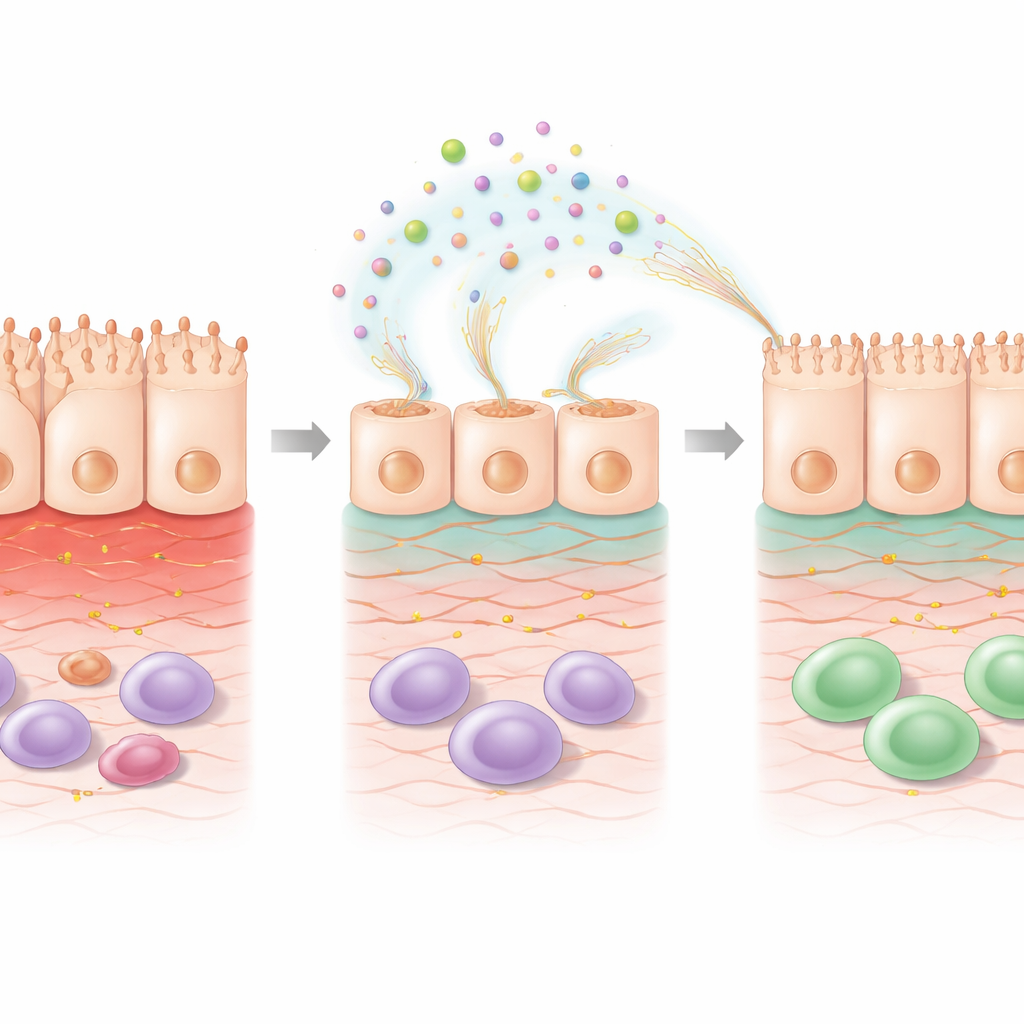
Hücre içinde: onarım programları devreye giriyor
Hücrelerin içinde nelerin değiştiğini anlamak için bilim insanları 5-FU tedavisi sonrası, EPS ile veya EPS olmadan, global gen aktivitesini analiz ettiler. Sadece kemoterapi, hücre hayatta kalması, stres yanıtı ve bağışıklık sinyalleşmesi ile ilişkili birçok geni değiştirdi. 5-FU üzerine EPS eklenmesi ise deseni daha da onarıma yönlendiren bir şekilde kaydırdı. Hücreleri destekleyen iskelet olan ekstracelüler matriksin düzenlenmesiyle ilişkili genler ve bağırsak bariyeri sağlığını desteklediği bilinen A vitamini türevi retinoik asitle bağlantılı yolaklarla ilişkili genler yukarı yönlü düzenlendi. Oksidatif stresin zararlı yan ürünlerini detoksifiye etmeye yardımcı genler aktifleştirildi, stres kaynaklı hasarla ilişkili bazı genler ise bastırıldı. Bu değişiklikler, EPS’nin sadece yüzeyi kaplamadığını; aynı zamanda yaralanmış hücreleri yapılarını yeniden inşa etmeye ve işlevi geri kazanmaya yönelik aktif bir biçimde programladığını düşündürüyor.
İyileşme sırasında bağışıklık hücreleriyle karşılıklı iletişim
Bağırsak bariyeri izole olarak iyileşmediği için ekip, epiteldeki bu değişikliklerin bağışıklık hücrelerini nasıl etkileyebileceğini sordu. 5-FU ile hasar görmüş, bakteri ürünü ile uyarılmış epitel kültürlerinden elde edilen sıvıyı alıp insan monositleri bu ortamda büyüterek makrofajlara dönüştürdüler. EPS ile muamele edilmiş hücrelerden elde edilen kondisiyonlu ortam makrofajları tipik olarak erken inflamatuvar yanıtlar ve doku temizliğiyle ilişkilendirilen M1-benzeri bir profile itti. Buna karşılık, hücresiz süpernatant ile muamele edilmiş kültürlerden elde edilen ortam genellikle inflamasyonu yatıştırma ve doku yeniden düzenlemesiyle ilişkili M2-benzeri bir profili destekledi; zar vezikülleri ise karışık bir desen üretti. Dikkate değer olarak, yüzey belirteçleri M1-benzeri bir eğilimi işaret etse bile, klasik güçlü inflamatuvar sitokinler olan IL‑1β ve TNF‑α artmadı; bu durum, kontrolden çıkmış bir inflamasyon yerine daha dengeli, onarıma odaklı bir aktivasyonu ima ediyor.
Gelecekteki kanser bakımına olası etkileri
Bu çalışma, bir probiyotik bakterinin —özellikle egzopolisakkaritlerinin— belirli moleküllerinin laboratuvar ortamında kemoterapi kaynaklı yaralanmadan sonra bağırsak hücrelerinin toparlanmasına yardımcı olabileceğini gösteriyor. EPS bariyeri sıkılaştırdı, iç onarım programlarını açtı ve bağışıklık hücresi davranışını düzenleyerek organize bir doku iyileşmesini destekleyen biçimde etkiledi. Çalışma hücre kültürlerinde yapıldığından, hayvanlarda ve hastalarda doğrulamaya ihtiyaç duyulsa da, canlı mikroplar yerine dikkatle tanımlanmış bakteri ürünlerinin kemoterapiye eşlik ederek ağrılı bağırsak yan etkilerini azaltmak ve hastaların hayat kurtaran tedavilere devam etmesini sağlamak için kullanılabileceği bir geleceğe işaret ediyor.
Atıf: Lasaviciute, G., López Plana, M., Sundberg Örtegren, S. et al. Limosilactobacillus reuteri metabolites modulate immune pathways and intestinal barrier repair after 5 fluorouracil exposure. Sci Rep 16, 11376 (2026). https://doi.org/10.1038/s41598-026-45524-y
Anahtar kelimeler: kemoterapi mukoziti, bağırsak bariyerinin onarımı, probiyotik metabolitleri, Limosilactobacillus reuteri, ekzopolisakkaritler