Clear Sky Science · de
Limosilactobacillus reuteri-Metaboliten modulieren Immunwege und Reparatur der Darmbarriere nach 5‑Fluorouracil-Exposition
Warum der Schutz des Darms während der Krebsbehandlung wichtig ist
Chemotherapie rettet Leben, schädigt aber häufig die Schleimhäute von Mund und Darm und verursacht Schmerzen, Durchfall und Infektionen, die die Behandlung unterbrechen oder abschwächen können. Diese Studie untersucht, ob harmlose Bakterien — oder genauer die von ihnen freigesetzten Moleküle — der Darmwand helfen können, sich nach einer Schädigung durch ein gängiges Krebsmedikament selbst zu reparieren. Die Arbeit konzentriert sich auf einen bekannten Probiotika-Stamm, Limosilactobacillus reuteri DSM 17938, und fragt: Können seine sekretorischen Zucker und winzigen Partikel die Heilung unterstützen, ohne lebende Bakterien an gefährdete Patientinnen und Patienten zu verabreichen?
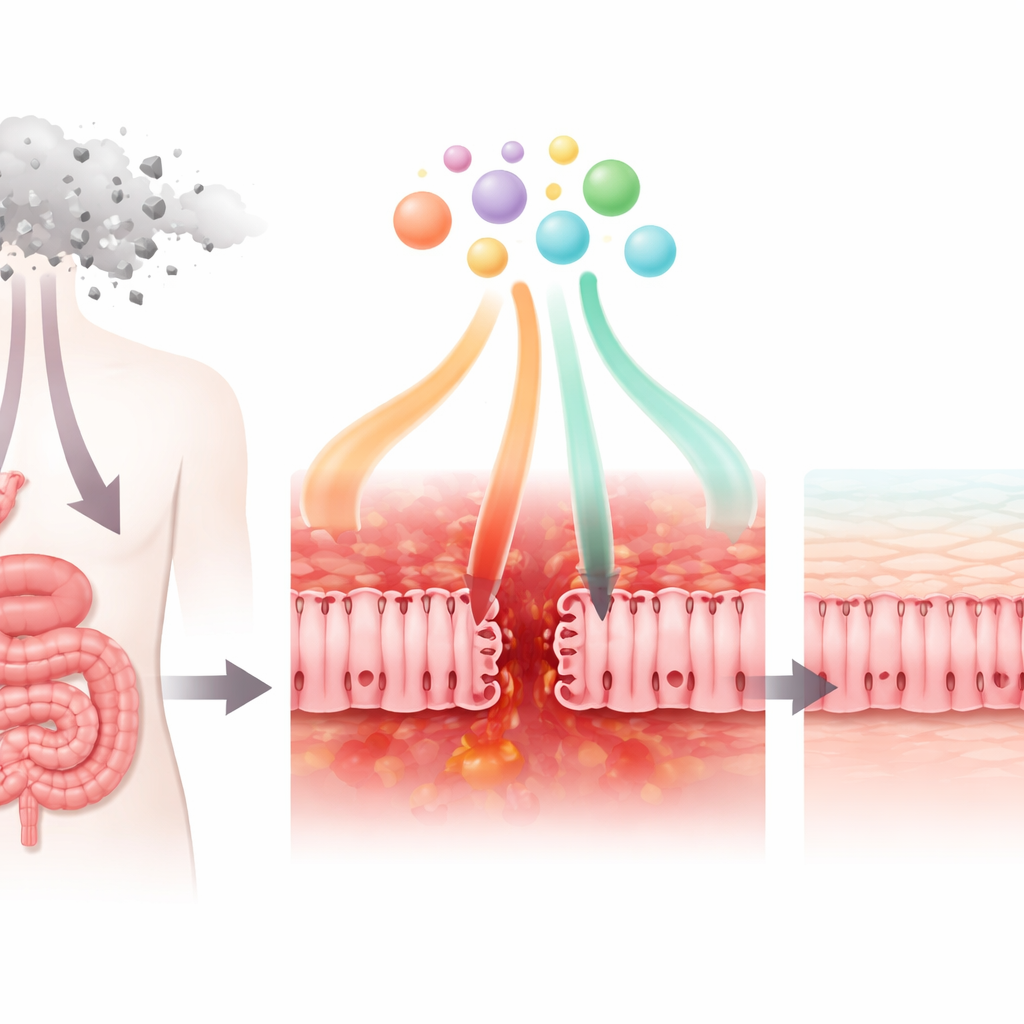
Wie ein gängiges Krebsmedikament die Darmwand schädigt
Die Forschenden untersuchten zunächst, wie das Chemotherapeutikum 5‑Fluorouracil (5‑FU), das häufig bei Brust-, Magen‑ und Darmkrebs eingesetzt wird, Zellen beeinflusst, die denen der Dünndarmschleimhaut ähneln. In Zellkultur verringerte 5‑FU das Überleben und die normale Stoffwechselaktivität dieser Zellen. Es schwächte außerdem die sogenannten Tight‑Junctions, die benachbarte Zellen zusammenhalten, wodurch die Zellschicht durchlässiger wurde. Mikroskopisch zeigte sich, dass wichtige Junction‑Proteine ihre geordnete, netzartige Anordnung verloren und desorganisiert waren. Gleichzeitig begannen die Zellen, mehr entzündliche Signale wie den Chemokine CXCL8 auszuschütten, während die Produktion des regulatorischen Faktors TGF‑β1 abnahm. Zusammengenommen spiegeln diese Veränderungen das wider, was bei Patientinnen und Patienten passiert, wenn die Darmbarriere geschädigt, entzündet ist und Mikroben schlechter abhalten kann.
Hilfreiche Zucker von freundlichen Bakterien
Das Team wandte sich dann den Produkten von L. reuteri DSM 17938 zu: einem zellfreien Überstand, der viele sekretierte Moleküle enthält, gereinigten Exopolysacchariden (EPS, lange Zuckerketten) und winzigen Membranvesikeln. Diese wurden erst nach dem Entfernen des Chemotherapeutikums zugegeben, wodurch eine unterstützende Behandlung und kein vorbeugender Schutz imitiert wurde. Sowohl in einer darmähnlichen Krebszelllinie als auch in primären menschlichen Dünndarmzellen eines Spenders verbesserte EPS deutlich die Barrierefunktion. Der elektrische Widerstand über die Zellschicht stieg und der Durchtritt eines fluoreszierenden Tracers sank, was auf eine festere Abdichtung hinweist. Interessanterweise steigerten EPS und die anderen Bakterienprodukte auch die Freisetzung von CXCL8 und einem weiteren Chemokine, CCL20, besonders auf der dem Darmlumen zugewandten Seite. Somit löste dieselbe Behandlung, die die Barriere stärkte, gleichzeitig Signale aus, die typischerweise mit Entzündung verbunden sind.
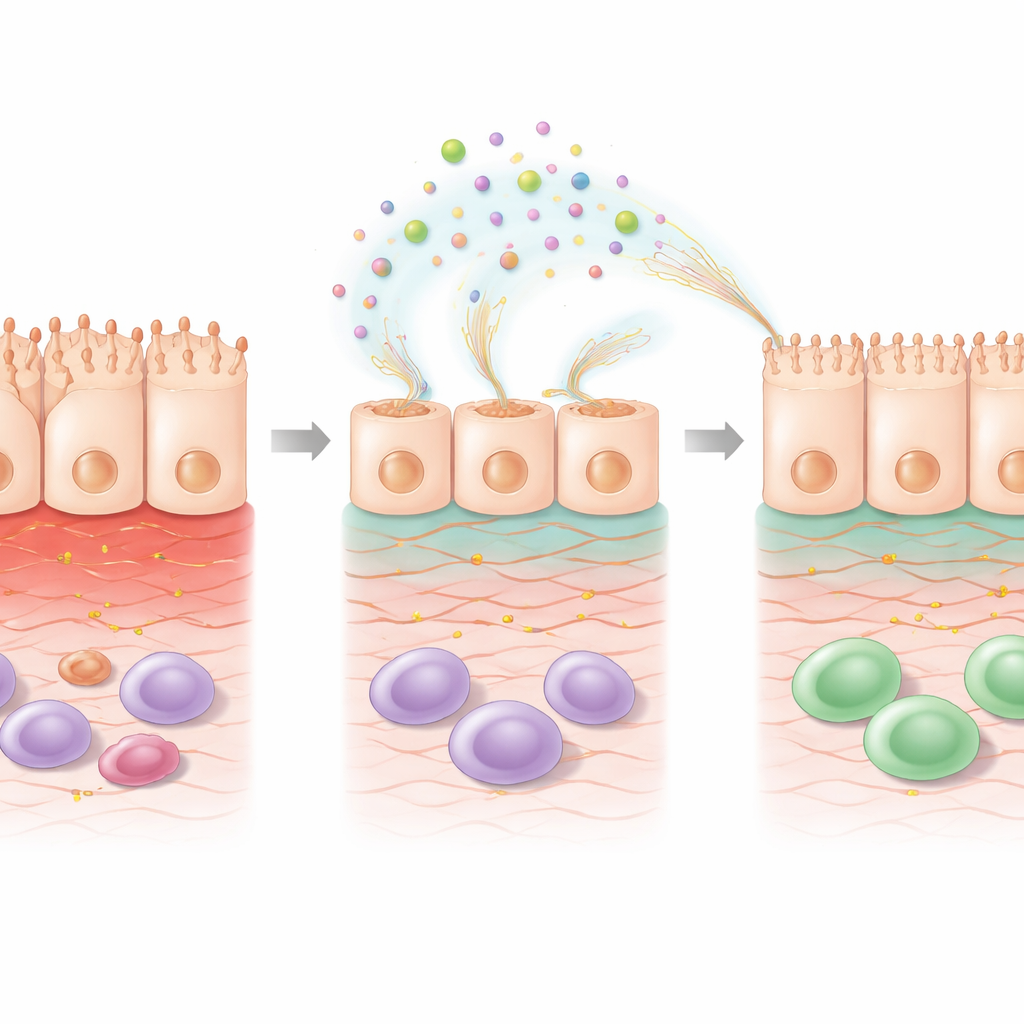
Im Inneren der Zelle: Reparaturprogramme schalten sich ein
Um zu verstehen, was sich innerhalb der Zellen veränderte, analysierten die Wissenschaftler die globale Genaktivität nach 5‑FU‑Behandlung mit und ohne EPS. Allein durch die Chemotherapie wurden viele Gene verändert, die mit Zellüberleben, Stressbewältigung und Immun‑Signalgebung zusammenhängen. Die Zugabe von EPS zu 5‑FU verschob das Expressionsmuster weiter in Richtung Reparatur. Gene, die an der Organisation der extrazellulären Matrix — dem Gerüst, das Zellen stützt — beteiligt sind, sowie Signalwege im Zusammenhang mit Retinsäure, einem aus Vitamin‑A‑abgeleiteten Molekül, das die Darmbarriere fördert, wurden hochreguliert. Andere Gene, die bei der Entgiftung schädlicher Nebenprodukte oxidativen Stresses helfen, wurden angeschaltet, während einige Gene, die mit stressbedingten Schäden verbunden sind, herunterreguliert wurden. Diese Veränderungen deuten darauf hin, dass EPS nicht einfach eine äußerliche Schicht bilden; sie programmieren die verletzten Zellen aktiv um, damit diese ihre Struktur wiederaufbauen und ihre Funktion återherstellen.
Kommunikation mit Immunzellen während der Heilung
Da die Darmbarriere nicht isoliert heilt, untersuchte das Team, wie diese epithelialen Veränderungen Immunzellen beeinflussen könnten. Sie verwendeten das Medium aus 5‑FU‑geschädigten, mit Bakterienprodukten stimulierten Epithelkulturen, um menschliche Monozyten zu Makrophagen zu differenzieren. Konditioniertes Medium aus EPS‑behandelten Zellen trieb Makrophagen in Richtung eines M1‑ähnlichen Profils, eines Zustands, der typischerweise mit frühen Entzündungsreaktionen und Reinigung des Gewebes verbunden ist. Im Gegensatz dazu förderte Medium aus Kulturen, die mit dem zellfreien Überstand behandelt worden waren, eher ein M2‑ähnliches Profil, das oft mit Dämpfung von Entzündungen und Gewebeumbau einhergeht, während Membranvesikeln ein gemischtes Muster erzeugten. Bemerkenswerterweise waren klassische proinflammatorische Zytokine wie IL‑1β und TNF‑α trotz eines M1‑ähnlichen Marker‑Profils nicht erhöht, was auf eine ausgewogenere, reparaturorientierte Aktivierung statt einer unkontrollierten Entzündung hindeutet.
Was das für die künftige Krebsversorgung bedeuten könnte
Diese Arbeit zeigt, dass spezifische Moleküle, die von einem Probiotikum freigesetzt werden — insbesondere seine Exopolysaccharide — Darmzellen im Labor bei der Erholung von chemotherapiebedingten Schäden unterstützen können. EPS stärkten die Barriere, schalteten interne Reparaturprogramme an und beeinflussten das Verhalten von Immunzellen in einer Weise, die zu orchestrierter Gewebeheilung passt. Obwohl die Studie in Zellkulturen durchgeführt wurde und Bestätigungen in Tiermodellen und beim Menschen benötigt, weist sie auf eine Zukunft hin, in der sorgfältig definierte bakterielle Produkte anstelle lebender Mikroben begleitend zur Chemotherapie eingesetzt werden könnten, um schmerzhafte Darmnebenwirkungen zu reduzieren und Patientinnen und Patienten das Fortsetzen lebensrettender Behandlungen zu erleichtern.
Zitation: Lasaviciute, G., López Plana, M., Sundberg Örtegren, S. et al. Limosilactobacillus reuteri metabolites modulate immune pathways and intestinal barrier repair after 5 fluorouracil exposure. Sci Rep 16, 11376 (2026). https://doi.org/10.1038/s41598-026-45524-y
Schlüsselwörter: Chemotherapie-Mukositis, Reparatur der Darmbarriere, probiotische Metaboliten, Limosilactobacillus reuteri, Exopolysaccharide