Clear Sky Science · pt
Metabólitos de Limosilactobacillus reuteri modulam vias imunes e a reparação da barreira intestinal após exposição ao 5-fluorouracil
Por que proteger o intestino durante o tratamento do câncer importa
A quimioterapia salva vidas, mas frequentemente danifica o revestimento da boca e do intestino, causando dor, diarreia e infecções que podem interromper ou enfraquecer o tratamento. Este estudo investiga se bactérias inofensivas, ou mais precisamente as moléculas que elas liberam, podem ajudar a parede intestinal a se reparar após lesão provocada por um fármaco oncológico comum. O trabalho foca numa cepa probiótica bem conhecida, Limosilactobacillus reuteri DSM 17938, e pergunta: seus açúcares secretados e partículas minúsculas podem apoiar a cicatrização sem a necessidade de administrar bactérias vivas a pacientes vulneráveis?
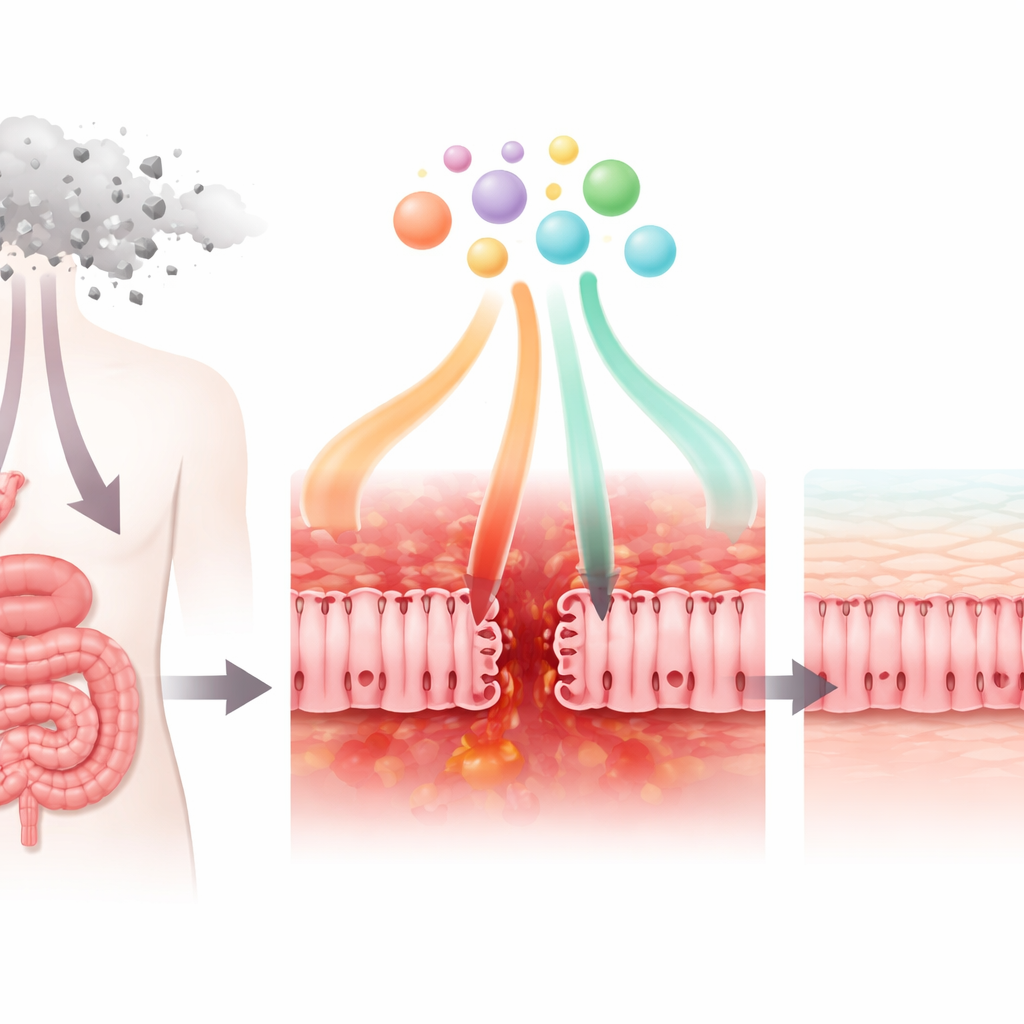
Como um fármaco comum contra o câncer prejudica a parede intestinal
Os pesquisadores primeiro examinaram como o fármaco quimioterápico 5‑fluorouracil (5‑FU), amplamente usado contra câncer de mama, estômago e cólon, afeta células que se assemelham às que revestem o intestino delgado. Em placas de cultura, o 5‑FU reduziu a sobrevivência dessas células e seu metabolismo normal. Também enfraqueceu as “junções apertadas” que mantêm as células vizinhas unidas, tornando a camada celular mais permeável. A microscopia revelou que proteínas chave das junções perderam sua organização habitual em padrão de rede e ficaram desordenadas. Ao mesmo tempo, as células passaram a secretar níveis maiores de sinais inflamatórios, como a quimiocina CXCL8, enquanto produziam menos do fator regulador TGF‑β1. Juntas, essas alterações refletem o que acontece em pacientes quando a barreira intestinal é danificada, inflamada e menos capaz de conter microrganismos.
Açúcares úteis de bactérias amigas
Em seguida, a equipe voltou sua atenção aos produtos fabricados por L. reuteri DSM 17938: um sobrenadante livre de células contendo muitas moléculas secretadas, exopolissacarídeos (EPS, longas cadeias de açúcar) purificados, e pequenas vesículas de membrana. Esses produtos foram adicionados apenas depois que o fármaco quimioterápico foi lavado, imitando um tratamento de apoio em vez de uma proteção preventiva. Tanto na linhagem celular tipo intestinal quanto em células primárias do intestino delgado humano de um doador, os EPS melhoraram claramente a função de barreira. A resistência elétrica através da camada celular aumentou e a passagem de um traçador fluorescente pelo revestimento diminuiu, indicando um selamento mais eficaz. Curiosamente, os EPS e outros produtos bacterianos também aumentaram a liberação de CXCL8 e de outra quimiocina, CCL20, especialmente no lado voltado ao lúmen intestinal. Assim, o mesmo tratamento que fortaleceu a barreira também estimulou sinais tipicamente associados à inflamação.
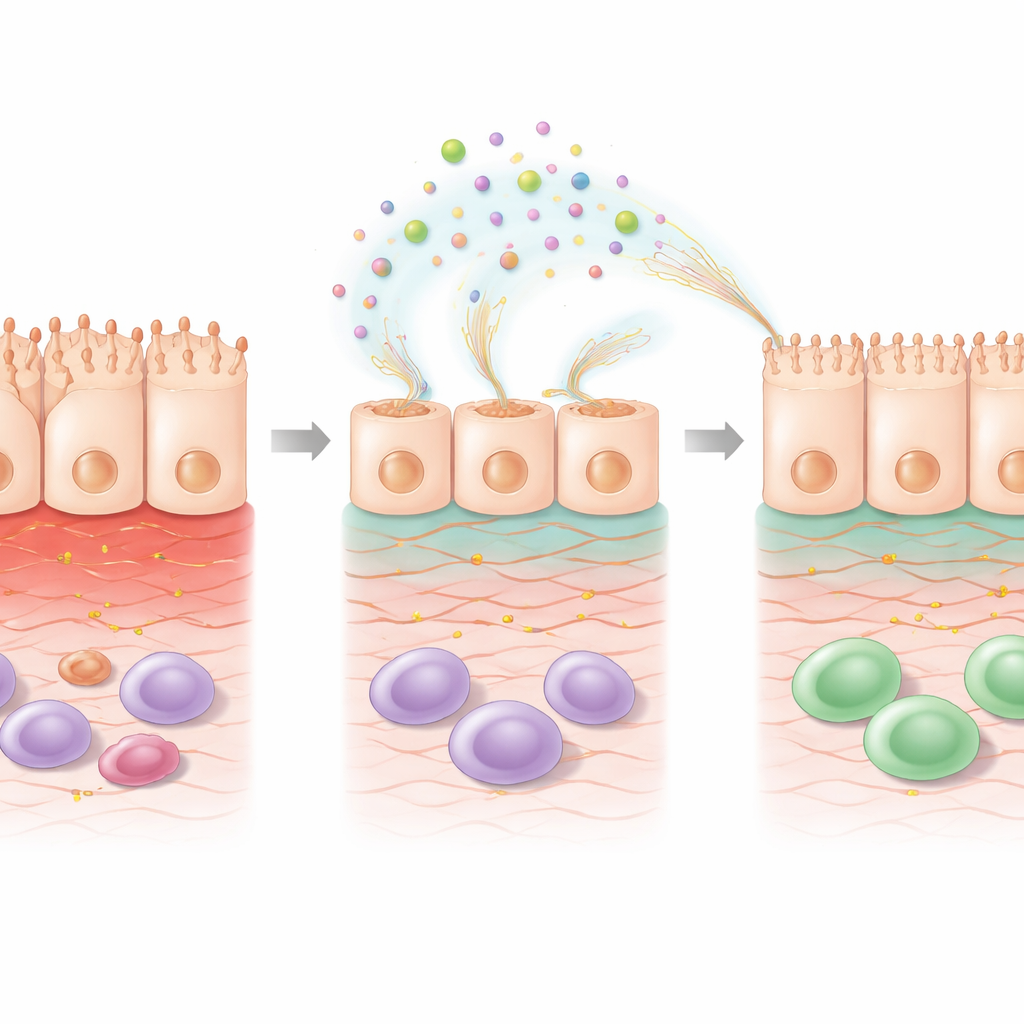
Dentro da célula: programas de reparo são ativados
Para entender o que mudava dentro das células, os cientistas analisaram a atividade gênica global após tratamento com 5‑FU com ou sem EPS. A quimioterapia por si só alterou muitos genes relacionados à sobrevivência celular, manejo de estresse e sinalização imune. A adição de EPS sobre o 5‑FU mudou ainda mais o padrão, de modo a apontar para reparo. Genes envolvidos na organização da matriz extracelular — o andaime que sustenta as células — e em vias ligadas ao ácido retinoico, uma molécula derivada da vitamina A conhecida por promover a saúde da barreira intestinal, foram regulados para cima. Outros genes que ajudam a desintoxicar subprodutos nocivos do estresse oxidativo foram ativados, enquanto alguns genes associados a danos induzidos por estresse foram reduzidos. Essas alterações sugerem que os EPS não se limitam a revestir a superfície; eles reprogramam ativamente as células lesionadas para reconstruir sua estrutura e restaurar a função.
Interação com células imunes durante a cura
Como a barreira intestinal não se regenera isoladamente, a equipe investigou como essas mudanças epiteliais poderiam afetar células imunes. Eles coletaram o líquido de culturas epiteliais danificadas pelo 5‑FU e estimuladas com produtos bacterianos e usaram esse meio para diferenciar monócitos humanos em macrófagos. O meio condicionado por células tratadas com EPS direcionou macrófagos para um perfil semelhante ao M1, um estado tipicamente associado a respostas inflamatórias iniciais e limpeza tecidual. Em contraste, o meio de culturas tratadas com o sobrenadante livre de células tendia a favorecer um perfil semelhante ao M2, frequentemente ligado à redução da inflamação e à remodelação tecidual, enquanto as vesículas de membrana produziram um padrão misto. Notavelmente, mesmo quando marcadores de superfície sugeriam uma tendência M1, citocinas inflamatórias clássicas e agressivas como IL‑1β e TNF‑α não aumentaram, sugerindo uma ativação mais equilibrada e focada no reparo, em vez de uma inflamação descontrolada.
O que isso pode significar para o cuidado oncológico futuro
Este trabalho demonstra que moléculas específicas liberadas por uma bactéria probiótica — especialmente seus exopolissacarídeos — podem ajudar células intestinais a se recuperar de lesões induzidas por quimioterapia em laboratório. Os EPS fortaleceram a barreira, ativaram programas internos de reparo e moldaram o comportamento de células imunes de maneiras consistentes com uma cura tecidual orquestrada. Embora o estudo tenha sido feito em culturas celulares e precise de confirmação em animais e em pacientes, ele aponta para um futuro em que produtos bacterianos bem definidos, em vez de micróbios vivos, possam ser usados junto à quimioterapia para reduzir efeitos colaterais dolorosos no intestino e ajudar pacientes a permanecerem nos tratamentos que salvam vidas.
Citação: Lasaviciute, G., López Plana, M., Sundberg Örtegren, S. et al. Limosilactobacillus reuteri metabolites modulate immune pathways and intestinal barrier repair after 5 fluorouracil exposure. Sci Rep 16, 11376 (2026). https://doi.org/10.1038/s41598-026-45524-y
Palavras-chave: mucosite por quimioterapia, reparação da barreira intestinal, metabólitos probióticos, Limosilactobacillus reuteri, exopolissacarídeos