Clear Sky Science · it
I metaboliti di Limosilactobacillus reuteri modulano le vie immunitarie e la riparazione della barriera intestinale dopo l’esposizione al 5‑fluorouracile
Perché è importante proteggere l’intestino durante il trattamento del cancro
La chemioterapia salva vite, ma spesso danneggia il rivestimento della bocca e dell’intestino, provocando dolore, diarrea e infezioni che possono interrompere o indebolire la cura. Questo studio indaga se batteri innocui, o più precisamente le molecole che rilasciano, possano aiutare la parete intestinale a ripararsi dopo il danno causato da un comune farmaco antitumorale. Il lavoro si concentra su un ceppo probiotico ben noto, Limosilactobacillus reuteri DSM 17938, e si chiede: i suoi zuccheri secretati e le sue piccole particelle possono favorire la guarigione senza somministrare batteri vivi a pazienti vulnerabili?
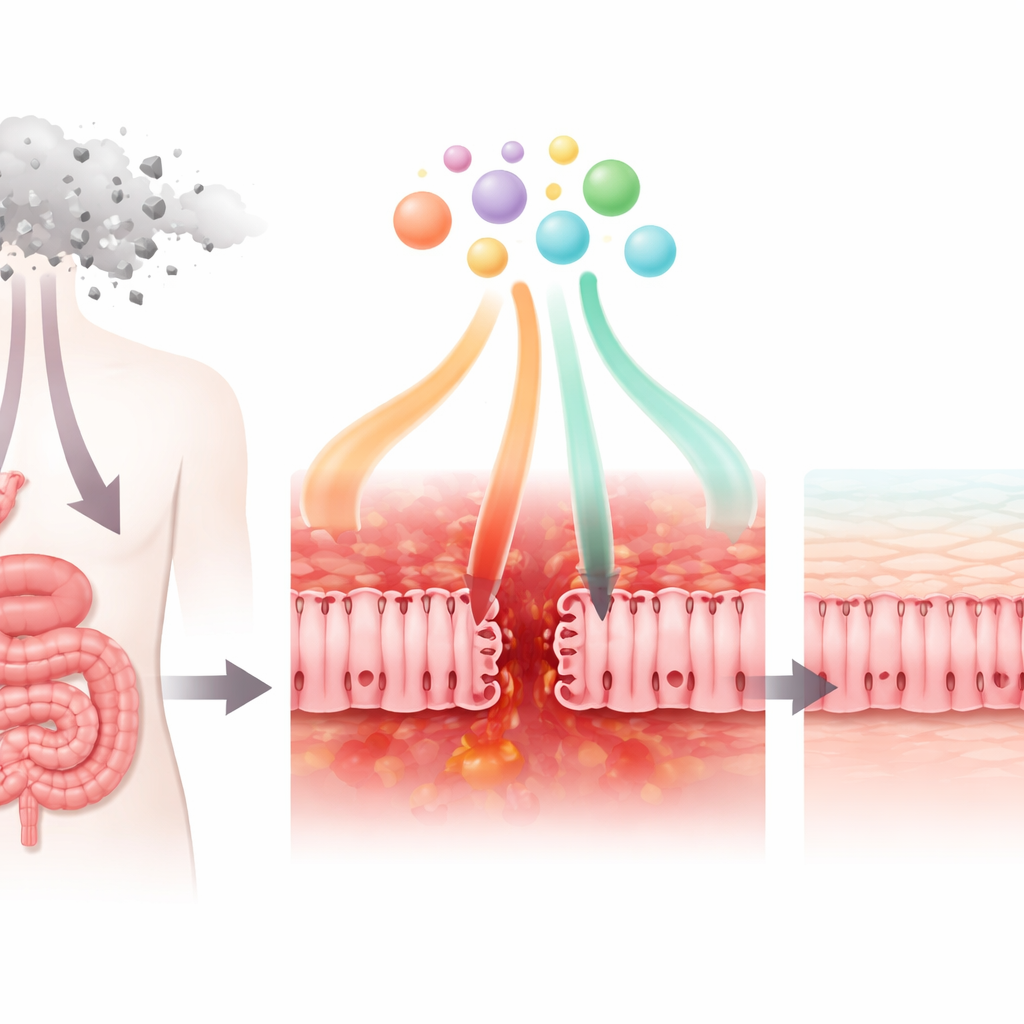
Come un farmaco antitumorale comune danneggia la parete intestinale
I ricercatori hanno prima esaminato come il farmaco chemioterapico 5‑fluorouracile (5‑FU), ampiamente usato contro tumori al seno, allo stomaco e al colon, influisce su cellule che somigliano a quelle del tenue. In colture in vitro, il 5‑FU ha ridotto la sopravvivenza e il normale metabolismo di queste cellule. Ha anche indebolito le “giunzioni strette” che tengono unite le cellule vicine, rendendo lo strato cellulare più permeabile. La microscopia ha mostrato che proteine chiave delle giunzioni hanno perso il consueto arrangiamento ordinato e sono diventate disorganizzate. Contemporaneamente, le cellule hanno cominciato a secernere livelli più alti di segnali infiammatori, come la chemochina CXCL8, mentre producevano meno del fattore regolatorio TGF‑β1. Nel loro insieme, questi cambiamenti rispecchiano ciò che accade nei pazienti quando la barriera intestinale è danneggiata, infiammata e meno capace di tenere fuori i microrganismi.
Zuccheri utili dai batteri amici
Il gruppo ha quindi studiato i prodotti di L. reuteri DSM 17938: un surnatante privo di cellule contenente molte molecole secrete, esopolisaccaridi purificati (EPS, lunghe catene di zuccheri) e piccole vescicole di membrana. Questi sono stati aggiunti solo dopo che il farmaco era stato rimosso, imitando un trattamento di supporto anziché una protezione preventiva. Sia nella linea cellulare intestinale simile al cancro sia in cellule primarie del tenue umano provenienti da un donatore, gli EPS hanno chiaramente migliorato la funzione di barriera. La resistenza elettrica attraverso lo strato cellulare è aumentata e il passaggio di un tracciante fluorescente è diminuito, indicando una sigillatura più efficace. Curiosamente, EPS e gli altri prodotti batterici hanno anche aumentato il rilascio di CXCL8 e di un’altra chemochina, CCL20, soprattutto sul lato rivolto verso la luce intestinale. Dunque, lo stesso trattamento che ha rafforzato la barriera ha anche stimolato segnali tipicamente associati all’infiammazione.
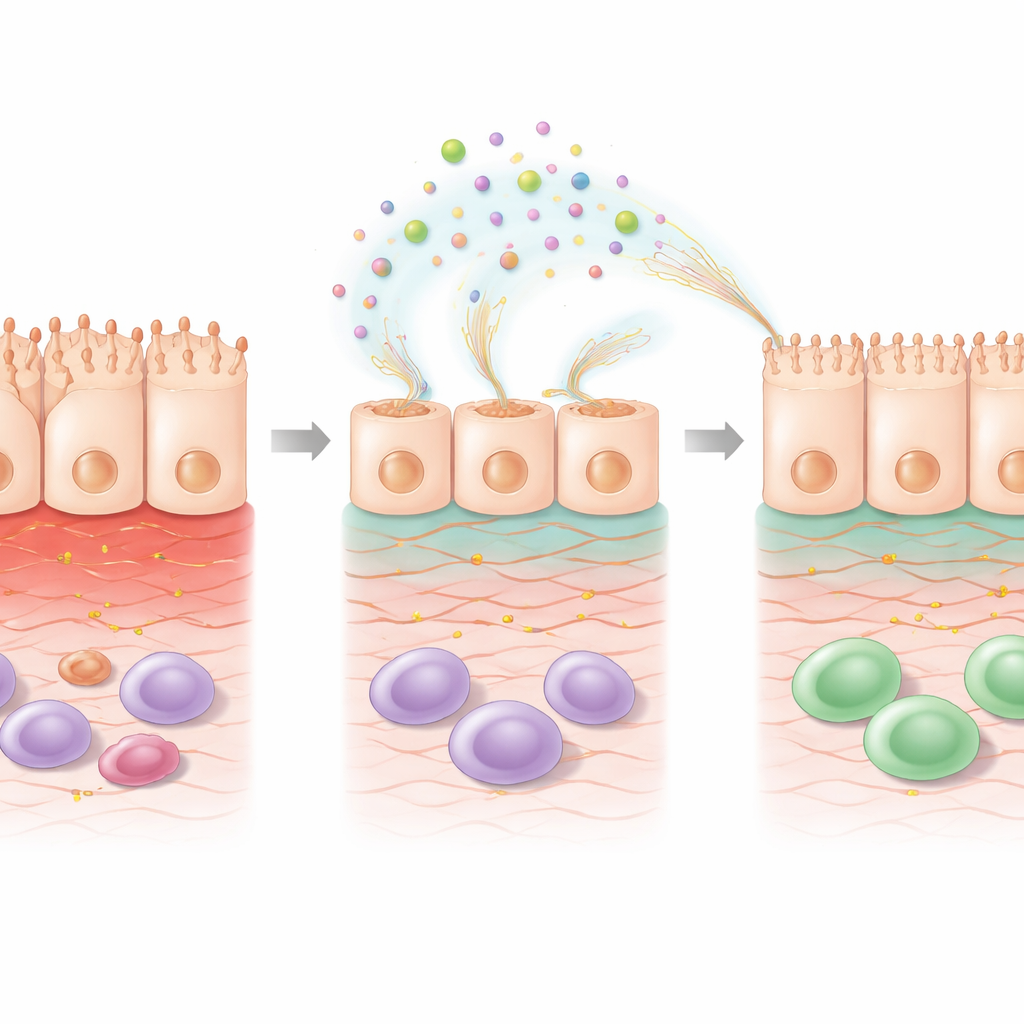
All’interno della cellula: si attivano programmi di riparazione
Per capire cosa cambiava all’interno delle cellule, gli scienziati hanno analizzato l’attività genica globale dopo il trattamento con 5‑FU con o senza EPS. La sola chemioterapia ha alterato molti geni correlati alla sopravvivenza cellulare, alla gestione dello stress e alla segnalazione immunitaria. L’aggiunta di EPS dopo il 5‑FU ha spostato ulteriormente il profilo in una direzione indicativa di riparazione. Sono stati sovraregolati geni coinvolti nell’organizzazione della matrice extracellulare—l’impalcatura che sostiene le cellule—e vie legate all’acido retinoico, una molecola derivata dalla vitamina A nota per promuovere la salute della barriera intestinale. Altri geni che aiutano a detossificare sottoprodotti dannosi dello stress ossidativo sono stati attivati, mentre alcuni geni associati a danni indotti dallo stress sono stati ridotti. Questi cambiamenti suggeriscono che gli EPS non si limitano a rivestire la superficie; riprogrammano attivamente le cellule danneggiate per ricostruire la loro struttura e ripristinare la funzione.
Dialogo con le cellule immunitarie durante la guarigione
Poiché la barriera intestinale non guarisce in isolamento, il gruppo ha valutato come questi cambiamenti epiteliali potessero influenzare le cellule immunitarie. Hanno prelevato il liquido proveniente da colture epiteliali danneggiate dal 5‑FU e stimolate con prodotti batterici e lo hanno usato per differenziare monociti umani in macrofagi. Il mezzo condizionato da cellule trattate con EPS ha spinto i macrofagi verso un profilo simile a M1, uno stato tipicamente collegato a risposte infiammatorie precoci e alla pulizia tissutale. Al contrario, il mezzo da colture trattate con il surnatante privo di cellule tendeva a favorire un profilo simile a M2, spesso associato alla riduzione dell’infiammazione e al rimodellamento tissutale, mentre le vescicole di membrana producevano un quadro misto. È notevole che, anche quando i marcatori di superficie suggerivano una inclinazione M1, le citochine infiammatorie classiche e aggressive come IL‑1β e TNF‑α non erano aumentate, suggerendo un’attivazione più bilanciata e orientata alla riparazione piuttosto che a un’infiammazione incontrollata.
Cosa potrebbe significare per la cura oncologica futura
Questo lavoro mostra che molecole specifiche rilasciate da un batterio probiotico—soprattutto i suoi esopolisaccaridi—possono aiutare le cellule intestinali a recuperare dal danno indotto dalla chemioterapia in laboratorio. Gli EPS hanno rafforzato la barriera, attivato programmi interni di riparazione e modellato il comportamento delle cellule immunitarie in modi coerenti con una guarigione tissutale orchestrata. Sebbene lo studio sia stato condotto in colture cellulari e richieda conferme in modelli animali e nei pazienti, indica un futuro in cui prodotti batterici definiti con cura, piuttosto che microrganismi vivi, potrebbero essere impiegati insieme alla chemioterapia per ridurre gli effetti collaterali intestinali dolorosi e aiutare i pazienti a continuare i trattamenti salvavita.
Citazione: Lasaviciute, G., López Plana, M., Sundberg Örtegren, S. et al. Limosilactobacillus reuteri metabolites modulate immune pathways and intestinal barrier repair after 5 fluorouracil exposure. Sci Rep 16, 11376 (2026). https://doi.org/10.1038/s41598-026-45524-y
Parole chiave: mucosite da chemioterapia, riparazione della barriera intestinale, metaboliti probiotici, Limosilactobacillus reuteri, esopolisaccaridi