Clear Sky Science · es
Los metabolitos de Limosilactobacillus reuteri modulan vías inmunitarias y la reparación de la barrera intestinal tras la exposición a 5 fluorouracilo
Por qué importa proteger el intestino durante el tratamiento del cáncer
La quimioterapia salva vidas, pero con frecuencia daña el revestimiento de la boca y del intestino, provocando dolor, diarrea e infecciones que pueden interrumpir o debilitar el tratamiento. Este estudio explora si bacterias inocuas, o más exactamente las moléculas que liberan, pueden ayudar a la pared intestinal a repararse tras el daño causado por un fármaco anticanceroso común. El trabajo se centra en una cepa probiótica conocida, Limosilactobacillus reuteri DSM 17938, y plantea la pregunta: ¿pueden sus azúcares secretados y sus pequeñas partículas favorecer la curación sin necesidad de administrar bacterias vivas a pacientes vulnerables?
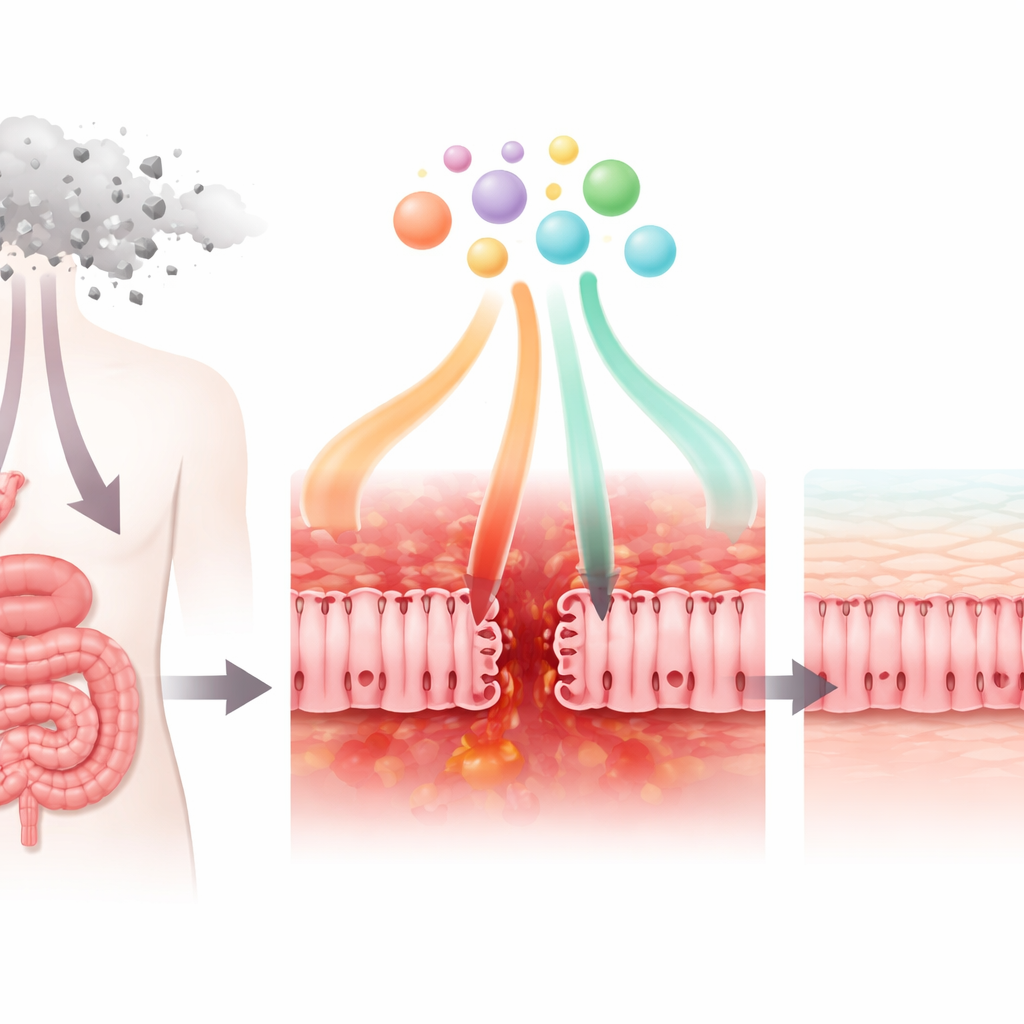
Cómo un fármaco común contra el cáncer daña la pared intestinal
Los investigadores examinaron primero cómo el fármaco de quimioterapia 5-fluorouracilo (5-FU), ampliamente usado contra cánceres de mama, estómago y colon, afecta a células que se parecen a las que recubren el intestino delgado. En placas de laboratorio, el 5-FU redujo la supervivencia de estas células y su metabolismo normal. También debilitó las “uniones estrechas” que mantienen unidas a las células vecinas, haciendo que la capa celular fuera más permeable. La microscopía mostró que proteínas clave de las uniones perdieron su disposición ordenada y se desorganizaron. Al mismo tiempo, las células empezaron a secretar mayores niveles de señales inflamatorias, como la quimiocina CXCL8, mientras producían menos del factor regulador TGF-β1. En conjunto, estos cambios reflejan lo que ocurre en los pacientes cuando la barrera intestinal está dañada, inflamada y menos capaz de impedir la entrada de microbios.
Azúcares beneficiosos de bacterias amigas
El equipo se centró luego en productos fabricados por L. reuteri DSM 17938: un sobrenadante libre de células que contiene muchas moléculas secretadas, exopolisacáridos purificados (EPS, largas cadenas de azúcares) y diminutas vesículas de membrana. Estos se añadieron solo después de lavar el fármaco de quimioterapia, imitando un tratamiento de apoyo en lugar de una protección previa. Tanto en la línea celular tipo intestinal como en células primarias del intestino delgado humano procedentes de un donante, los EPS mejoraron claramente la función de la barrera. La resistencia eléctrica a través de la capa celular aumentó y el paso de un trazador fluorescente disminuyó, lo que indica un sellado más eficaz. Curiosamente, los EPS y otros productos bacterianos también incrementaron la liberación de CXCL8 y de otra quimiocina, CCL20, especialmente en el lado que mira al lumen intestinal. Por tanto, el mismo tratamiento que reforzó la barrera también activó señales típicamente asociadas a inflamación.
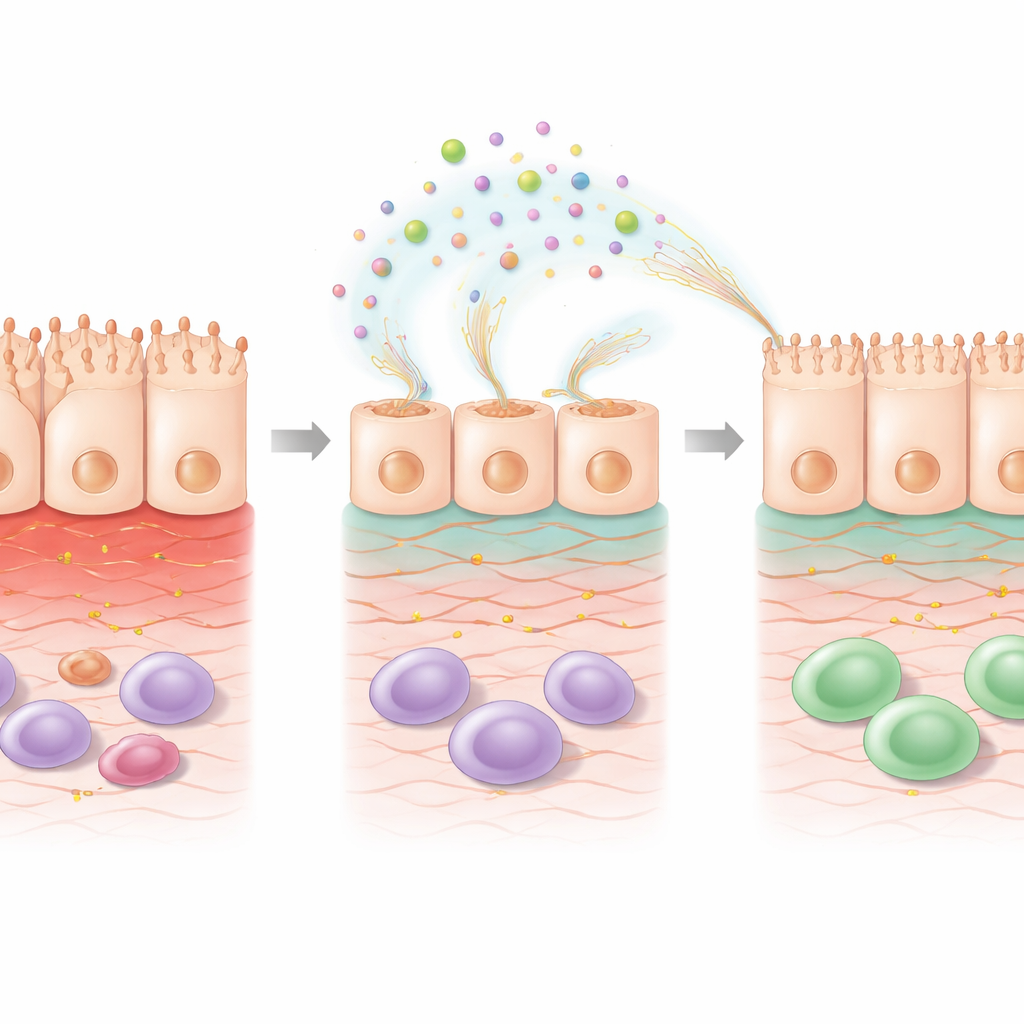
Dentro de la célula: se activan programas de reparación
Para entender qué cambiaba dentro de las células, los científicos analizaron la actividad génica global tras el tratamiento con 5-FU con o sin EPS. La quimioterapia por sí sola alteró muchos genes relacionados con la supervivencia celular, la respuesta al estrés y la señalización inmunitaria. Añadir EPS sobre el 5-FU modificó aún más el patrón, de una manera que apuntaba a la reparación. Se reguló al alza la expresión de genes implicados en la organización de la matriz extracelular—el andamiaje que sostiene a las células—y de vías vinculadas al ácido retinoico, una molécula derivada de la vitamina A conocida por promover la salud de la barrera intestinal. Otros genes que ayudan a desintoxicar subproductos dañinos del estrés oxidativo se activaron, mientras que algunos genes asociados con daño inducido por estrés se redujeron. Estos cambios sugieren que los EPS no se limitan a cubrir la superficie; reprograman activamente las células lesionadas para reconstruir su estructura y restaurar la función.
Comunicación con células inmunitarias durante la curación
Puesto que la barrera intestinal no se repara de manera aislada, el equipo preguntó cómo esos cambios epiteliales podrían afectar a las células inmunitarias. Tomaron el líquido de cultivos epiteliales dañados por 5-FU y estimulados con productos bacterianos y lo usaron para diferenciar monocitos humanos en macrófagos. El medio condicionado procedente de células tratadas con EPS empujó a los macrófagos hacia un perfil tipo M1, un estado típicamente asociado a respuestas inflamatorias tempranas y limpieza tisular. En cambio, el medio de cultivos tratados con el sobrenadante libre de células tendió a favorecer un perfil tipo M2, a menudo vinculado a la moderación de la inflamación y a la remodelación tisular, mientras que las vesículas de membrana produjeron un patrón mixto. Es notable que, aun cuando los marcadores de superficie sugerían una inclinación tipo M1, las citoquinas clásicamente agresivas como IL‑1β y TNF‑α no aumentaron, lo que apunta a una activación más equilibrada y orientada a la reparación en lugar de una inflamación descontrolada.
Qué podría significar esto para la atención oncológica futura
Este trabajo muestra que moléculas específicas liberadas por una bacteria probiótica—especialmente sus exopolisacáridos—pueden ayudar a las células intestinales a recuperarse del daño inducido por quimioterapia en el laboratorio. Los EPS estrecharon la barrera, activaron programas internos de reparación y moldearon el comportamiento de las células inmunitarias de maneras coherentes con una curación tisular coordinada. Aunque el estudio se realizó en cultivos celulares y necesitará confirmación en animales y pacientes, apunta hacia un futuro en el que productos bacterianos cuidadosamente definidos, en lugar de microbios vivos, podrían usarse junto con la quimioterapia para reducir los dolorosos efectos secundarios intestinales y ayudar a los pacientes a continuar con tratamientos que les salvan la vida.
Cita: Lasaviciute, G., López Plana, M., Sundberg Örtegren, S. et al. Limosilactobacillus reuteri metabolites modulate immune pathways and intestinal barrier repair after 5 fluorouracil exposure. Sci Rep 16, 11376 (2026). https://doi.org/10.1038/s41598-026-45524-y
Palabras clave: mucositis por quimioterapia, reparación de la barrera intestinal, metabolitos probióticos, Limosilactobacillus reuteri, exopolisacáridos