Clear Sky Science · sv
Limosilactobacillus reuteri-metaboliter påverkar immunsignaler och tarmbarriärens reparation efter exponering för 5‑fluorouracil
Varför det är viktigt att skydda tarmen under cancerbehandling
Kemoterapi räddar liv, men skadar ofta slemhinnan i mun och tarm och ger smärta, diarré och infektioner som kan avbryta eller försämra behandlingen. Denna studie undersöker om ofarliga bakterier, eller mer precist de molekyler de utsöndrar, kan hjälpa tarmväggen att reparera sig efter skador orsakade av ett vanligt cancerläkemedel. Arbetet fokuserar på en välkänd probiotisk stam, Limosilactobacillus reuteri DSM 17938, och frågar: kan dess utsöndrade sockerarter och små partiklar stödja läkning utan att leva bakterier behöver ges till sårbara patienter?
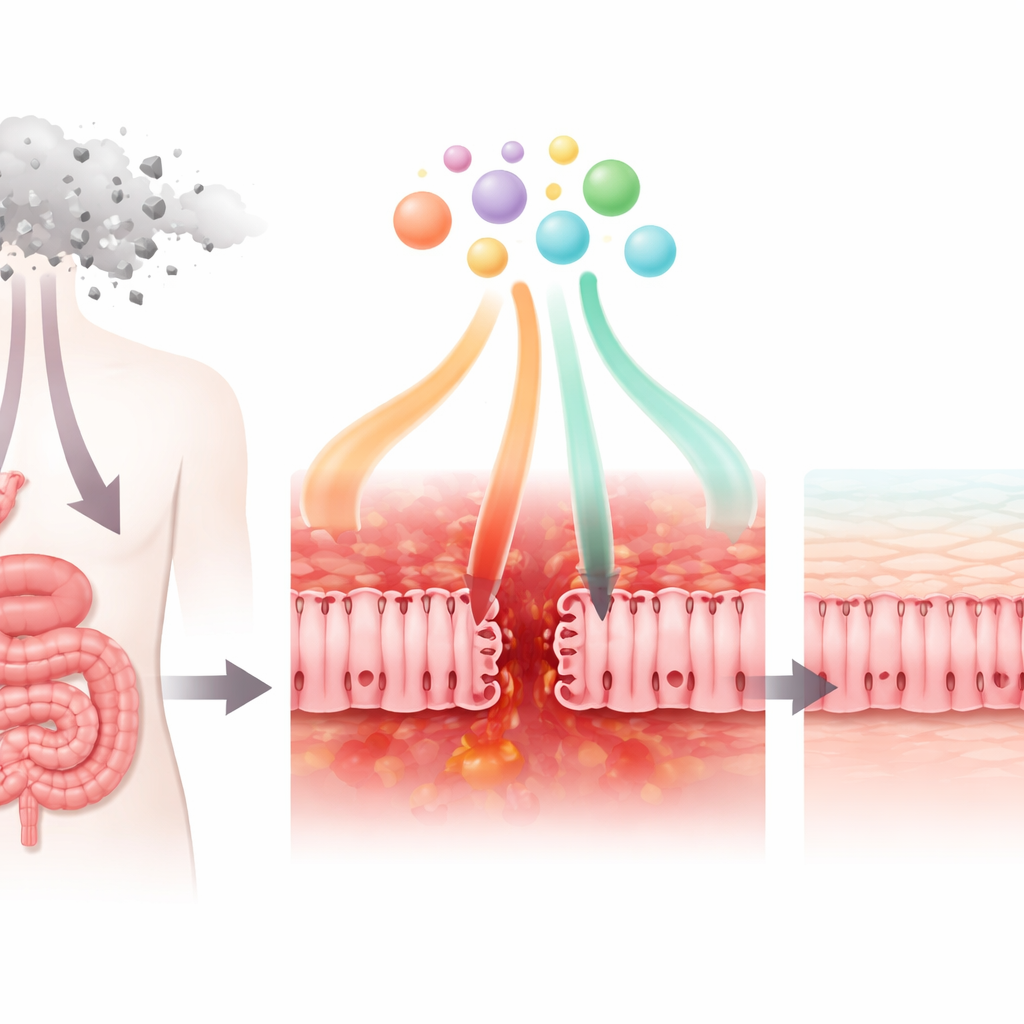
Hur ett vanligt cancerläkemedel skadar tarmväggen
Forskarna undersökte först hur kemoterapiläkemedlet 5‑fluorouracil (5‑FU), som ofta används mot bröst-, mags- och koloncancer, påverkar celler som liknar dem som bekläder tunntarmen. I odlingsskålar minskade 5‑FU cellernas överlevnad och normala ämnesomsättning. Det försvagade också de så kallade ”tight junctions” som håller intilliggande celler samman, vilket gjorde cellskiktet mer läckande. Mikroskopi visade att viktiga junction-proteiner förlorade sin vanliga prydliga, nätliknande ordning och blev oorganiserade. Samtidigt började cellerna utsöndra högre nivåer av inflammatoriska signaler, såsom kemokinen CXCL8, samtidigt som produktionen av den reglerande faktorn TGF‑β1 minskade. Tillsammans speglar dessa förändringar vad som händer hos patienter när tarmbarriären är skadad, inflammerad och mindre förmögen att hålla ute mikrober.
Hjälpsamma sockerarter från vänliga bakterier
Teamet vände sig sedan till produkter från L. reuteri DSM 17938: ett cellfritt supernatant som innehåller många utsöndrade molekyler, renade exopolysackarider (EPS, långa sockerkedjor) och små membranvesiklar. Dessa tillsattes först efter att kemoterapiläkemedlet tvättats bort, för att efterlikna en stödjande behandling snarare än ett skydd som ges i förväg. I både den tarmliknande cancercellinjen och i primära humana tunntarmceller från en donator förbättrade EPS tydligt barriärfunktionen. Det elektriska motståndet över cellskiktet ökade och passage av ett fluorescerande spårämne över barriären minskade, vilket indikerar tätare förslutning. Intressant nog ökade både EPS och de andra bakteriella produkterna även utsöndringen av CXCL8 och en annan kemokin, CCL20, särskilt på sidan mot tarmlumen. Således förstärkte samma behandling som stärkte barriären också signaler som vanligtvis kopplas till inflammation.
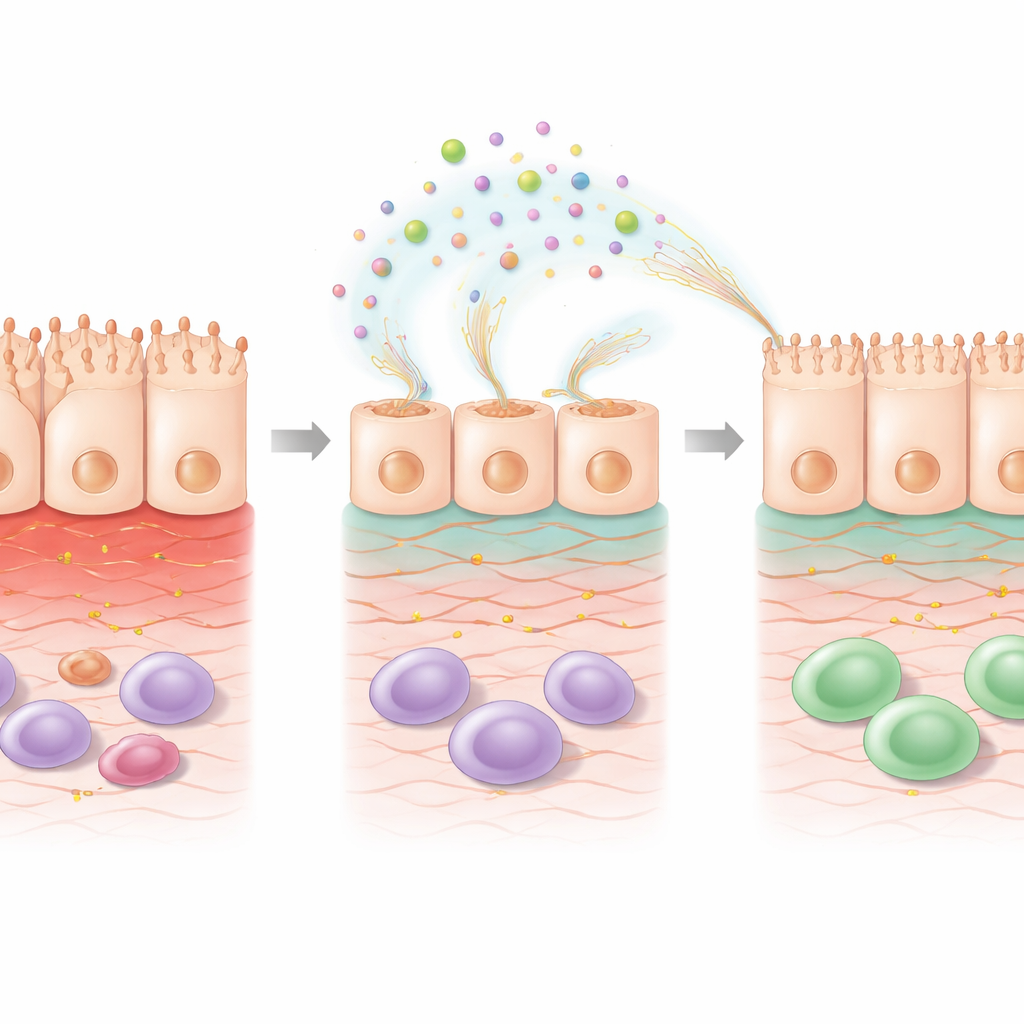
Inuti cellen: reparationsprogram aktiveras
För att förstå vad som förändrades inuti cellerna analyserade forskarna global genaktivitet efter 5‑FU‑behandling med eller utan EPS. Endast kemoterapi förändrade många gener kopplade till cellsurvival, stresshantering och immunsignalering. Att lägga till EPS ovanpå 5‑FU försköt mönstret ytterligare i en riktning som pekade mot reparation. Gener som är involverade i organisering av extracellulär matrix—det stödjande skelettet runt cellerna—och i vägar kopplade till retinoinsyra, en vitamin A‑deriverad molekyl känd för att främja tarmbarriärhälsa, uppreglerades. Andra gener som hjälper till att avgifta skadliga restprodukter från oxidativ stress sattes på, medan vissa gener associerade med stressinducerad skada nedreglerades. Dessa förändringar tyder på att EPS inte bara lägger sig som ett lager på ytan; de omprogrammerar aktivt de skadade cellerna för att återskapa deras struktur och återställa funktion.
Samtal med immunceller under läkningsprocessen
Eftersom tarmbarriären inte läker isolerat frågade teamet hur dessa epiteliala förändringar kan påverka immunceller. De tog vätskan från 5‑FU‑skadade epiteliala kulturer som stimulerats med bakteriella produkter och använde den för att odla humana monocyter till makrofager. Konditionerat medium från EPS‑behandlade celler drev makrofager mot en M1‑lik profil, ett tillstånd vanligen kopplat till tidiga inflammatoriska svar och vävnadsstädning. I kontrast tenderade medium från kulturer behandlade med det cellfria supernatantet att favorisera en M2‑lik profil, ofta associerad med dämpning av inflammation och vävnadsombyggnad, medan membranvesiklar gav ett blandat mönster. Noterbart är att även när ytmärken antydde en M1‑lik lutning, ökade inte klassiska aggressiva inflammatoriska cytokiner som IL‑1β och TNF‑α, vilket antyder en mer balanserad, reparationsinriktad aktivering snarare än ett okontrollerat inflammatoriskt svar.
Vad detta kan innebära för framtida cancervård
Detta arbete visar att specifika molekyler utsläppta av en probiotisk bakterie—särskilt dess exopolysackarider—kan hjälpa tarmceller att återhämta sig från kemoterapirelaterad skada i laboratoriet. EPS tätade barriären, aktiverade interna reparationsprogram och formade immuncellers beteende på sätt som är förenliga med koordinerad vävnadsläkning. Även om studien är gjord i cellkulturer och kräver bekräftelse i djur och patienter, pekar den mot en framtid där noggrant definierade bakteriella produkter, istället för levande mikrober, kan användas tillsammans med kemoterapi för att minska smärtsamma tarmsymtom och hjälpa patienter att fullfölja livräddande behandlingar.
Citering: Lasaviciute, G., López Plana, M., Sundberg Örtegren, S. et al. Limosilactobacillus reuteri metabolites modulate immune pathways and intestinal barrier repair after 5 fluorouracil exposure. Sci Rep 16, 11376 (2026). https://doi.org/10.1038/s41598-026-45524-y
Nyckelord: kemoterapi mukosit, reparation av tarmbarriär, probiotiska metaboliter, Limosilactobacillus reuteri, exopolysackarider