Clear Sky Science · fr
Les métabolites de Limosilactobacillus reuteri modulent les voies immunitaires et la réparation de la barrière intestinale après exposition au 5-fluorouracile
Pourquoi protéger l’intestin pendant le traitement du cancer est important
La chimiothérapie sauve des vies, mais elle attaque souvent la muqueuse de la bouche et de l’intestin, provoquant douleur, diarrhée et infections qui peuvent interrompre ou affaiblir le traitement. Cette étude examine si des bactéries inoffensives, ou plus précisément les molécules qu’elles sécrètent, peuvent aider la paroi intestinale à se réparer après une lésion causée par un médicament anticancéreux courant. Le travail se concentre sur une souche probiotique bien connue, Limosilactobacillus reuteri DSM 17938, et pose la question : ses sucres sécrétés et ses particules microscopiques peuvent-ils soutenir la guérison sans administrer de bactéries vivantes à des patients vulnérables ?
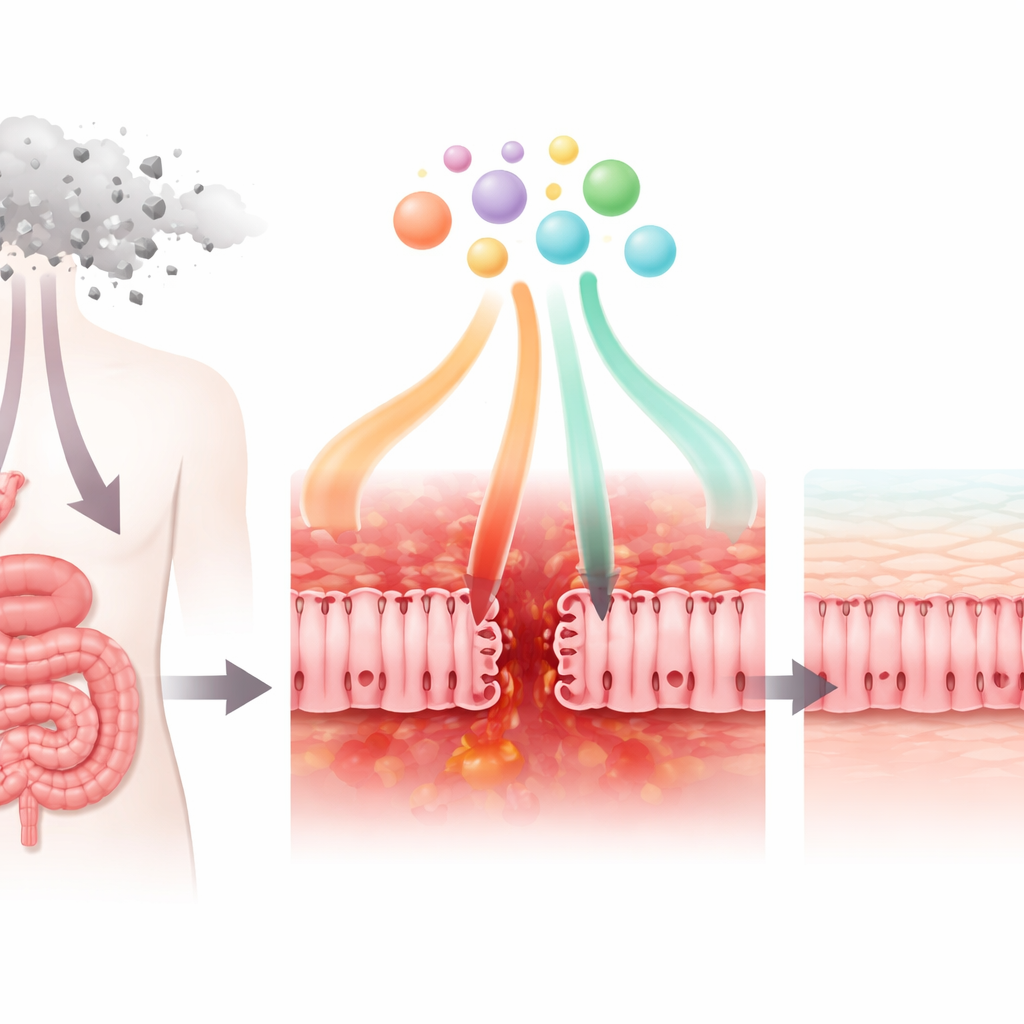
Comment un médicament anticancéreux courant endommage la paroi intestinale
Les chercheurs ont d’abord examiné comment le médicament de chimiothérapie 5‑fluorouracile (5‑FU), largement utilisé contre les cancers du sein, de l’estomac et du côlon, affecte des cellules qui ressemblent à celles qui tapissent l’intestin grêle. En culture, le 5‑FU a réduit la survie de ces cellules et leur métabolisme normal. Il a aussi affaibli les « jonctions serrées » qui maintiennent les cellules voisines ensemble, rendant la couche cellulaire plus perméable. La microscopie a révélé que des protéines clés des jonctions perdaient leur arrangement habituel en réseau et devenaient désorganisées. Parallèlement, les cellules ont commencé à sécréter des niveaux accrus de signaux inflammatoires, tels que la chimiokine CXCL8, tout en produisant moins du facteur régulateur TGF‑β1. Ensemble, ces changements reflètent ce qui se passe chez les patients lorsque la barrière intestinale est endommagée, enflammée et moins capable d’empêcher l’entrée des microbes.
Des sucres utiles produits par des bactéries amies
L’équipe s’est ensuite intéressée aux produits fabriqués par L. reuteri DSM 17938 : un surnageant cellulaire débarrassé de cellules, contenant de nombreuses molécules sécrétées, des exopolysaccharides purifiés (EPS, longues chaînes de sucres) et de petites vésicules membranaires. Ceux‑ci ont été ajoutés seulement après l’élimination du médicament de chimiothérapie, mimant un traitement de soutien plutôt qu’une protection préventive. Tant sur la lignée cellulaire d’origine intestinale que sur des cellules primaires humaines de l’intestin grêle issues d’un donneur, les EPS ont nettement amélioré la fonction de barrière. La résistance électrique au travers de la couche cellulaire a augmenté et le passage d’un traceur fluorescent à travers la barrière a diminué, indiquant une meilleure étanchéité. Fait intéressant, les EPS et les autres produits bactériens ont également amplifié la libération de CXCL8 et d’une autre chimiokine, CCL20, surtout du côté faisant face à la lumière intestinale. Ainsi, le même traitement qui renforçait la barrière a aussi suscité des signaux généralement associés à l’inflammation.
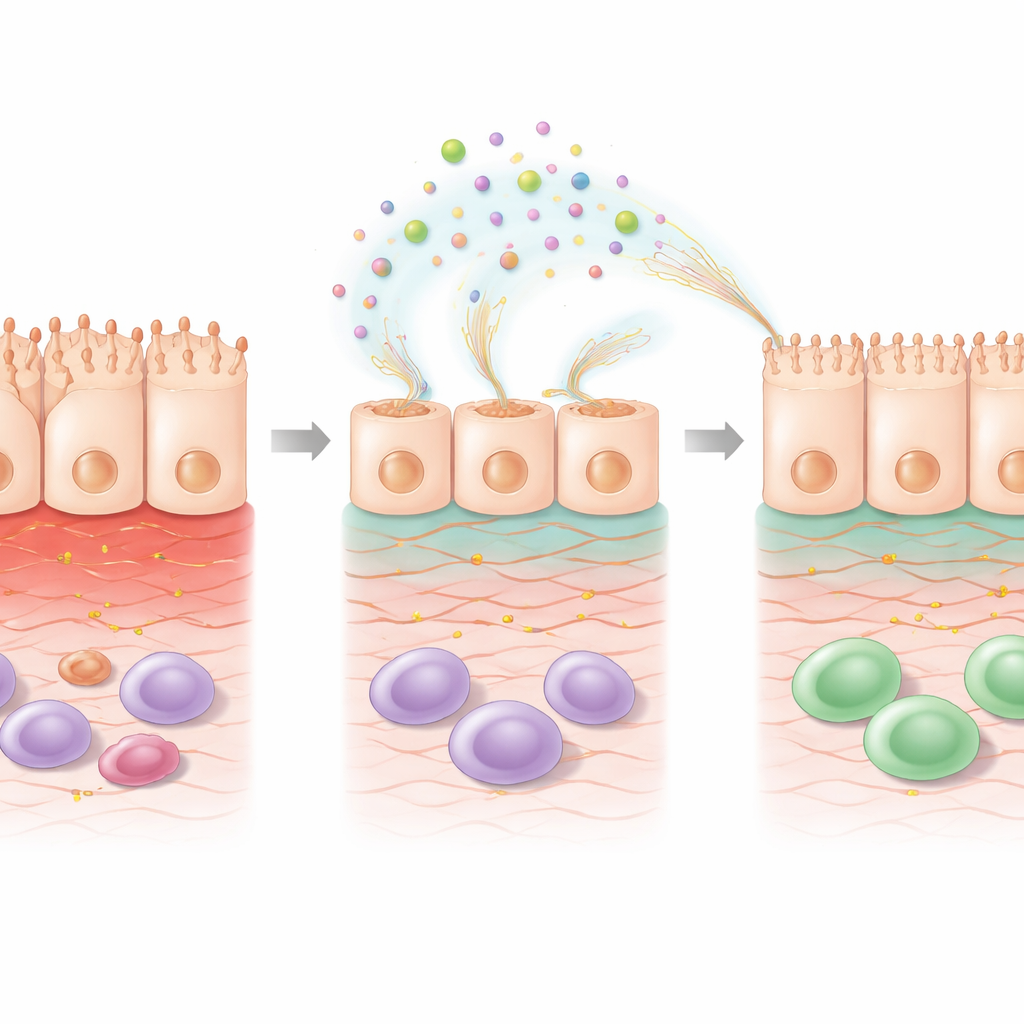
À l’intérieur de la cellule : des programmes de réparation activés
Pour comprendre ce qui changeait à l’intérieur des cellules, les scientifiques ont analysé l’activité génique globale après un traitement au 5‑FU avec ou sans EPS. La chimiothérapie seule modifiait de nombreux gènes liés à la survie cellulaire, à la gestion du stress et aux signaux immunitaires. L’ajout d’EPS après le 5‑FU a encore modulé ce profil, d’une manière orientée vers la réparation. Des gènes impliqués dans l’organisation de la matrice extracellulaire — l’armature qui soutient les cellules — et des voies liées à l’acide rétinoïque, une molécule dérivée de la vitamine A connue pour favoriser la santé de la barrière intestinale, étaient surexprimés. D’autres gènes participant à la détoxification des sous‑produits nocifs du stress oxydatif étaient activés, tandis que certains gènes associés aux dommages induits par le stress étaient diminués. Ces changements suggèrent que les EPS ne se contentent pas d’enrober la surface : ils reprogramment activement les cellules blessées pour reconstruire leur structure et restaurer leur fonction.
Dialogue avec les cellules immunitaires pendant la guérison
Parce que la réparation de la barrière intestinale ne se fait pas isolément, l’équipe a étudié comment ces changements épithéliaux pouvaient influencer les cellules immunitaires. Ils ont prélevé le liquide provenant de cultures épithéliales endommagées par le 5‑FU et stimulées par les produits bactériens, puis l’ont utilisé pour faire maturer des monocytes humains en macrophages. Le milieu conditionné par des cellules traitées aux EPS a poussé les macrophages vers un profil de type M1, un état généralement associé aux réponses inflammatoires précoces et au nettoyage tissulaire. En revanche, le milieu issu des cultures traitées par le surnageant cellulaire favorisait plutôt un profil de type M2, souvent lié à l’apaisement de l’inflammation et au remodelage tissulaire, tandis que les vésicules membranaires produisaient un schéma mixte. Il est notable que, même lorsque les marqueurs de surface suggéraient une inclinaison de type M1, des cytokines inflammatoires classiques et agressives telles que IL‑1β et TNF‑α n’étaient pas augmentées, ce qui laisse penser à une activation plus équilibrée, axée sur la réparation plutôt qu’à une inflammation incontrôlée.
Ce que cela pourrait signifier pour les soins du cancer à venir
Ce travail montre que des molécules spécifiques libérées par une bactérie probiotique — en particulier ses exopolysaccharides — peuvent aider les cellules intestinales à récupérer d’une lésion induite par la chimiothérapie en culture. Les EPS ont resserré la barrière, activé des programmes internes de réparation et modulé le comportement des cellules immunitaires de façon cohérente avec une guérison tissulaire orchestrée. Bien que l’étude ait été réalisée sur des cultures cellulaires et doive être confirmée chez l’animal et chez l’humain, elle ouvre la voie à un avenir où des produits bactériens définis avec précision, plutôt que des microbes vivants, pourraient être utilisés en complément de la chimiothérapie pour réduire les effets indésirables douloureux sur l’intestin et aider les patients à poursuivre des traitements salvateurs.
Citation: Lasaviciute, G., López Plana, M., Sundberg Örtegren, S. et al. Limosilactobacillus reuteri metabolites modulate immune pathways and intestinal barrier repair after 5 fluorouracil exposure. Sci Rep 16, 11376 (2026). https://doi.org/10.1038/s41598-026-45524-y
Mots-clés: mucosite liée à la chimiothérapie, réparation de la barrière intestinale, métabolites probiotiques, Limosilactobacillus reuteri, exopolysaccharides