Clear Sky Science · zh
癌症进展中的间质向上皮转化(MET):来自逻辑建模的见解
为何癌细胞形态变化至关重要
癌细胞不仅仅是分裂繁殖;它们还通过改变形态和行为在体内扩散。为了从肿瘤脱离,它们会放松与邻近细胞的连接,变得更具迁移性;而要在他处形成新肿瘤,常常需要重新获得原有的紧密相连形态。这种往返变换,被称为细胞可塑性,是转移的核心。这里总结的研究使用基于计算的逻辑模型来理解癌细胞如何从移动状态逆转回更稳定的状态,以及为何这种逆转高度依赖周围环境条件。
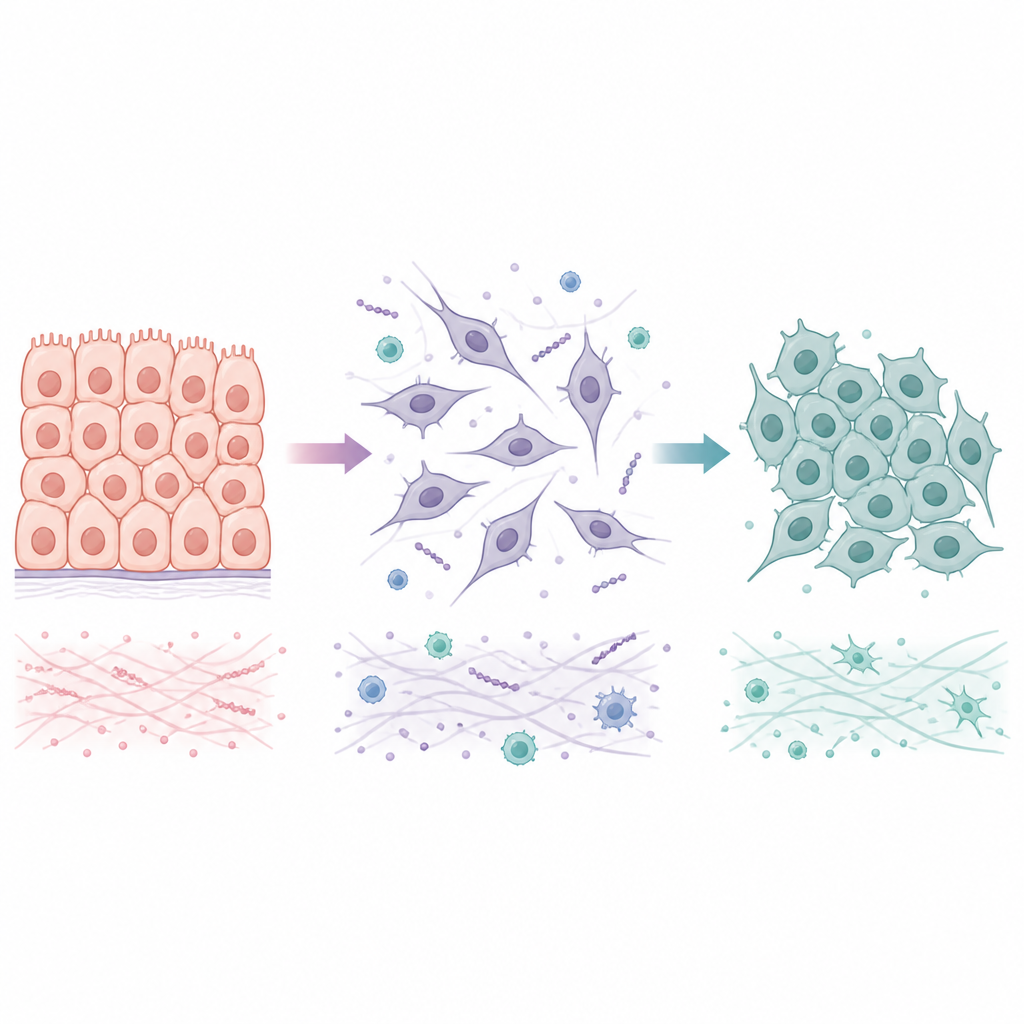
细胞在定居与迁移状态之间迁移的两种方式
许多肿瘤起始于上皮细胞,上皮细胞以有序的片层紧密相连。在被称为上皮向间质转化的过程中,这些细胞失去紧密连接、改变形状并获得迁移和入侵周围组织与血管的能力。当它们到达新的器官时,常发生相反的转变——间质向上皮转化,帮助它们形成稳定的群落。与其在两个端点之间简单翻转,癌细胞常处于混合状态,兼具定居与迁移特征。这些中间状态似乎尤其善于抵抗压力并播撒转移种子,因此理解不仅是首次转化如何发生,还要明白何时以及如何能够逆转,同样重要。
影响癌细胞身份的推拉信号
来自肿瘤微环境的外部信号强烈影响细胞更像上皮还是间质细胞。研究充分的驱动因子如TGFβ和各种生长因子倾向于鼓励迁移和侵袭特性,而包括BMP在内的蛋白家族等其他信号则可能有利于向上皮状态的回归。细胞内部,基因和小RNA网络互相强化某一身份。某些转录因子促进细胞连接的解体和基质的重塑,另一类因子则致力于恢复紧密接触和上皮特征。实验证据表明不存在单一、通用的路径;结果取决于哪些信号存在、持续时间以及细胞类型。
构建细胞决策的逻辑图谱
由于涉及的分子和反馈回路众多,很难直接预测特定环境下癌细胞的反应。作者汇集了关于与两种转化方向相关的关键通路的已发表信息,并将其组织成调控网络。随后他们把该网络转化为布尔(开/关)逻辑模型并进行了大量计算机模拟。这种方法并不试图测量精确的分子量,而是探索哪些信号和内部调节因子的组合会导致稳定的基因活动模式。模型产生了25种长期稳态,这些稳态自然分为上皮、间质、混合和原始(naive)类别,反映了实验室研究中观察到的谱系。
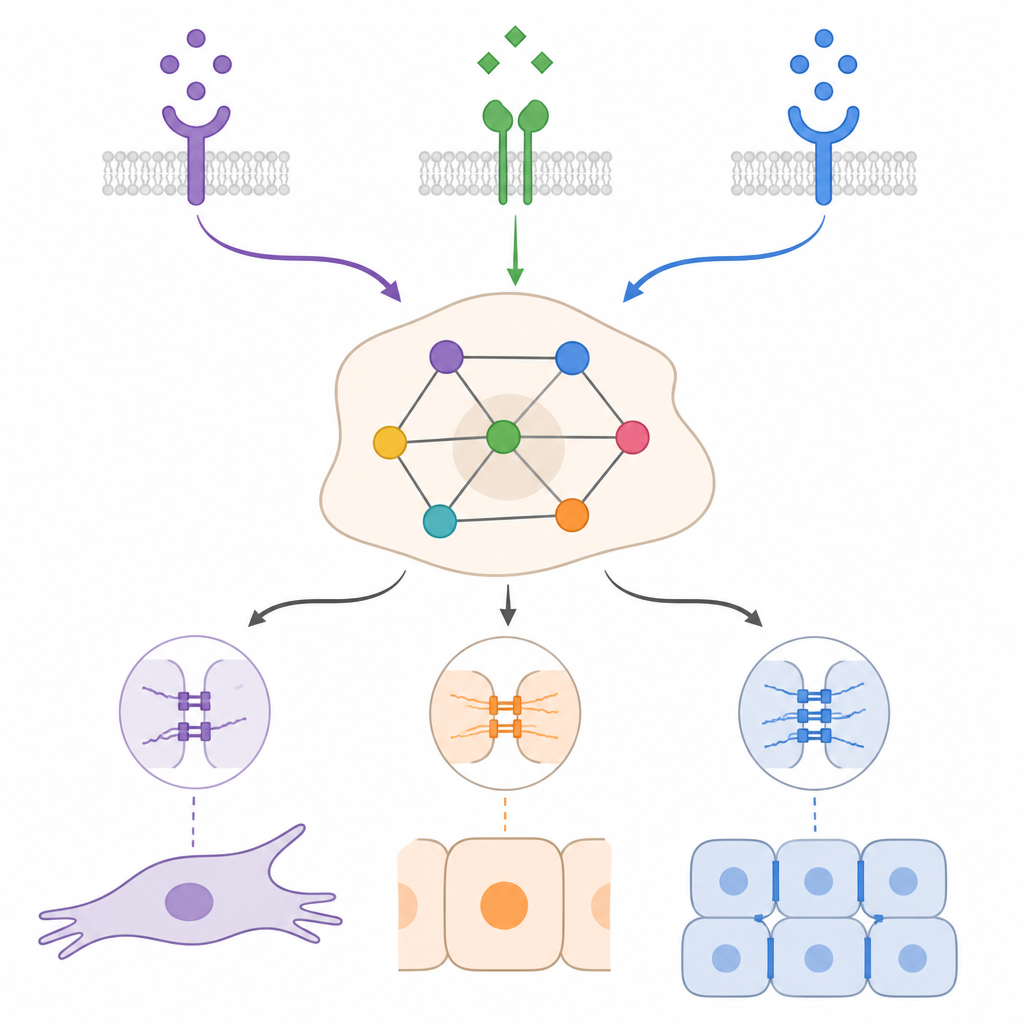
情境决定细胞能回退到何种程度
通过在不同TGFβ、BMP和生长因子组合下模拟类上皮和类间质的起始条件,模型显示相同的外部线索在不同情境下可以产生截然不同的效果。在许多情况下,BMP能够削弱由TGFβ驱动的间质程序并将细胞推向更上皮或混合的状态,但往往无法完全恢复为上皮。模拟还突出了自我维持反馈环路的重要性,即癌细胞自身产生TGFβ或生长因子信号。这些回路可以在外部刺激消失后维持间质状态。模型预测,通过破坏这些回路的特定部分或增强某些促上皮调节因子,细胞可被转向混合或上皮状态,但确切结果仍取决于信号组合和起始条件。
这对理解转移意味着什么
总体而言,该研究表明癌症中的间质向上皮转化并非由单一主开关决定,而是由相互重叠的信号网络控制,其影响高度依赖情境。有些分子似乎仅在狭窄条件下才能促使细胞回归上皮样状态,而其他分子作用更广泛,但常常仍使细胞停留在保留侵袭特征的混合状态。对非专业读者来说,主要信息是:转移依赖于可塑的细胞身份,任何试图强制细胞回到更安全、迁移性更低的形态的策略,都必须考虑稳定这些危险中间状态的众多反馈回路和环境线索。
引用: Orozco-Ruiz, S., Ruscone, M., Barillot, E. et al. Mesenchymal to epithelial transition (MET) in cancer progression: insights from logical modeling. Sci Rep 16, 15032 (2026). https://doi.org/10.1038/s41598-026-44905-7
关键词: 上皮-间质转化, 癌症转移, 细胞可塑性, 逻辑建模, 骨形态发生蛋白