Clear Sky Science · es
Transición mesenquimal a epitelial (MET) en la progresión del cáncer: ideas desde el modelado lógico
Por qué importa que las células cancerosas cambien de forma
Las células cancerosas no solo se dividen; también cambian su forma y comportamiento para diseminarse por el organismo. Para escapar de un tumor, aflojan sus vínculos con las células vecinas y se vuelven más móviles. Para formar nuevos tumores en otro lugar, a menudo deben recuperar su forma original, más fuertemente conectada. Este ir y venir, conocido como plasticidad celular, está en el núcleo de la metástasis. El estudio resumido aquí utiliza modelos lógicos por ordenador para comprender cómo las células cancerosas regresan de un estado móvil a uno más asentado, y por qué esa reversión depende tanto del entorno circundante.
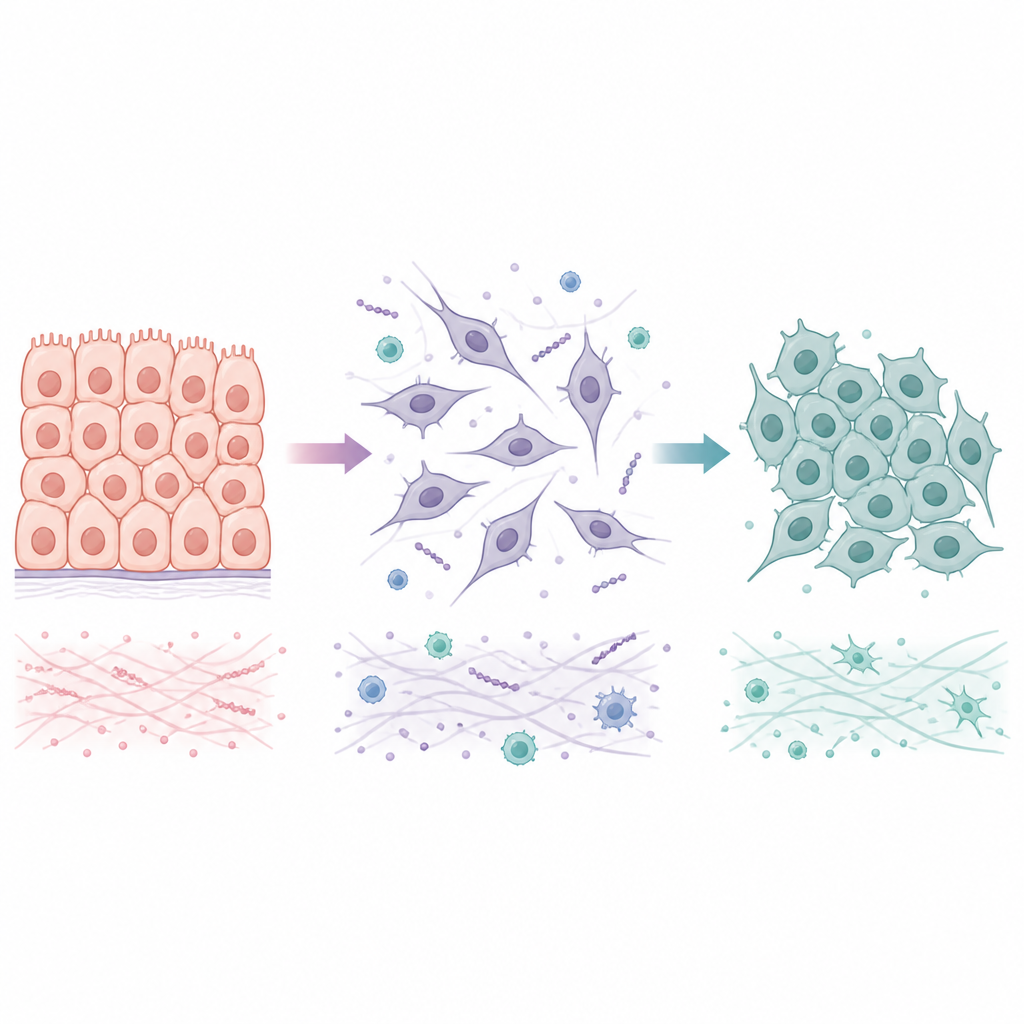
Dos maneras en que las células transitan entre estados asentados y móviles
Muchos tumores se inician como células epiteliales, que están fuertemente unidas en láminas ordenadas. Durante un proceso llamado transición epitelial a mesenquimal, estas células pierden sus uniones estrechas, cambian de forma y adquieren la capacidad de moverse e invadir tejidos y vasos sanguíneos vecinos. Cuando llegan a un nuevo órgano, con frecuencia experimentan el cambio inverso, la transición mesenquimal a epitelial, que les ayuda a formar colonias estables. En lugar de alternar solo entre dos extremos, las células cancerosas a menudo ocupan estados híbridos que combinan rasgos asentados y móviles. Estos estados intermedios parecen especialmente aptos para sobrevivir al estrés y sembrar metástasis, por lo que es importante entender no solo cómo ocurre la primera transición, sino también cómo y cuándo puede revertirse.
Señales que empujan o tiran de la identidad celular cancerosa
Las señales externas del microentorno tumoral influyen fuertemente en si una célula se comporta más como una epitelial o una mesenquimal. Impulsores bien estudiados, como TGFβ y diversos factores de crecimiento, tienden a favorecer el lado móvil e invasivo, mientras que otras señales, incluida una familia de proteínas llamada BMP, pueden promover el regreso hacia un estado epitelial. Dentro de la célula, redes de genes y pequeños ARN refuerzan una u otra identidad. Ciertos factores de transcripción promueven la degradación de las uniones celulares y la remodelación de la matriz circundante, mientras que otro grupo de factores trabaja para restaurar los contactos estrechos y el carácter epitelial. La evidencia experimental muestra que no existe una única ruta universal a través de estos programas; en cambio, el resultado depende de qué señales estén presentes, durante cuánto tiempo y en qué tipo de célula.
Construir un mapa lógico de decisiones celulares
Dado que intervienen tantos moléculas y bucles de retroalimentación, es difícil predecir cómo responderá una célula cancerosa en un contexto particular. Los autores reunieron información publicada sobre las vías clave vinculadas a ambas direcciones de la transición y la organizaron en una red reguladora. Luego tradujeron esta red a un modelo lógico booleano, de encendido‑apagado, y ejecutaron muchas simulaciones por ordenador. Este enfoque no intenta medir cantidades exactas de moléculas; en su lugar, explora qué combinaciones de señales y reguladores internos conducen a patrones estables de actividad génica. El modelo produjo 25 estados a largo plazo que se agruparon naturalmente en categorías epitelial, mesenquimal, híbrida y naïve, reflejando el espectro observado en estudios de laboratorio.
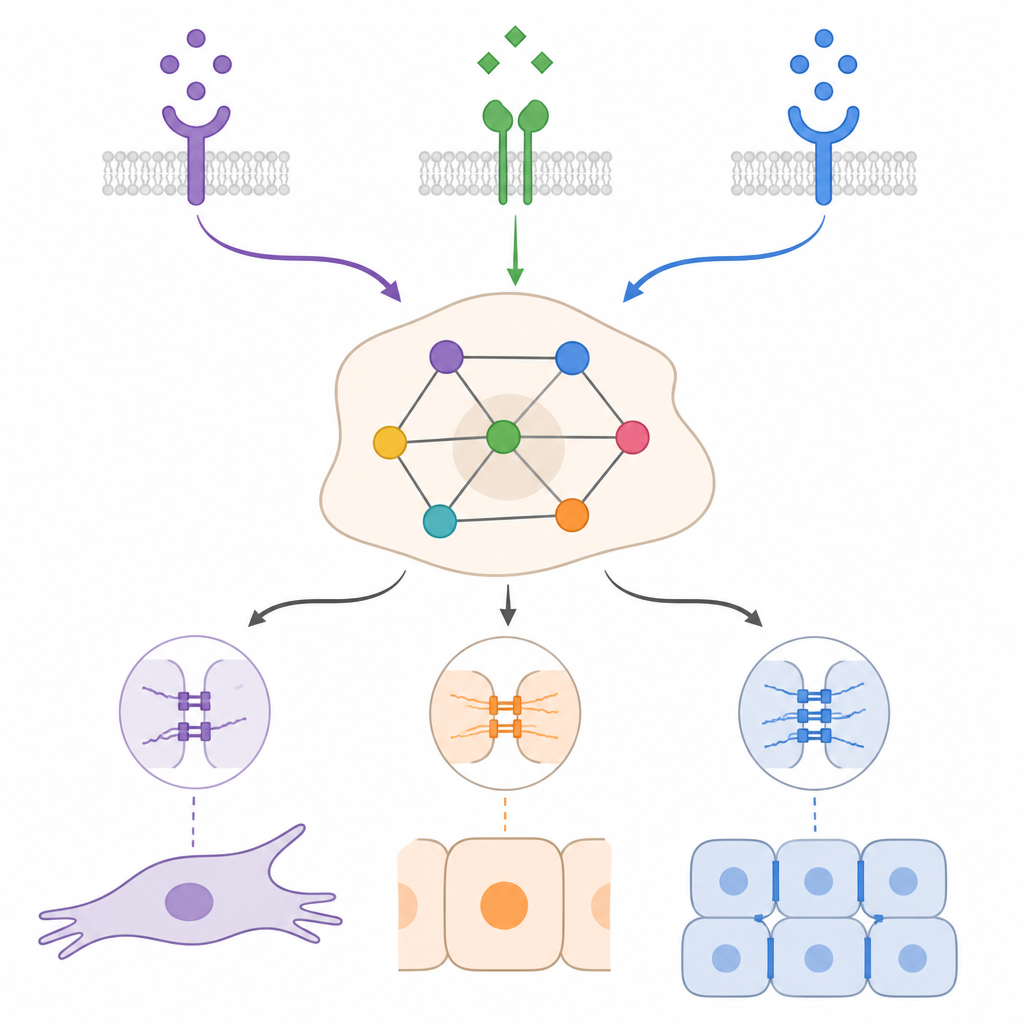
El contexto determina hasta qué punto las células pueden revertir
Al simular condiciones iniciales de tipo epitelial y mesenquimal bajo distintas combinaciones de TGFβ, BMP y factores de crecimiento, el modelo mostró que la misma señal externa puede tener efectos muy distintos según el contexto. En muchos casos, BMP fue capaz de debilitar un programa mesenquimal impulsado por TGFβ y empujar a las células hacia estados más epiteliales o híbridos, pero a menudo no alcanzó una vuelta completa. Las simulaciones también resaltaron la importancia de los bucles de retroalimentación autosostenidos, en los que las propias células cancerosas producen TGFβ o factores de crecimiento. Estos bucles pueden mantener un estado mesenquimal incluso después de que la estimulación externa desaparezca. Romper partes específicas de estos bucles, o potenciar ciertos reguladores pro‑epiteliales, se predijo que desplazaría a las células hacia estados híbridos o epiteliales, pero el resultado exacto dependía nuevamente de la combinación de señales y de las condiciones iniciales.
Qué significa esto para entender la metástasis
En conjunto, el trabajo sugiere que la transición mesenquimal a epitelial en el cáncer no está gobernada por un interruptor maestro único, sino por redes superpuestas de señales cuyo impacto es altamente dependiente del contexto. Algunas moléculas parecen capaces de empujar a las células de vuelta hacia un estado similar al epitelial solo en circunstancias estrechas, mientras que otras actúan de forma más amplia pero a menudo aún dejan a las células en estados híbridos que conservan rasgos invasivos. Para el público general, el mensaje principal es que la metástasis depende de identidades celulares flexibles, y que los intentos de forzar a las células de regreso a una forma más segura y menos móvil tendrán que tener en cuenta los numerosos bucles de retroalimentación y las señales ambientales que estabilizan estas condiciones intermedias peligrosas.
Cita: Orozco-Ruiz, S., Ruscone, M., Barillot, E. et al. Mesenchymal to epithelial transition (MET) in cancer progression: insights from logical modeling. Sci Rep 16, 15032 (2026). https://doi.org/10.1038/s41598-026-44905-7
Palabras clave: transición epitelial mesenquimal, metástasis del cáncer, plasticidad celular, modelado lógico, proteína morfogenética ósea