Clear Sky Science · pl
Przejście mezenchymalno‑nabłonkowe (MET) w progresji nowotworu: wnioski z modelowania logicznego
Dlaczego zmiana kształtu komórek nowotworowych ma znaczenie
Komórki nowotworowe nie tylko się dzielą; zmieniają też kształt i zachowanie, by rozprzestrzeniać się po organizmie. Aby uciec z guza, poluzowują więzi z sąsiednimi komórkami i stają się bardziej ruchome. Aby utworzyć nowe guzy w innych miejscach, często muszą odzyskać pierwotną, silnie połączoną postać. Ta zmienność w obie strony, nazywana plastycznością komórkową, jest sednem przerzutów. Streszczone tutaj badanie wykorzystuje komputerowe modele logiczne, by zrozumieć, jak komórki nowotworowe przełączają się z powrotem z postaci mobilnej do bardziej osiadłej i dlaczego to odwrócenie jest tak zależne od warunków otoczenia.
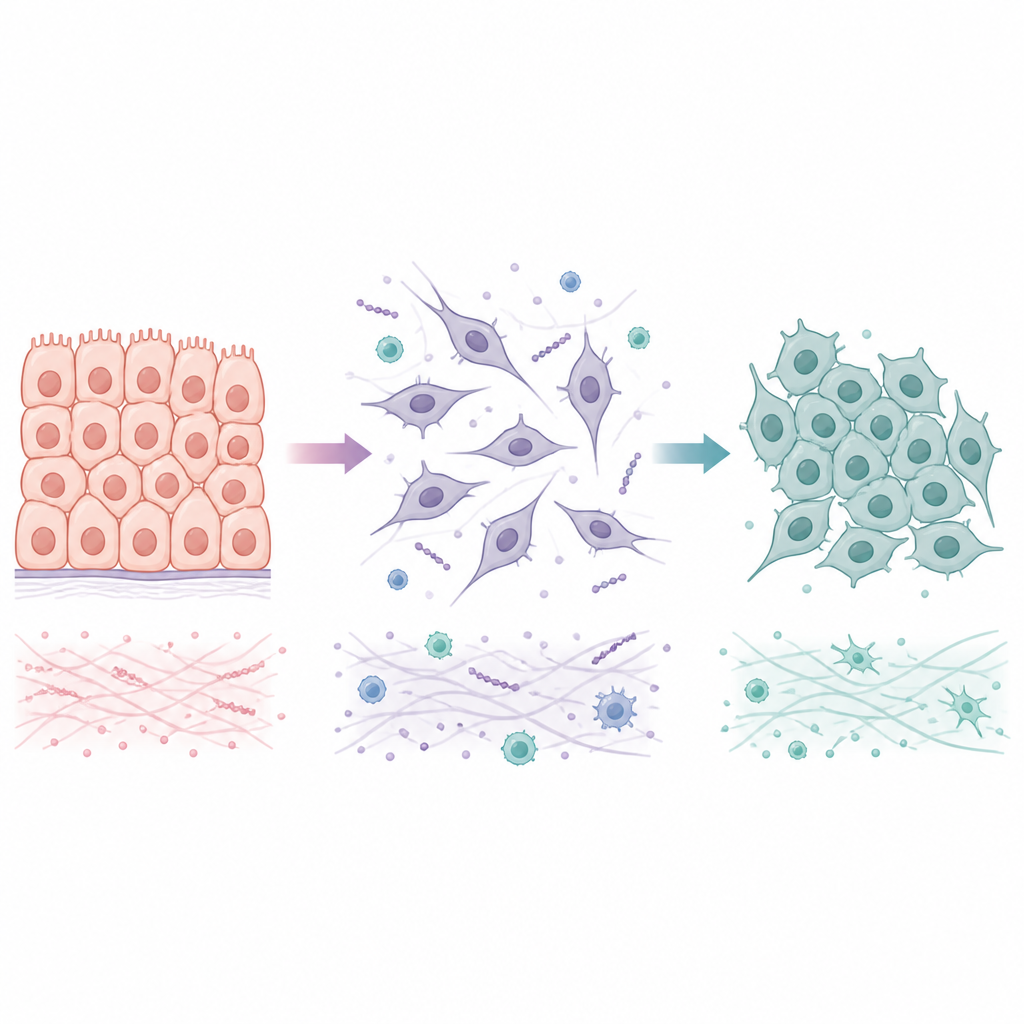
Dwa sposoby, w jakie komórki przemieszczają się między stanami osiadłymi a ruchliwymi
Wiele guzów zaczyna się jako komórki nabłonkowe, ściśle połączone w uporządkowane warstwy. W procesie zwanym przejściem nabłonkowo‑mezenchymalnym te komórki tracą połączenia ścisłe, zmieniają kształt i zyskują zdolność do ruchu oraz inwazji okolicznych tkanek i naczyń krwionośnych. Kiedy docierają do nowego organu, często zachodzi odwrotna zmiana — przejście mezenchymalno‑nabłonkowe — co pomaga im tworzyć stabilne kolonie. Zamiast przełączać się tylko między dwoma skrajnymi stanami, komórki nowotworowe często zajmują stany hybrydowe łączące cechy osiadłe i ruchliwe. Stany pośrednie wydają się szczególnie odporne na stres i zdolne do zainicjowania przerzutów, dlatego ważne jest zrozumienie nie tylko tego, jak zachodzi pierwsze przejście, ale też jak i kiedy może ono zostać odwrócone.
Sygnały, które przyciągają lub odciągają tożsamość komórki nowotworowej
Sygnały z otoczenia guza silnie wpływają na to, czy komórka zachowuje się bardziej jak nabłonkowa, czy mezenchymalna. Dobrze poznane czynniki, takie jak TGFβ i różne czynniki wzrostu, zwykle sprzyjają stronie ruchliwej i inwazyjnej, podczas gdy inne sygnały, w tym rodzina białek BMP, mogą faworyzować powrót ku stanowi nabłonkowemu. Wewnątrz komórki sieci genów i małych RNA wzmacniają jedną lub drugą tożsamość. Niektóre czynniki transkrypcyjne promują rozpad połączeń komórkowych i przebudowę macierzy zewnątrzkomórkowej, podczas gdy inna grupa czynników dąży do przywrócenia ścisłych kontaktów i cech nabłonkowych. Dane eksperymentalne pokazują, że nie istnieje jedna uniwersalna ścieżka przez te programy; wynik zależy od obecnych sygnałów, czasu ich trwania i typu komórki.
Budowanie logicznej mapy decyzji komórkowych
Ponieważ zaangażowanych jest tak wiele cząsteczek i pętli sprzężeń zwrotnych, trudno przewidzieć, jak komórka nowotworowa zareaguje w danym kontekście. Autorzy zebrali opublikowane informacje o kluczowych ścieżkach powiązanych z oboma kierunkami przejścia i uporządkowali je w sieć regulacyjną. Następnie przetłumaczyli tę sieć na model Boolowski, czyli logiczny model włącz/wyłącz, i wykonali liczne symulacje komputerowe. Podejście to nie próbuje mierzyć dokładnych ilości cząsteczek; zamiast tego bada, które kombinacje sygnałów i wewnętrznych regulatorów prowadzą do stabilnych wzorców aktywności genów. Model wygenerował 25 długotrwałych stanów, które naturalnie pogrupowały się w kategorie nabłonkowe, mezenchymalne, hybrydowe i naiwne, odzwierciedlając spektrum obserwowane w badaniach laboratoryjnych.
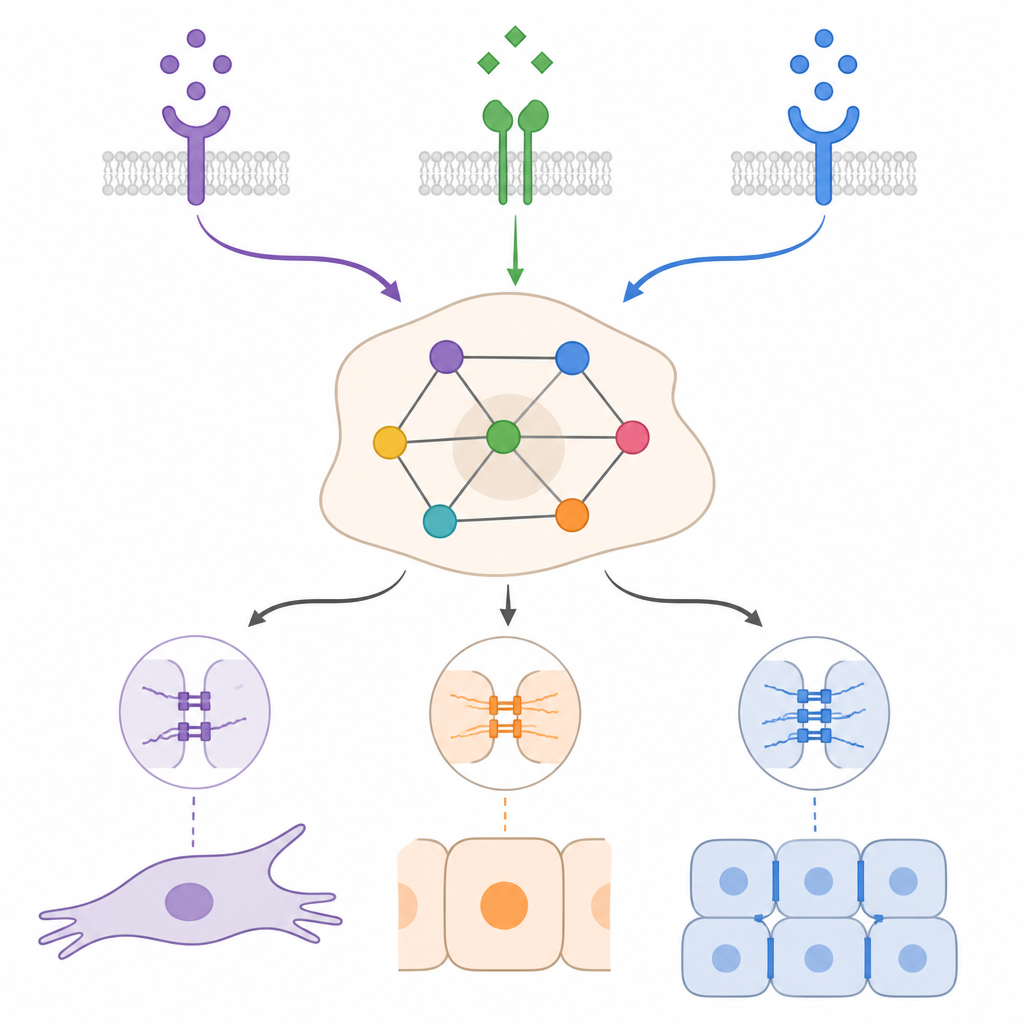
Kontekst warunkuje, jak daleko komórki mogą się cofnąć
Symulując początkowe warunki przypominające komórki nabłonkowe i mezenchymalne pod różnymi miksami TGFβ, BMP i czynników wzrostu, model pokazał, że ten sam zewnętrzny bodziec może mieć bardzo różne efekty w zależności od kontekstu. W wielu przypadkach BMP osłabiał program mezenchymalny napędzany przez TGFβ i przesuwał komórki w kierunku bardziej nabłonkowych lub hybrydowych stanów, ale często nie prowadził do pełnego powrotu. Symulacje uwydatniły też znaczenie samopodtrzymujących się pętli sprzężenia zwrotnego, w których komórki nowotworowe produkują własne sygnały TGFβ lub czynniki wzrostu. Takie pętle mogą podtrzymywać stan mezenchymalny nawet po ustaniu zewnętrznej stymulacji. Przerwanie konkretnych elementów tych pętli lub wzmocnienie pewnych pro‑nabłonkowych regulatorów przewidywano jako sposoby przesunięcia komórek ku stanom hybrydowym lub nabłonkowym, ale ostateczny efekt znów zależał od kombinacji sygnałów i warunków początkowych.
Co to oznacza dla rozumienia przerzutów
Podsumowując, praca sugeruje, że przejście mezenchymalno‑nabłonkowe w nowotworach nie jest rządzone przez jedyny „główny przełącznik”, lecz przez nakładające się sieci sygnałów, których wpływ jest silnie zależny od kontekstu. Niektóre cząsteczki zdają się być w stanie popchnąć komórki z powrotem ku stanowi podobnemu do nabłonkowego tylko w wąskich warunkach, podczas gdy inne działają szerzej, ale często pozostawiają komórki w stanach hybrydowych, które zachowują cechy inwazyjne. Dla osób niezajmujących się specjalistycznie tematem główny wniosek jest taki, że przerzuty opierają się na elastycznych tożsamościach komórkowych, a próby wymuszenia powrotu komórek do bezpieczniejszej, mniej ruchliwej formy będą musiały uwzględnić liczne pętle sprzężenia zwrotnego i sygnały środowiskowe stabilizujące te niebezpieczne stany pośrednie.
Cytowanie: Orozco-Ruiz, S., Ruscone, M., Barillot, E. et al. Mesenchymal to epithelial transition (MET) in cancer progression: insights from logical modeling. Sci Rep 16, 15032 (2026). https://doi.org/10.1038/s41598-026-44905-7
Słowa kluczowe: przejście nabłonkowo‑mezenchymalne, przerzuty nowotworowe, plastyczność komórek, modelowanie logiczne, białko morfogenetyczne kości