Clear Sky Science · pt
Transição mesenquimal para epitelial (MET) na progressão do câncer: insights a partir da modelagem lógica
Por que a mudança de forma das células cancerígenas importa
As células cancerígenas não apenas se dividem; elas também mudam sua forma e comportamento para se espalhar pelo corpo. Para escapar de um tumor, elas afrouxam seus laços com as células vizinhas e tornam-se mais móveis. Para formar novos tumores em outro lugar, frequentemente precisam recuperar sua forma original, mais firmemente conectada. Esse vaivém, conhecido como plasticidade celular, está no cerne da metástase. O estudo resumido aqui usa modelos lógicos computacionais para entender como as células cancerígenas reverteram de um estado móvel para um estado mais estabelecido, e por que essa reversão depende tanto das condições ao redor.
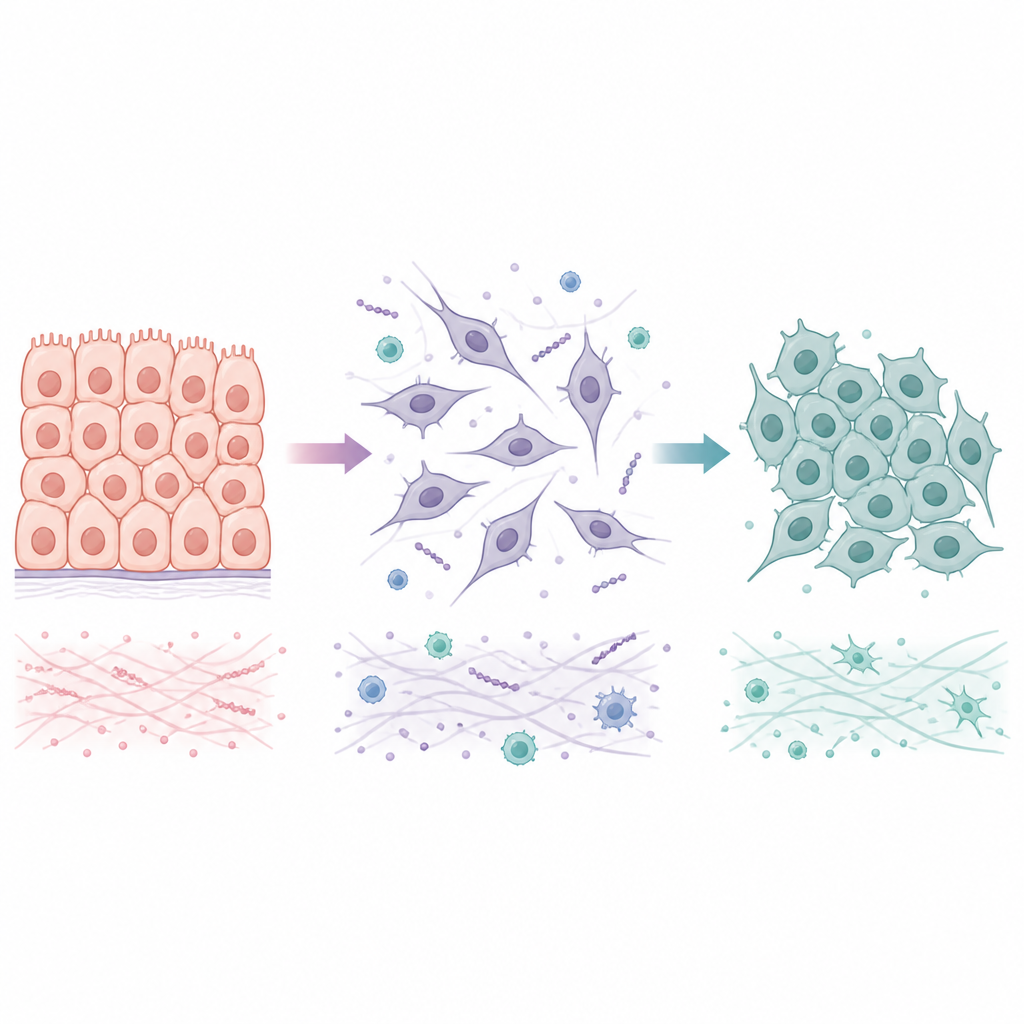
DuAS vias pelas quais as células transitam entre estados estabelecidos e móveis
Muitos tumores começam como células epiteliais, que estão fortemente ligadas em camadas ordenadas. Durante um processo chamado transição epitelial para mesenquimal, essas células perdem suas junções apertadas, mudam de forma e ganham capacidade de se mover e invadir tecidos e vasos sanguíneos próximos. Quando chegam a um novo órgão, frequentemente passam pela mudança inversa, transição mesenquimal para epitelial, o que as ajuda a formar colônias estáveis. Em vez de alternar apenas entre dois extremos, as células cancerígenas costumam ocupar estados híbridos que misturam características estabelecidas e móveis. Esses estados intermediários parecem especialmente aptos a sobreviver ao estresse e a semear metástases, tornando importante entender não apenas como ocorre a primeira transição, mas também como e quando ela pode ser revertida.
Sinais que empurram ou puxam a identidade da célula cancerígena
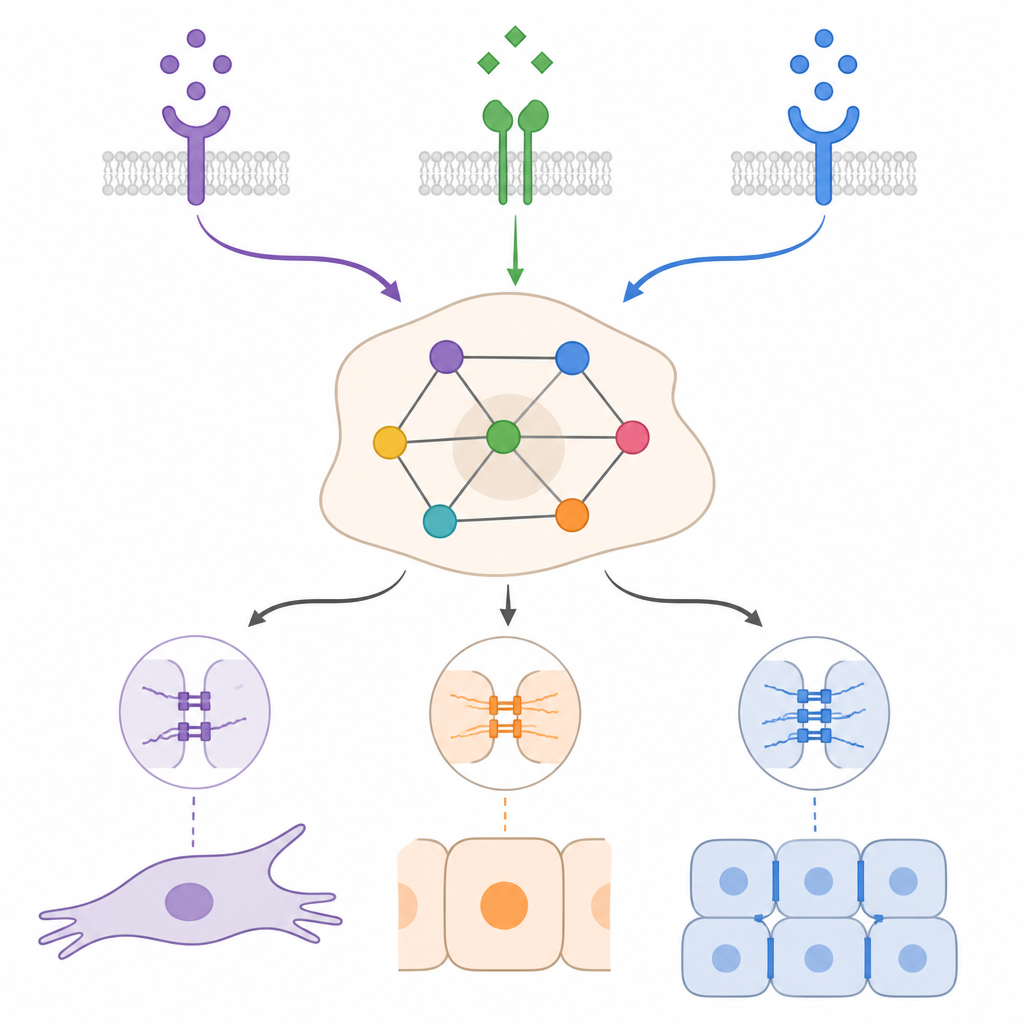
Sinais externos do microambiente tumoral influenciam fortemente se uma célula se comporta mais como epitelial ou mesenquimal. Sensores bem estudados, como TGFβ e vários fatores de crescimento, tendem a favorecer o lado móvel e invasivo, enquanto outros sinais, incluindo uma família de proteínas chamada BMP, podem favorecer o retorno a um estado epitelial. No interior da célula, redes de genes e pequenos RNAs reforçam uma identidade ou outra. Certos fatores de transcrição promovem a quebra das junções celulares e a remodelação da matriz circundante, enquanto outro grupo de fatores trabalha para restaurar contatos apertados e uma característica epitelial. Evidências experimentais mostram que não existe uma rota única e universal por esses programas; em vez disso, o resultado depende de quais sinais estão presentes, por quanto tempo e em qual tipo celular.
Construindo um mapa lógico das decisões celulares
Como muitos moléculas e circuitos de retroalimentação estão envolvidos, é difícil prever como uma célula cancerígena responderá em um cenário particular. Os autores reuniram informações publicadas sobre as vias-chave ligadas a ambas as direções da transição e as organizaram em uma rede regulatória. Em seguida, traduziram essa rede em um modelo lógico booleano, ou liga-desliga, e rodaram muitas simulações computacionais. Essa abordagem não tenta medir quantidades exatas de moléculas; em vez disso, explora quais combinações de sinais e reguladores internos levam a padrões estáveis de atividade gênica. O modelo produziu 25 estados de longo prazo que se agruparam naturalmente em categorias epitelial, mesenquimal, híbrida e ingênua, refletindo o espectro visto em estudos de laboratório.
O contexto molda o quanto as células podem reverter
Ao simular condições iniciais do tipo epitelial e do tipo mesenquimal sob diferentes combinações de TGFβ, BMP e fatores de crescimento, o modelo mostrou que o mesmo estímulo externo pode ter efeitos muito diferentes dependendo do contexto. Em muitos casos, o BMP foi capaz de enfraquecer um programa mesenquimal dirigido por TGFβ e empurrar as células para estados mais epiteliais ou híbridos, mas frequentemente parou antes de um retorno completo. As simulações também destacaram a importância de circuitos de retroalimentação auto-sustentáveis, nos quais as próprias células cancerígenas produzem TGFβ ou fatores de crescimento. Esses circuitos podem manter um estado mesenquimal mesmo após o desaparecimento do estímulo externo. Romper partes específicas desses circuitos, ou reforçar certos reguladores pró-epiteliais, foi previsto para deslocar as células em direção a estados híbridos ou epiteliais, mas o resultado exato novamente dependia da combinação de sinais e das condições iniciais.
O que isso significa para entender a metástase
No geral, o trabalho sugere que a transição mesenquimal para epitelial no câncer não é governada por um único interruptor mestre, mas por redes de sinais sobrepostas cujo impacto é altamente dependente do contexto. Algumas moléculas parecem capazes de empurrar as células de volta para um estado semelhante ao epitelial apenas em circunstâncias restritas, enquanto outras atuam de forma mais ampla, mas frequentemente ainda deixam as células em estados híbridos que retêm traços invasivos. Para não especialistas, a mensagem principal é que a metástase depende de identidades celulares flexíveis, e que tentativas de forçar as células de volta a uma forma mais segura e menos móvel precisarão levar em conta os muitos circuitos de retroalimentação e sinais ambientais que estabilizam essas condições intermediárias perigosas.
Citação: Orozco-Ruiz, S., Ruscone, M., Barillot, E. et al. Mesenchymal to epithelial transition (MET) in cancer progression: insights from logical modeling. Sci Rep 16, 15032 (2026). https://doi.org/10.1038/s41598-026-44905-7
Palavras-chave: transição epitelial mesenquimal, metástase do câncer, plasticidade celular, modelagem lógica, proteína morfogenética óssea