Clear Sky Science · tr
Kanser ilerlemesinde mezenkimalden epitele geçiş (MET): mantıksal modellemeden çıkarımlar
Neden kanser hücrelerinin şekil değiştirmesi önemlidir
Kanser hücreleri sadece bölünmez; ayrıca yayılarak vücutta konum değiştirmek için şekillerini ve davranışlarını değiştirirler. Bir tümörün dışına kaçmak için komşu hücrelerle bağlantılarını gevşetir ve daha hareketli hale gelirler. Başka yerde yeni tümörler oluşturmak için genellikle orijinal, sıkı bağlantılı hallerini yeniden kazanmaları gerekir. Hücresel plastisite olarak adlandırılan bu gidip gelmeler metastazın merkezindedir. Burada özetlenen çalışma, kanser hücrelerinin hareketli bir durumdan daha yerleşik bir duruma nasıl geri döndüğünü ve neden bu ters dönüşün çevresel koşullara bu kadar bağımlı olduğunu anlamak için bilgisayar tabanlı mantıksal modelleri kullanır.
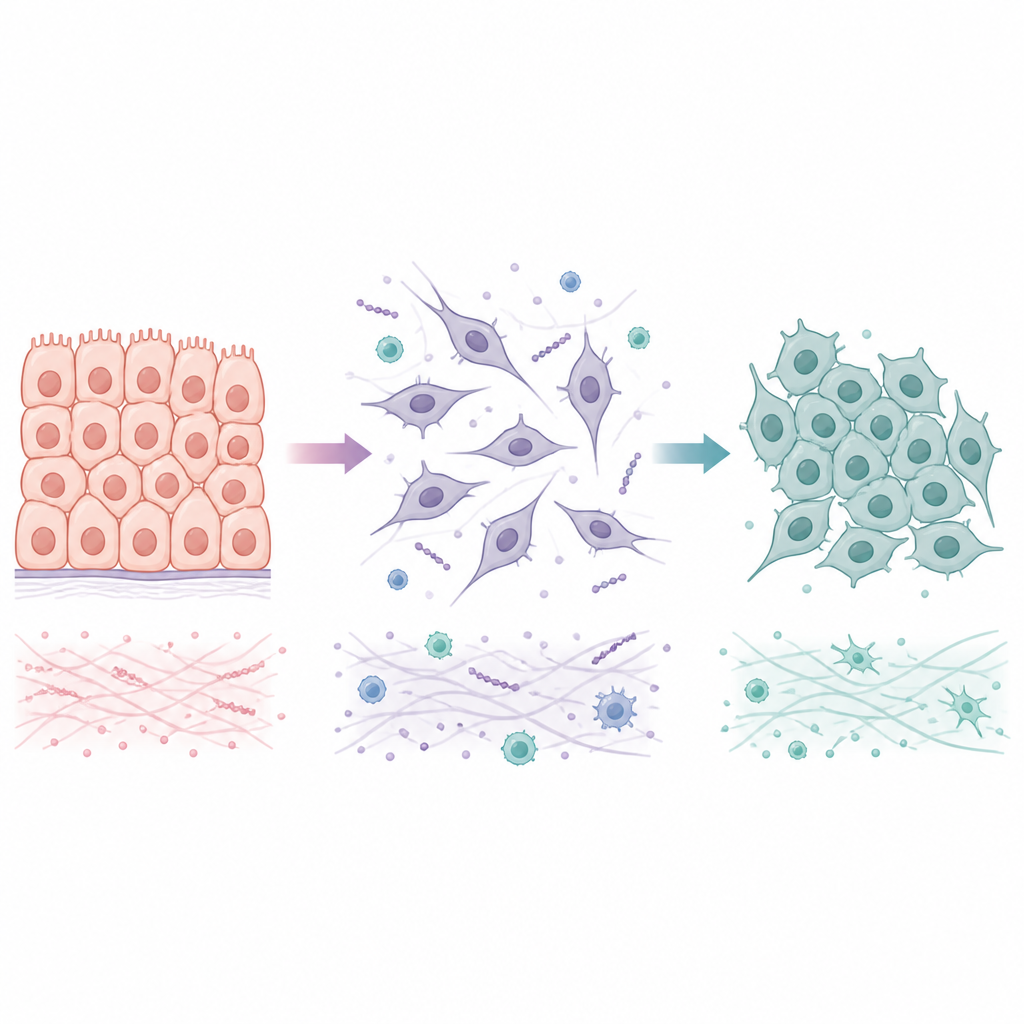
Hücrelerin yerleşik ve hareketli durumlar arasında seyahat etmesinin iki yolu
Birçok tümör epitel hücreleri olarak başlar; bunlar düzenli tabakalar halinde sıkı bağlantılıdır. Epitelden mezenkimale geçiş olarak bilinen süreç sırasında bu hücreler sıkı birleşimlerini kaybeder, şekil değiştirir ve hareket etme ile yakın doku ve kan damarlarına invaze olma yeteneği kazanır. Yeni bir organa ulaştıklarında ise genellikle ters yönde, mezenkimalden epitelyale geçişi yaşarlar; bu da stabil koloniler oluşturmalarına yardımcı olur. Sadece iki uç arasında tam bir anahtar gibi geçiş yapmak yerine, kanser hücreleri sıklıkla yerleşik ve hareketli özellikleri harmanlayan hibrit durumlarda bulunur. Bu ara durumlar stres altında hayatta kalma ve metastaz başlatma açısından özellikle yetenekli göründüğünden, yalnızca ilk geçişin nasıl gerçekleştiğini değil, aynı zamanda tersinin nasıl ve ne zaman olabileceğini de anlamak önem taşır.
Kanser hücre kimliğini iten veya çeken sinyaller
Tümör ortamından gelen dış sinyaller bir hücrenin daha çok epitel ya da mezenkimal davranıp davranmayacağını güçlü biçimde etkiler. TGFβ ve çeşitli büyüme faktörleri gibi iyi incelenmiş sürücüler genellikle hareketli, invaziv tarafı teşvik ederken, BMP adı verilen protein ailesi dahil bazı sinyaller epitelik bir duruma geri dönmeyi destekleyebilir. Hücre içinde ise genler ve küçük RNA’lardan oluşan ağlar bir kimliği veya diğerini pekiştirir. Belirli transkripsiyon faktörleri hücre bağlantılarının yıkımını ve çevreleyen matriksin yeniden düzenlenmesini teşvik ederken, başka bir faktör grubu sıkı temasları ve epitel karakteri geri kazanmaya çalışır. Deneysel kanıtlar, bu programlar boyunca tek, evrensel bir yol olmadığını; sonucun hangi sinyallerin var olduğuna, ne kadar süreyle etkili olduklarına ve hangi hücre tipinde olduklarına bağlı olduğunu gösterir.
Hücresel kararların mantıksal haritasını kurmak
Bu kadar çok molekül ve geri besleme döngüsü dahil olduğu için, belirli bir ortamda bir kanser hücresinin nasıl tepki vereceğini tahmin etmek zordur. Yazarlar, geçişin her iki yönüyle ilişkili ana yolaklara dair yayımlanmış bilgileri topladılar ve bunları bir düzenleyici ağ halinde organize ettiler. Ardından bu ağı bir Boole, yani açık–kapalı mantıksal modele çevirdiler ve çok sayıda bilgisayar simülasyonu çalıştırdılar. Bu yaklaşım belirli molekül miktarlarını ölçmeyi amaçlamaz; bunun yerine hangi sinyal ve iç düzenleyici kombinasyonlarının gen aktivitesinin stabil desenlerine yol açtığını araştırır. Model, laboratuvar çalışmalarında görülen spektrumu yansıtarak epitel, mezenkimal, hibrit ve naif kategorilerine doğal olarak gruplanan 25 uzun dönemli durum üretti.
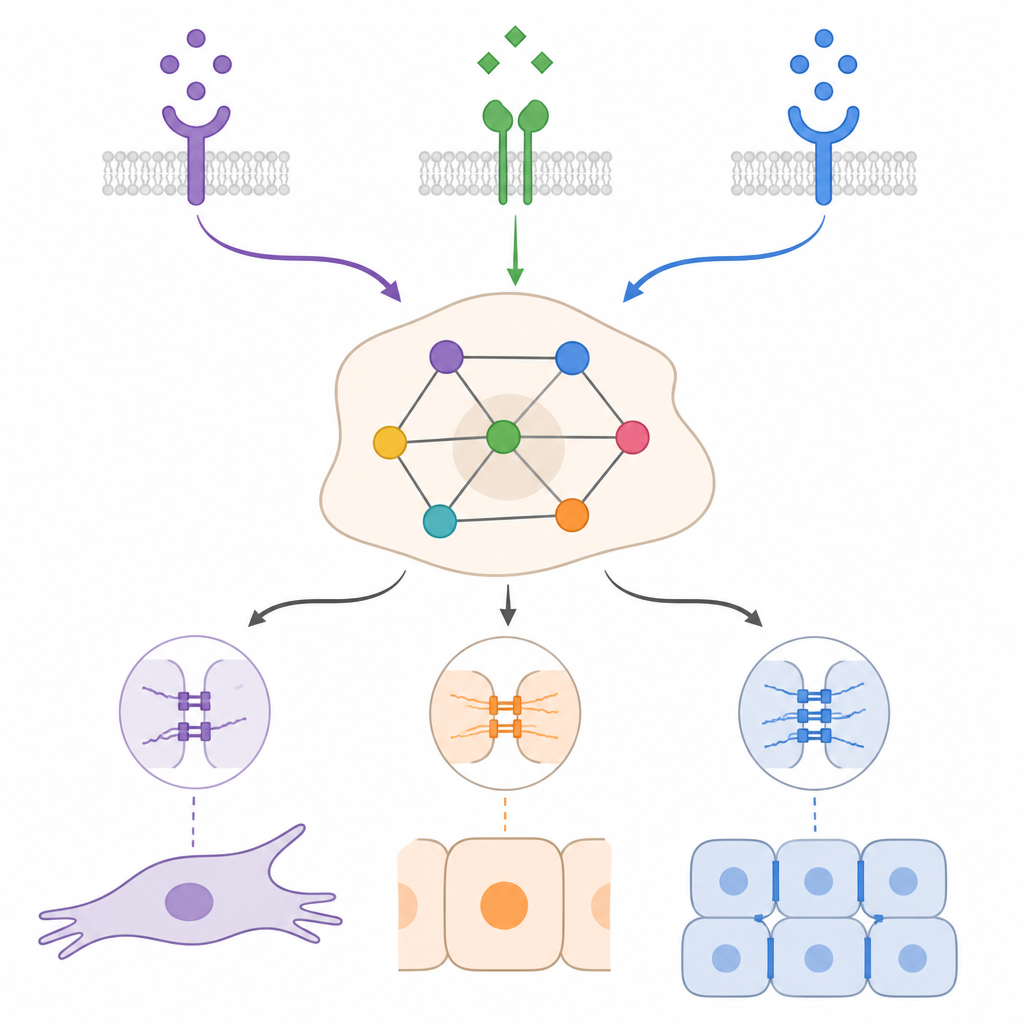
Bağlam, hücrelerin ne kadar geri dönebileceğini şekillendirir
Epitel-benzeri ve mezenkimal-benzeri başlangıç koşullarını farklı TGFβ, BMP ve büyüme faktörü karışımları altında simüle ederek, model aynı dış ipucunun bağlama bağlı olarak çok farklı etkileri olabileceğini gösterdi. Birçok durumda BMP, TGFβ odaklı mezenkimal programı zayıflatıp hücreleri daha epitelik veya hibrit durumlara itebiliyordu, ancak çoğunlukla tam bir geri dönüşün eşiğinde durdu. Simülasyonlar ayrıca kanser hücrelerinin kendi TGFβ veya büyüme faktörü sinyallerini ürettikleri kendi kendini sürdüren geri besleme döngülerinin önemini vurguladı. Bu döngüler, dış uyarı ortadan kalktıktan sonra bile mezenkimal durumu koruyabilir. Bu döngülerin belirli kısımlarını kırmak veya bazı pro-epitel düzenleyicileri güçlendirmek hücreleri hibrit veya epitel durumlarına kaydırmayı öngördü, ancak kesin sonuç yine sinyal kombinasyonuna ve başlangıç koşullarına bağlıydı.
Metastazı anlamak için ne anlama geliyor
Genel olarak çalışma, kanserde mezenkimalden epitele geçişin tek bir ana anahtar tarafından değil, etkisi büyük ölçüde bağlama bağlı olan örtüşen sinyal ağları tarafından yönetildiğini öne sürüyor. Bazı moleküller hücreleri yalnızca sınırlı koşullarda epitel-benzeri bir duruma geri itebilecek gibi görünürken, diğerleri daha geniş çapta etki gösterebilir ama çoğu zaman hücreleri invaziv özellikleri koruyan hibrit durumlarda bırakır. Uzman olmayanlar için ana mesaj şudur: Metastaz esnek hücre kimliklerine dayanır ve hücreleri daha güvenli, daha az hareketli bir forma zorlamaya yönelik girişimler bu tehlikeli ara koşulları stabilize eden çok sayıda geri besleme döngüsünü ve çevresel ipucunu göz önünde bulundurmalıdır.
Atıf: Orozco-Ruiz, S., Ruscone, M., Barillot, E. et al. Mesenchymal to epithelial transition (MET) in cancer progression: insights from logical modeling. Sci Rep 16, 15032 (2026). https://doi.org/10.1038/s41598-026-44905-7
Anahtar kelimeler: epitel mezenkimal geçiş, kanser metastazı, hücre plastisitesi, mantıksal modelleme, kemik morfogenetik protein