Clear Sky Science · sv
Mesenkymal till epitelial övergång (MET) i cancerprogression: insikter från logisk modellering
Varför det spelar roll att cancerceller ändrar form
Cancerceller delar sig inte bara; de ändrar också form och beteende för att sprida sig i kroppen. För att lämna en tumör släpper de sina bindningar till grannceller och blir mer rörliga. För att växa nya tumörer på andra ställen behöver de ofta återfå sin ursprungliga, tätt sammanhållna form. Denna växling fram och tillbaka, känd som cellulär plasticitet, står i centrum för metastasering. Studien som sammanfattas här använder datorbaserade logiska modeller för att förstå hur cancerceller växlar tillbaka från en rörlig till en mer stationär form, och varför denna återgång är så beroende av omgivande förhållanden.
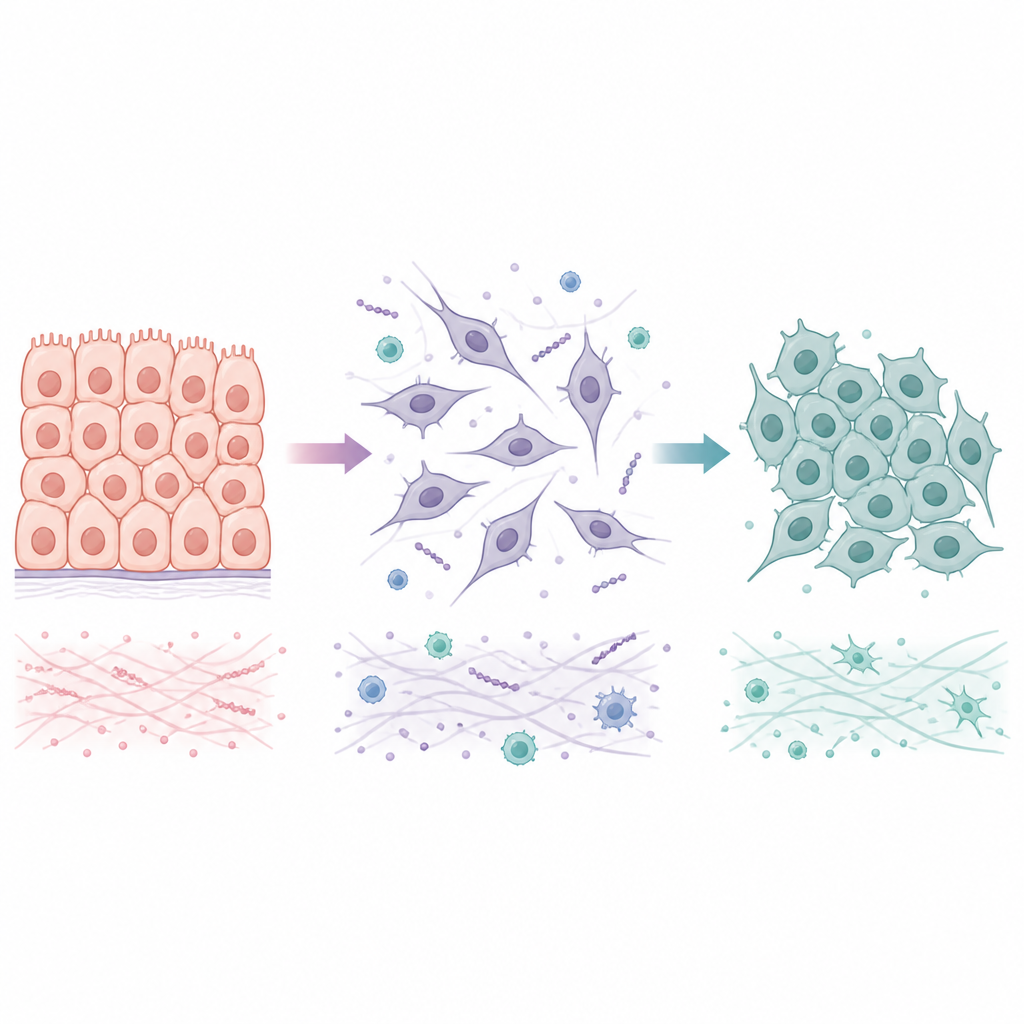
Två sätt celler rör sig mellan stationära och rörliga tillstånd
Många tumörer börjar som epitelceller, som sitter tätt ihop i ordnade lager. Under en process kallad epitelial till mesenkymal övergång förlorar dessa celler sina täta förbindelser, ändrar form och får förmågan att röra sig och invadera intilliggande vävnad och blodkärl. När de når ett nytt organ genomgår de ofta den omvända förskjutningen, mesenkymal till epitelial övergång, vilket hjälper dem att bilda stabila kolonier. Istället för att växla mellan bara två ändpunkter intar cancerceller ofta hybrida tillstånd som blandar stationära och rörliga egenskaper. Dessa mellanliggande tillstånd tycks vara särskilt bra på att tåla stress och så frö för metastaser, vilket gör det viktigt att förstå inte bara hur den första övergången sker utan också hur och när den kan vändas.
Signaler som skjuter eller drar i cancercellsidentitet
Yttre signaler från tumörmiljön påverkar starkt om en cell beter sig mer som en epitelial eller mesenkymal cell. Välstuderade drivkrafter som TGFβ och olika tillväxtfaktorer tenderar att gynna den rörliga, invasiva sidan, medan andra signaler, inklusive en proteinfamilj kallad BMP, kan främja återgång mot ett epitelialt tillstånd. Inuti cellen förstärker nätverk av gener och små RNA antingen den ena eller den andra identiteten. Vissa transkriptionsfaktorer främjar nedbrytning av cellförbindelser och ombyggnad av den omgivande matrisen, medan en annan grupp faktorer arbetar för att återställa täta kontakter och ett epitelialt uttryck. Experimentella bevis visar att det inte finns en enda universell väg genom dessa program; i stället beror utfallet på vilka signaler som är närvarande, hur länge och i vilken celltyp.
Att bygga en logisk karta över cellulära beslut
Eftersom så många molekyler och återkopplingsslingor är involverade är det svårt att gissa hur en cancercell kommer att reagera i en viss situation. Författarna sammanställde publicerad information om nyckelvägar kopplade till båda riktningarna av övergången och organiserade det i ett regleringsnätverk. De översatte sedan detta nätverk till en Boolesk, eller av/på, logisk modell och körde många datorsimuleringar. Detta tillvägagångssätt försöker inte mäta exakta mängder molekyler; i stället utforskar det vilka kombinationer av signaler och interna regulatorer som leder till stabila mönster av genaktivitet. Modellen gav 25 långsiktiga tillstånd som naturligt grupperade sig i epiteliala, mesenkymala, hybrida och naiva kategorier, vilket speglar det spektrum som observerats i laboratoriestudier.
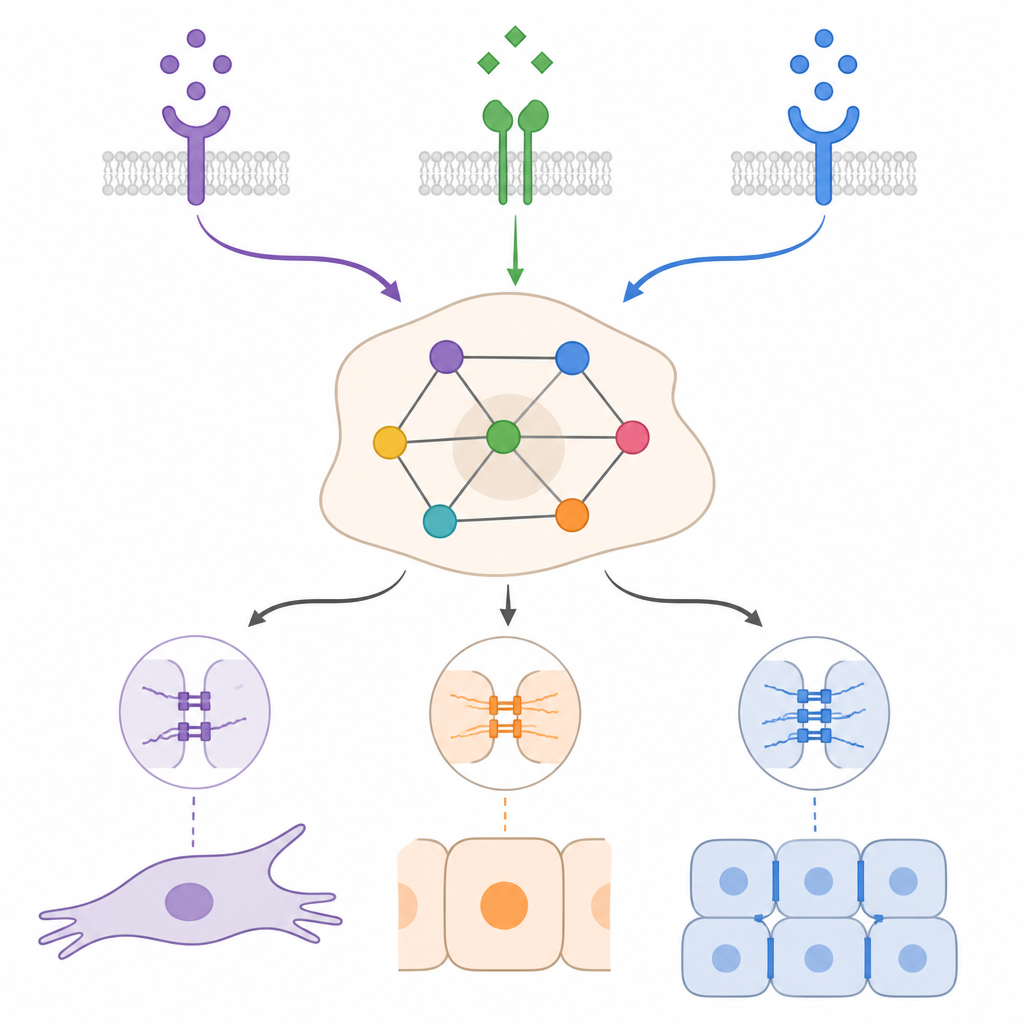
Kontext formar hur långt celler kan återgå
Genom att simulera epiteliala och mesenkymala börjanstillstånd under olika blandningar av TGFβ, BMP och tillväxtfaktorer visade modellen att samma yttre signal kan ha mycket olika effekter beroende på kontext. I många fall kunde BMP försvaga ett TGFβ-drivet mesenkymalt program och skjuta celler mot mer epiteliala eller hybrida tillstånd, men ofta räckte det inte till en fullständig återgång. Simulatorerna framhävde också vikten av självuppehållande återkopplingsslingor där cancerceller producerar sina egna TGFβ- eller tillväxtfaktorsignaler. Dessa slingor kan upprätthålla ett mesenkymalt tillstånd även efter att yttre stimulans försvunnit. Att bryta specifika delar av dessa slingor, eller att öka vissa pro-epiteliala regulatorer, förutsågs flytta celler mot hybrida eller epiteliala tillstånd, men det exakta utfallet berodde återigen på kombinationen av signaler och börjanstillstånd.
Vad detta innebär för förståelsen av metastas
Sammantaget tyder arbetet på att mesenkymal till epitelial övergång i cancer inte styrs av en enda huvudomkopplare, utan av överlappande nätverk av signaler vars effekter är starkt kontextberoende. Vissa molekyler verkar kunna knuffa celler tillbaka mot ett epitelialt liknande tillstånd endast under snäva omständigheter, medan andra verkar verka mer brett men ofta ändå lämnar celler i hybrida tillstånd som behåller invasiva egenskaper. För icke-specialister är huvudbudskapet att metastas bygger på flexibla cellidentiteter, och att försök att tvinga celler tillbaka till en säkrare, mindre rörlig form måste ta hänsyn till de många återkopplingsslingor och miljösignaler som stabiliserar dessa farliga mellanliggande tillstånd.
Citering: Orozco-Ruiz, S., Ruscone, M., Barillot, E. et al. Mesenchymal to epithelial transition (MET) in cancer progression: insights from logical modeling. Sci Rep 16, 15032 (2026). https://doi.org/10.1038/s41598-026-44905-7
Nyckelord: epitelial mesenkymal övergång, cancermetastas, cellplastiskhet, logisk modellering, benmorfogenetiskt protein