Clear Sky Science · nl
Mesenchymale naar epitheliale overgang (MET) bij kankerprogressie: inzichten uit logisch modelleren
Waarom het van belang is dat kankercellen van vorm veranderen
Kankercellen delen niet alleen; ze veranderen ook hun vorm en gedrag om zich door het lichaam te verspreiden. Om een tumor te verlaten, laten ze hun verbindingen met naburige cellen los en worden ze beweeglijker. Om elders nieuwe tumoren te doen groeien, moeten ze vaak hun oorspronkelijke, strak verbonden vorm herstellen. Dit heen en weer schuiven, bekend als cellulaire plasticiteit, staat centraal in metastase. De hier samengevatte studie gebruikt computergestuurde logische modellen om te begrijpen hoe kankercellen terugschakelen van een beweeglijke naar een meer vaste staat, en waarom deze omkering zo afhankelijk is van de omliggende omstandigheden.
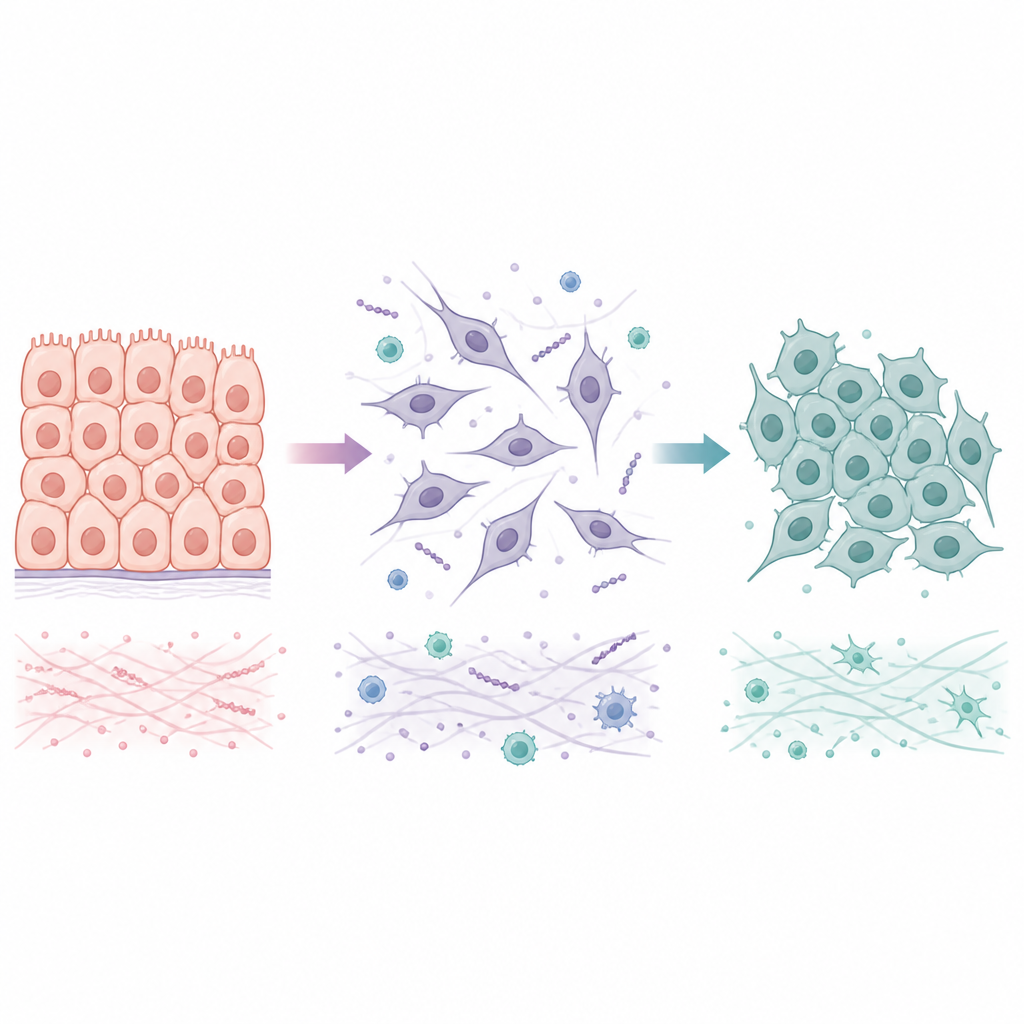
Twee manieren waarop cellen tussen vaste en beweeglijke staten reizen
Veel tumoren beginnen als epitheliale cellen, die stevig in ordelijke lagen met elkaar verbonden zijn. Tijdens een proces dat epitheliale naar mesenchymale transitie heet, verliezen deze cellen hun nauwe verbindingen, veranderen van vorm en verwerven het vermogen om te bewegen en naburig weefsel en bloedvaten binnen te dringen. Wanneer ze in een nieuw orgaan aankomen, ondergaan ze vaak de omgekeerde verschuiving, mesenchymale naar epitheliale transitie, wat helpt bij het vormen van stabiele kolonies. In plaats van slechts tussen twee uitersten te schakelen, nemen kankercellen vaak hybride toestanden in waarin zowel vaste als beweeglijke kenmerken gemengd zijn. Deze tussenliggende toestanden blijken bijzonder goed bestand tegen stress en effectief in het zaaien van metastasen, wat het belangrijk maakt om niet alleen te begrijpen hoe de eerste transitie plaatsvindt, maar ook hoe en wanneer deze kan worden omgekeerd.
Signalen die aan de identiteit van kankercellen trekken of duwen
Externe signalen uit de tumoromgeving beïnvloeden sterk of een cel zich meer gedraagt als een epitheliale of mesenchymale cel. Goed bestudeerde drijfveren zoals TGFβ en verschillende groeifactoren bevorderen doorgaans de beweeglijke, invasieve kant, terwijl andere signalen, waaronder een proteïne-familie die BMP wordt genoemd, een terugkeer naar een epitheliale staat kunnen begunstigen. Binnenin de cel versterken netwerken van genen en kleine RNA’s de ene identiteit of de andere. Bepaalde transcriptiefactoren bevorderen de afbraak van celkoppelingen en de herinrichting van de omringende matrix, terwijl een andere groep factoren werkt aan het herstellen van nauwe contacten en een epitheliaal karakter. Experimenteel bewijs toont aan dat er geen enkele universele route door deze programma’s bestaat; in plaats daarvan hangt de uitkomst af van welke signalen aanwezig zijn, hoe lang ze aanhouden en in welk celtype ze optreden.
Het bouwen van een logisch kaart van cellulaire beslissingen
Aangezien zoveel moleculen en terugkoppelingslussen betrokken zijn, is het moeilijk te voorspellen hoe een kankercel in een bepaalde situatie zal reageren. De auteurs verzamelden gepubliceerde informatie over sleutelroutes die met beide richtingen van de transitie verbonden zijn en organiseerden die in een regulatoir netwerk. Ze vertaalden dit netwerk vervolgens naar een Booleaans, oftewel aan-uit, logisch model en voerden veel computersimulaties uit. Deze aanpak probeert geen exacte molecuulhoeveelheden te meten; in plaats daarvan onderzoekt ze welke combinaties van signalen en interne regulatoren leiden tot stabiele patronen van genactiviteit. Het model leverde 25 langetermijnstaten op die zich vanzelf groeperen in epitheliale, mesenchymale, hybride en naïeve categorieën, wat het spectrum weerspiegelt dat in laboratoriumstudies wordt gezien.
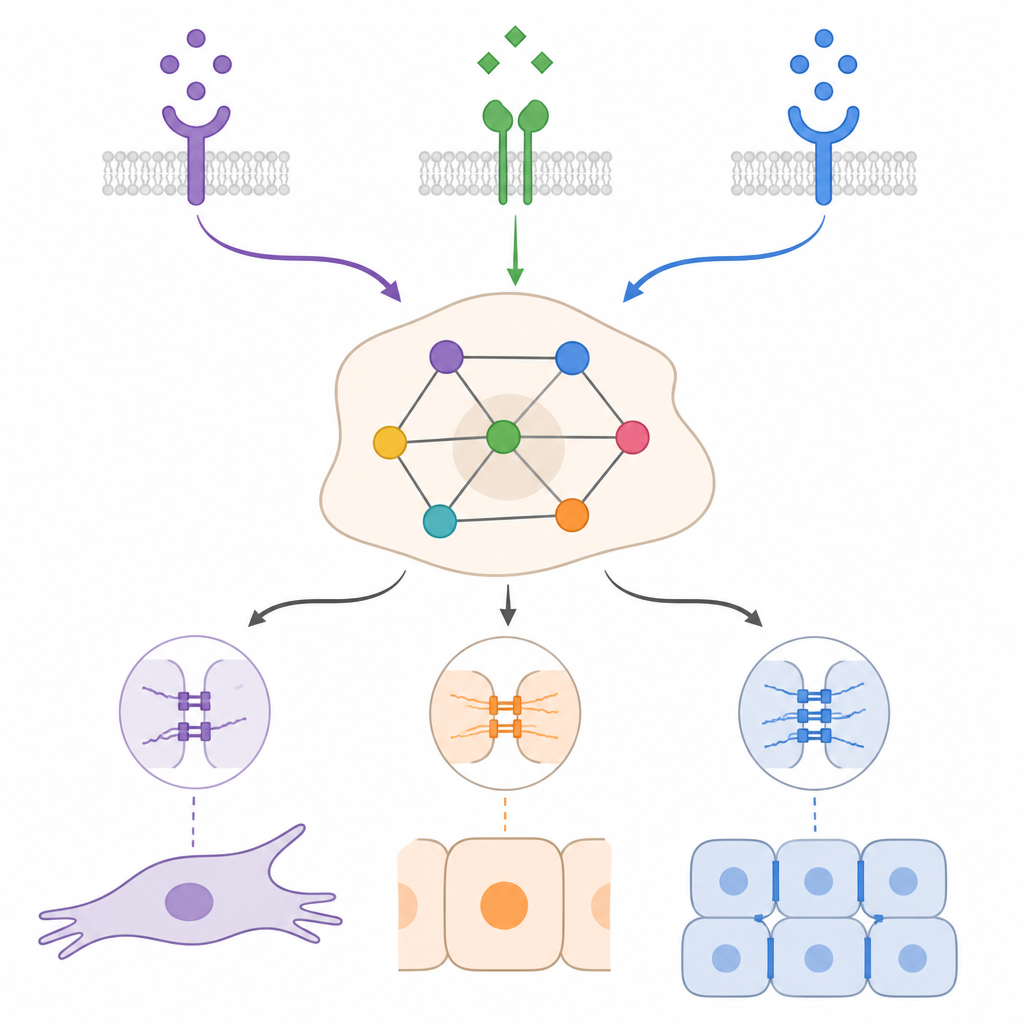
Context bepaalt in hoeverre cellen kunnen terugkeren
Door epitheliaal-achtige en mesenchymaal-achtige begintoestanden te simuleren onder verschillende mixes van TGFβ, BMP en groeifactoren, toonde het model aan dat dezelfde externe prikkel zeer verschillende effecten kan hebben, afhankelijk van de context. In veel gevallen kon BMP een door TGFβ aangestuurd mesenchymaal programma verzwakken en cellen richting meer epitheliale of hybride toestanden duwen, maar vaak bleef het steken vóór een volledige terugkeer. De simulaties benadrukten ook het belang van zelfonderhoudende terugkoppelingslussen, waarbij kankercellen hun eigen TGFβ- of groeifactorsignalen produceren. Deze lussen kunnen een mesenchymale staat in stand houden, zelfs nadat de externe stimulatie verdwenen is. Het breken van specifieke onderdelen van deze lussen, of het versterken van bepaalde pro-epitheliale regulatoren, voorspelde een verschuiving van cellen richting hybride of epitheliale staten, maar de precieze uitkomst hing opnieuw af van de combinatie van signalen en begintoestanden.
Wat dit betekent voor het begrip van metastase
Samenvattend suggereert het werk dat mesenchymale naar epitheliale overgang bij kanker niet wordt bestuurd door één enkele hoofdschakelaar, maar door overlappende netwerken van signalen waarvan de impact sterk contextafhankelijk is. Sommige moleculen lijken in beperkte omstandigheden cellen terug richting een epitheliaal-achtig stadium te kunnen duwen, terwijl anderen breder werken maar vaak nog steeds cellen in hybride toestanden achterlaten die invasieve eigenschappen behouden. Voor niet-specialisten is de belangrijkste boodschap dat metastase afhankelijk is van flexibele celidentiteiten, en dat pogingen om cellen gedwongen terug te brengen naar een veiligere, minder beweeglijke vorm rekening moeten houden met de vele terugkoppelingslussen en omgevingssignalen die deze gevaarlijke tussentoestanden stabiliseren.
Bronvermelding: Orozco-Ruiz, S., Ruscone, M., Barillot, E. et al. Mesenchymal to epithelial transition (MET) in cancer progression: insights from logical modeling. Sci Rep 16, 15032 (2026). https://doi.org/10.1038/s41598-026-44905-7
Trefwoorden: epitheliale mesenchymale transitie, kankermetastase, celplasticiteit, logisch modelleren, bone morphogenetic protein