Clear Sky Science · it
Transizione mesenchimale-epiteliale (MET) nella progressione del cancro: intuizioni dalla modellizzazione logica
Perché conta che le cellule tumorali cambino forma
Le cellule tumorali non si limitano a dividersi; cambiano anche forma e comportamento per diffondersi nell’organismo. Per sfuggire al tumore si allentano i legami con le cellule vicine e diventano più mobili. Per crescere nuovi tumori in altri siti, spesso devono riconquistare la loro forma originaria, più compatta e connessa. Questo continuo passaggio, noto come plasticità cellulare, è al centro della metastasi. Lo studio qui riassunto usa modelli logici al computer per comprendere come le cellule tumorali ritornino da uno stato mobile a uno più stabile e perché questo ripristino dipenda tanto dalle condizioni circostanti.
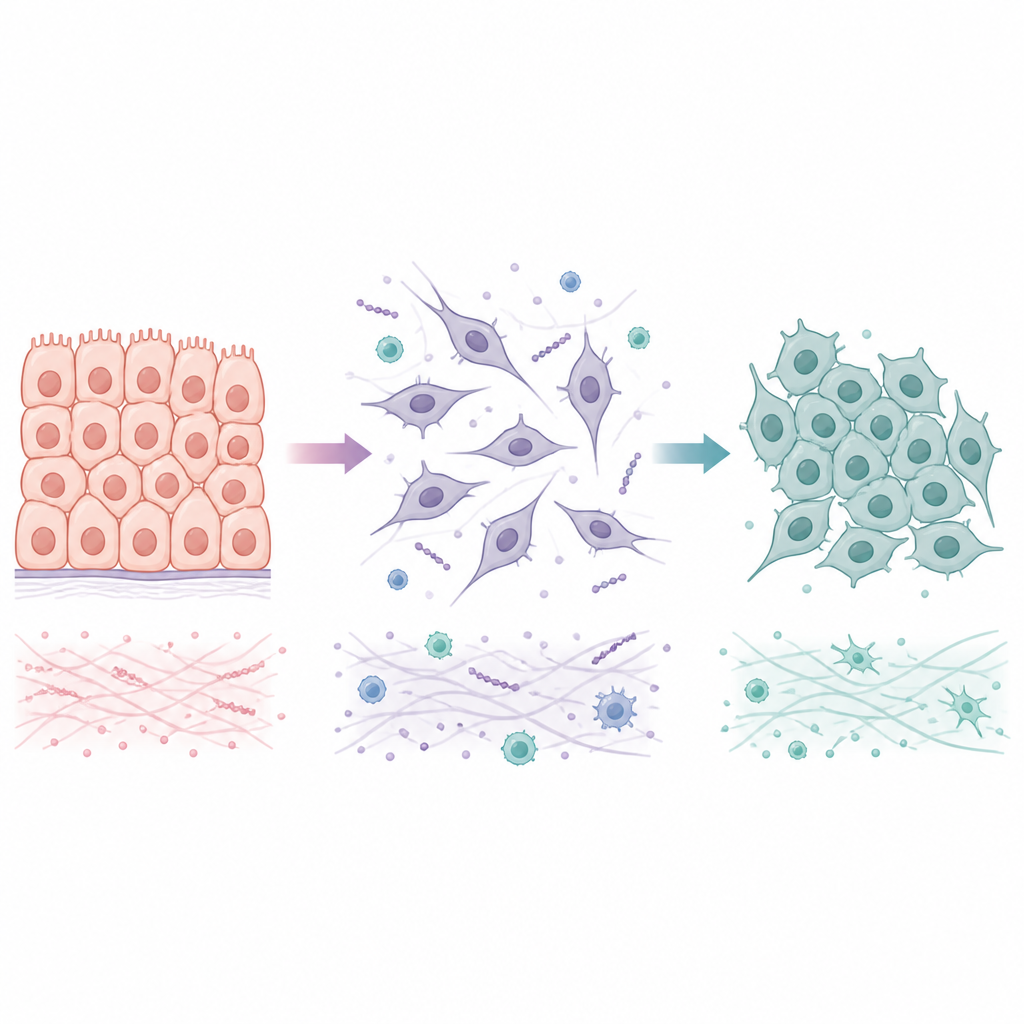
Due modi in cui le cellule transitano tra stati stabili e mobili
Molti tumori iniziano come cellule epiteliali, strettamente collegate in fogli ordinati. Durante un processo chiamato transizione epiteliale-mesenchimale, queste cellule perdono le giunzioni strette, cambiano forma e acquisiscono la capacità di muoversi e invadere i tessuti circostanti e i vasi sanguigni. Quando raggiungono un nuovo organo, spesso subiscono lo spostamento inverso, la transizione mesenchimale-epiteliale, che le aiuta a formare colonie stabili. Piuttosto che passare solo tra due estremi, le cellule tumorali spesso occupano stati ibridi che mescolano caratteristiche stabili e mobili. Questi stati intermedi sembrano particolarmente abili a sopravvivere allo stress e a dare origine a metastasi, perciò è importante capire non solo come avvenga la prima transizione, ma anche come e quando possa essere invertita.
I segnali che spingono o tirano sull’identità delle cellule tumorali
I segnali esterni dall’ambiente tumorale influenzano fortemente se una cellula si comporta più da epiteliale o da mesenchimale. Driver ben studiati come il TGFβ e vari fattori di crescita tendono a favorire il lato mobile e invasivo, mentre altri segnali, inclusa una famiglia di proteine chiamata BMP, possono favorire il ritorno verso uno stato epiteliale. All’interno della cellula, reti di geni e piccoli RNA rinforzano un’identità piuttosto che l’altra. Certi fattori di trascrizione promuovono la disgregazione delle giunzioni cellulari e il rimodellamento della matrice circostante, mentre un altro gruppo di fattori lavora per ristabilire contatti stretti e un carattere epiteliale. L’evidenza sperimentale mostra che non esiste un’unica via universale attraverso questi programmi; piuttosto, l’esito dipende da quali segnali sono presenti, per quanto tempo e in quale tipo cellulare.
Costruire una mappa logica delle decisioni cellulari
Poiché sono coinvolte così tante molecole e anelli di retroazione, è difficile prevedere come risponderà una cellula tumorale in un dato contesto. Gli autori hanno raccolto informazioni pubblicate sui percorsi chiave legati a entrambe le direzioni della transizione e le hanno organizzate in una rete regolatoria. Hanno poi tradotto questa rete in un modello logico booleano, cioè acceso–spento, e hanno eseguito molte simulazioni al computer. Questo approccio non cerca di misurare quantità precise di molecole; esplora invece quali combinazioni di segnali e regolatori interni portano a schemi stabili di attività genica. Il modello ha prodotto 25 stati a lungo termine che si sono raggruppati naturalmente in categorie epiteliale, mesenchimale, ibrida e naive, rispecchiando lo spettro osservato negli studi di laboratorio.
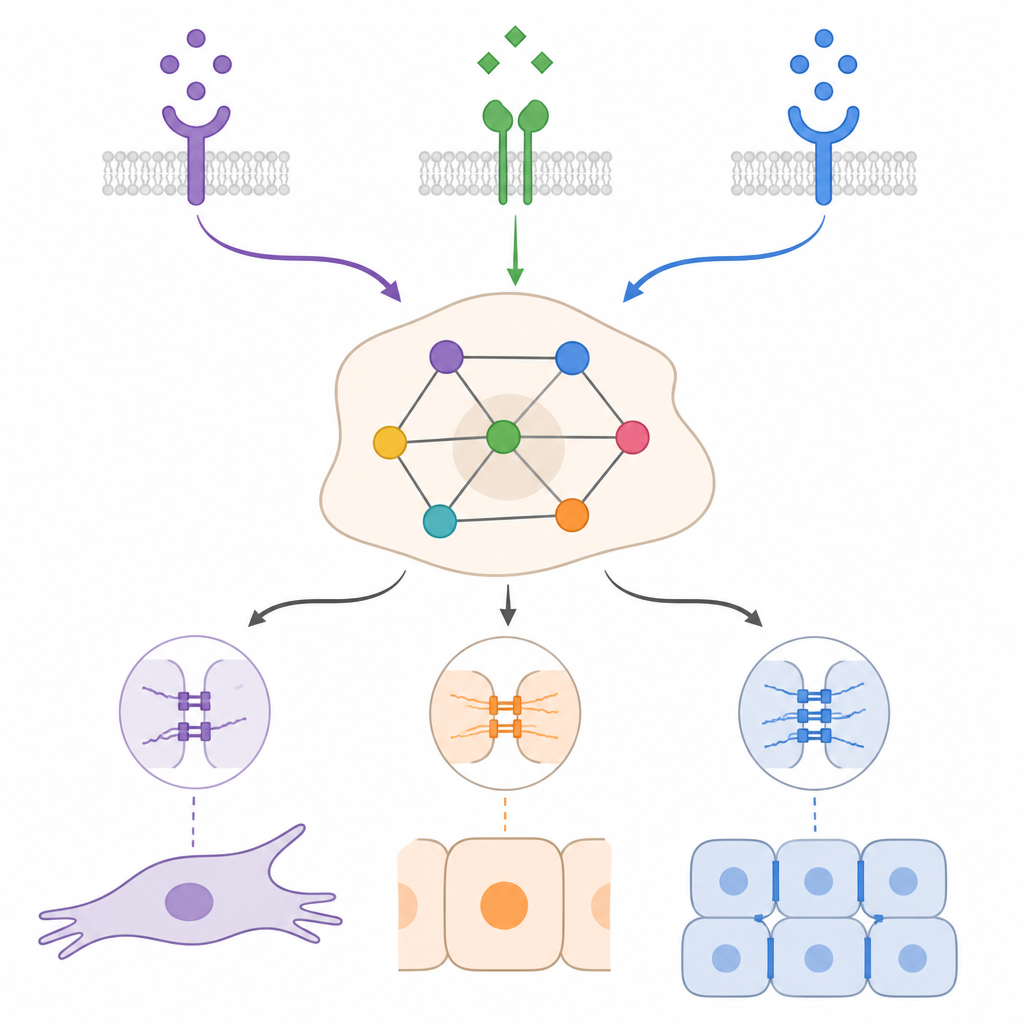
Il contesto modella quanto le cellule possano regredire
Simulando condizioni iniziali di tipo epiteliale e mesenchimale con diverse combinazioni di TGFβ, BMP e fattori di crescita, il modello ha mostrato che lo stesso stimolo esterno può avere effetti molto diversi a seconda del contesto. In molti casi il BMP è stato in grado di indebolire un programma mesenchimale guidato dal TGFβ e spingere le cellule verso stati più epiteliali o ibridi, ma spesso si fermava prima di un ritorno completo. Le simulazioni hanno inoltre evidenziato l’importanza di anelli di retroazione auto-sostenuti, in cui le cellule tumorali producono il proprio TGFβ o fattori di crescita. Questi circuiti possono mantenere uno stato mesenchimale anche dopo che lo stimolo esterno è scomparso. Rompere parti specifiche di questi anelli, o potenziare certi regolatori pro-epiteliali, era previsto spostare le cellule verso stati ibridi o epiteliali, ma l’esito preciso dipendeva nuovamente dalla combinazione di segnali e dalle condizioni iniziali.
Cosa significa per la comprensione delle metastasi
Nel complesso, il lavoro suggerisce che la transizione mesenchimale-epiteliale nel cancro non è governata da un singolo interruttore maestro, ma da reti sovrapposte di segnali il cui impatto è altamente dipendente dal contesto. Alcune molecole sembrano in grado di spingere le cellule verso uno stato epiteliale-like solo in circostanze ristrette, mentre altre agiscono più ampiamente ma spesso lasciano comunque le cellule in stati ibridi che conservano tratti invasivi. Per i non specialisti, il messaggio principale è che la metastasi si basa su identità cellulari flessibili e che i tentativi di forzare le cellule a tornare a una forma meno mobile e più sicura dovranno tener conto dei molti anelli di retroazione e dei segnali ambientali che stabilizzano queste pericolose condizioni intermedie.
Citazione: Orozco-Ruiz, S., Ruscone, M., Barillot, E. et al. Mesenchymal to epithelial transition (MET) in cancer progression: insights from logical modeling. Sci Rep 16, 15032 (2026). https://doi.org/10.1038/s41598-026-44905-7
Parole chiave: transizione epiteliale mesenchimale, metastasi del cancro, plasticità cellulare, modellizzazione logica, proteina morfogenetica ossea