Clear Sky Science · fr
Transition mésenchymateuse vers épithéliale (MET) dans la progression du cancer : éclairages issus de la modélisation logique
Pourquoi le changement de forme des cellules cancéreuses a de l’importance
Les cellules cancéreuses ne se contentent pas de se diviser ; elles modifient aussi leur forme et leur comportement pour se disséminer dans l’organisme. Pour quitter une tumeur, elles relâchent leurs liens avec les cellules voisines et gagnent en mobilité. Pour former de nouvelles tumeurs ailleurs, elles doivent souvent retrouver leur état initial, fortement connecté. Ce va-et-vient, appelé plasticité cellulaire, est au cœur de la métastase. L’étude résumée ici utilise des modèles logiques informatiques pour comprendre comment les cellules cancéreuses repassent d’un état mobile à un état plus sédentaire, et pourquoi cette inversion dépend tant des conditions environnantes.
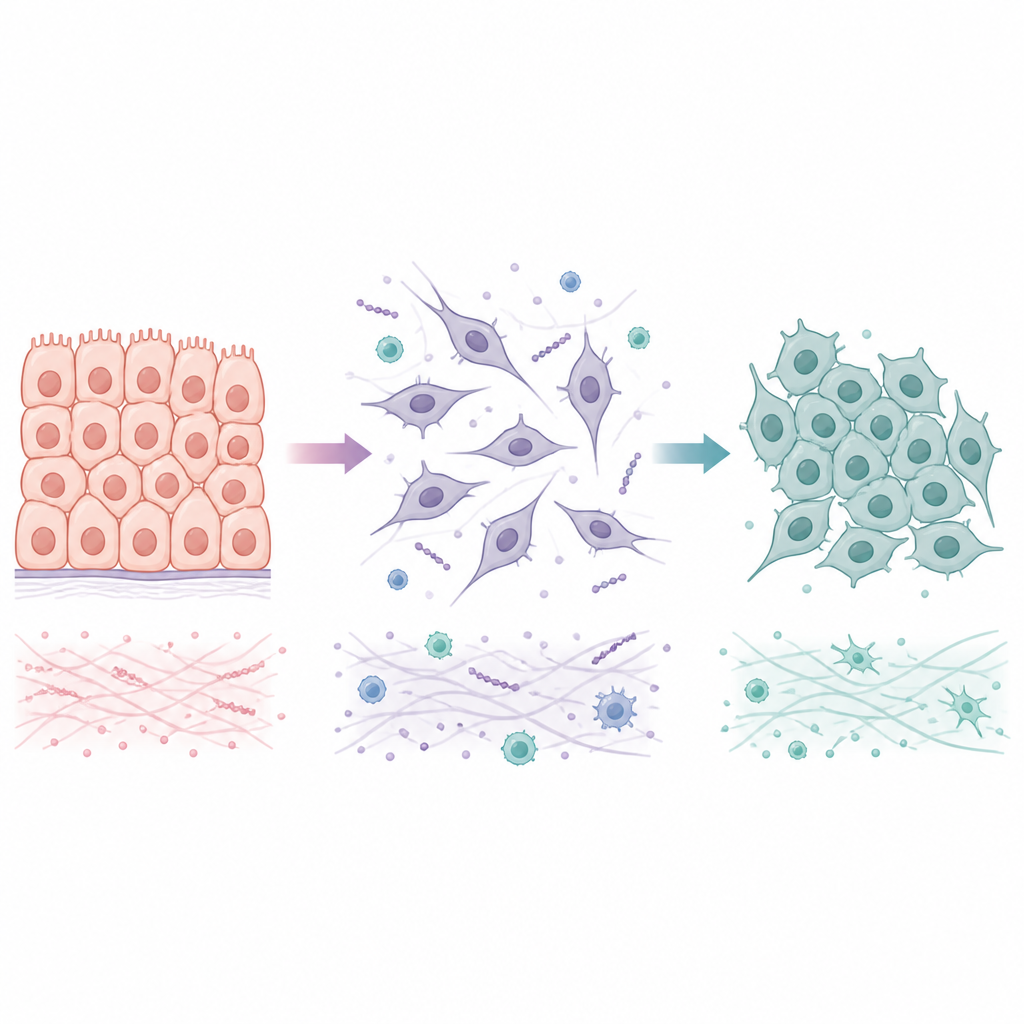
Deux manières pour les cellules de passer entre états sédentaires et mobiles
Beaucoup de tumeurs proviennent de cellules épithéliales, fortement liées en feuillets ordonnés. Lors d’un processus appelé transition épithéliale–mésenchymateuse, ces cellules perdent leurs jonctions serrées, changent de forme et acquièrent la capacité de se déplacer et d’envahir les tissus voisins et les vaisseaux sanguins. Quand elles atteignent un nouvel organe, elles subissent souvent la transition inverse, mésenchymateuse–épithéliale, qui les aide à former des colonies stables. Plutôt que de basculer entre deux états extrêmes, les cellules cancéreuses occupent fréquemment des états hybrides mêlant caractéristiques sédentaires et mobiles. Ces états intermédiaires semblent particulièrement aptes à survivre au stress et à initier des métastases, ce qui rend important de comprendre non seulement comment la première transition se produit, mais aussi comment et quand elle peut être inversée.
Les signaux qui poussent ou tirent l’identité cellulaire
Les signaux externes issus du microenvironnement tumoral influencent fortement si une cellule se comporte davantage comme une cellule épithéliale ou mésenchymateuse. Des moteurs bien étudiés, tels que le TGFβ et divers facteurs de croissance, favorisent en général l’état mobile et invasif, tandis que d’autres signaux, y compris une famille de protéines appelée BMP, peuvent favoriser le retour vers un état épithélial. À l’intérieur de la cellule, des réseaux de gènes et de petits ARN renforcent l’une ou l’autre identité. Certains facteurs de transcription favorisent la dégradation des jonctions cellulaires et le remodelage de la matrice environnante, tandis qu’un autre groupe de facteurs travaille à restaurer des contacts serrés et un caractère épithélial. Les données expérimentales montrent qu’il n’y a pas de parcours universel à travers ces programmes ; le résultat dépend des signaux présents, de leur durée et du type cellulaire concerné.
Construire une carte logique des décisions cellulaires
Parce que tant de molécules et de boucles de rétroaction interviennent, il est difficile de prédire la réponse d’une cellule cancéreuse dans un contexte donné. Les auteurs ont rassemblé des informations publiées sur les voies clés liées aux deux directions de la transition et les ont organisées en un réseau régulateur. Ils ont ensuite traduit ce réseau en un modèle logique booléen, c’est‑à‑dire marche–arrêt, et exécuté de nombreuses simulations informatiques. Cette approche ne cherche pas à mesurer des quantités moléculaires exactes ; elle explore plutôt quelles combinaisons de signaux et de régulateurs internes conduisent à des motifs stables d’activité génique. Le modèle a produit 25 états à long terme qui se regroupent naturellement en catégories épithéliales, mésenchymateuses, hybrides et naïves, reflétant le spectre observé en laboratoire.
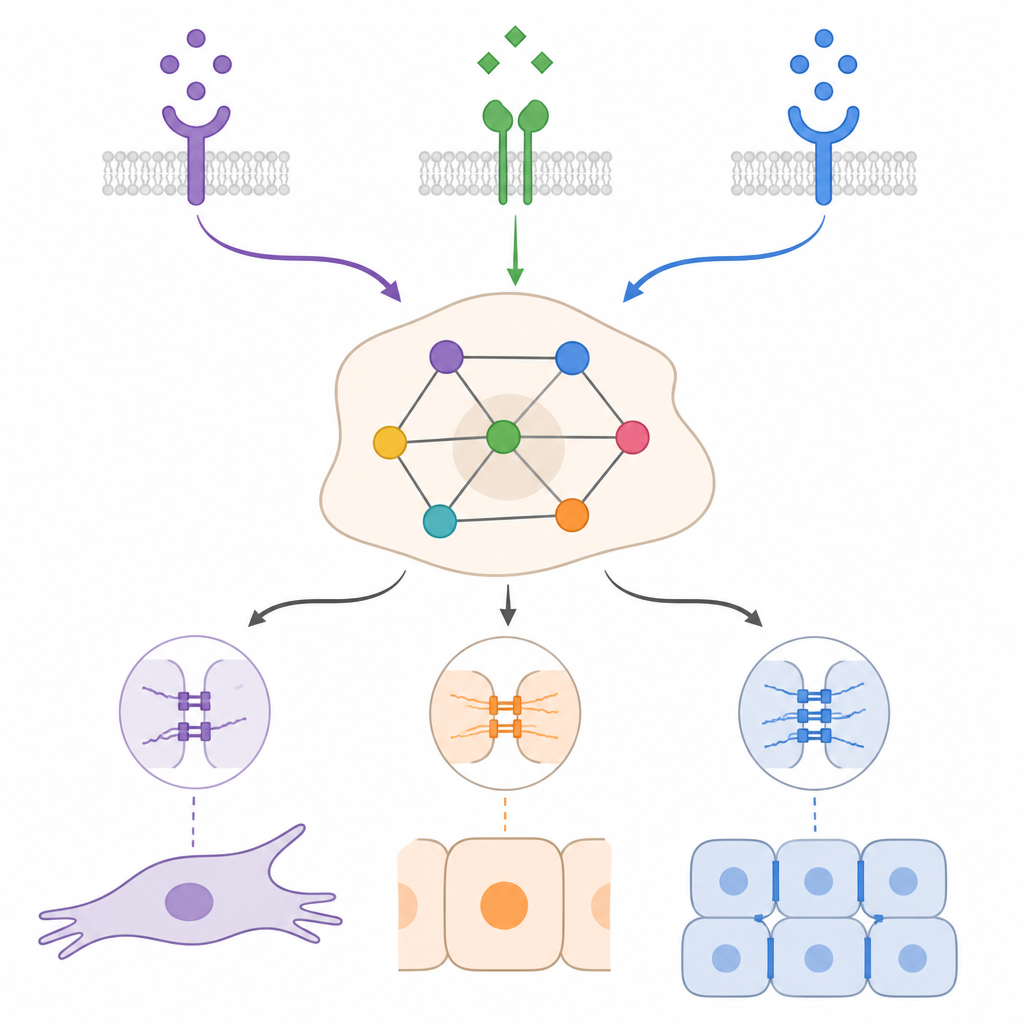
Le contexte détermine jusqu’où les cellules peuvent revenir
En simulant des conditions initiales de type épithélial et mésenchymateux sous différents mélanges de TGFβ, BMP et facteurs de croissance, le modèle a montré qu’un même signal externe peut avoir des effets très différents selon le contexte. Dans de nombreux cas, le BMP a pu affaiblir un programme mésenchymateux piloté par le TGFβ et pousser les cellules vers des états plus épithéliaux ou hybrides, mais s’est souvent arrêté avant un retour complet. Les simulations ont aussi mis en évidence l’importance des boucles de rétroaction auto‑entretenues, dans lesquelles les cellules cancéreuses produisent leur propre TGFβ ou leurs propres facteurs de croissance. Ces boucles peuvent maintenir un état mésenchymateux même après la disparition du signal externe. Rompre des éléments spécifiques de ces boucles, ou renforcer certains régulateurs pro‑épithéliaux, est prédictivement susceptible de faire basculer les cellules vers des états hybrides ou épithéliaux, mais le résultat exact dépend encore une fois de la combinaison de signaux et des conditions de départ.
Ce que cela implique pour la compréhension des métastases
Au total, ce travail suggère que la transition mésenchyme–épithélium dans le cancer n’est pas gouvernée par un interrupteur maître unique, mais par des réseaux de signaux qui se chevauchent et dont l’impact est fortement dépendant du contexte. Certaines molécules semblent capables de pousser les cellules vers un état épithélial seulement dans des circonstances limitées, tandis que d’autres agissent de manière plus large mais laissent souvent les cellules dans des états hybrides conservant des caractères invasifs. Pour les non‑spécialistes, le message principal est que la métastase repose sur des identités cellulaires flexibles, et que les tentatives visant à forcer les cellules à retrouver une forme plus sûre et moins mobile devront tenir compte des nombreuses boucles de rétroaction et des indices environnementaux qui stabilisent ces conditions intermédiaires dangereuses.
Citation: Orozco-Ruiz, S., Ruscone, M., Barillot, E. et al. Mesenchymal to epithelial transition (MET) in cancer progression: insights from logical modeling. Sci Rep 16, 15032 (2026). https://doi.org/10.1038/s41598-026-44905-7
Mots-clés: transition épithéliale mésenchymateuse, métastase cancéreuse, plasticité cellulaire, modélisation logique, protéine morphogénétique osseuse