Clear Sky Science · ar
التحول من الميزنكيمالي إلى الطلائي (MET) في تقدم السرطان: رؤى من النمذجة المنطقية
لماذا يهم تغيّر شكل خلايا السرطان
خلايا السرطان لا تكتفي بالانقسام؛ فهي أيضاً تغير شكلها وسلوكها للانتشار في الجسم. للهروب من الورم، تضعف روابطها مع الخلايا المجاورة وتصبح أكثر حركة. ولتنمية أورام جديدة في مواقع بعيدة، غالباً ما تحتاج إلى استعادة شكلها الأصلي المترابط بإحكام. هذا التأرجح ذهاباً وإياباً، المعروف بليونة الخلايا، يعتبر جوهر عملية الانبثاث. تستخدم الدراسة الملخصة هنا نماذج منطقية قائمة على الحاسوب لفهم كيف تعود الخلايا السرطانية من حالة الحركة إلى حالة أكثر استقراراً، ولماذا يكون هذا الرجوع معتمداً بشدة على الظروف المحيطة.
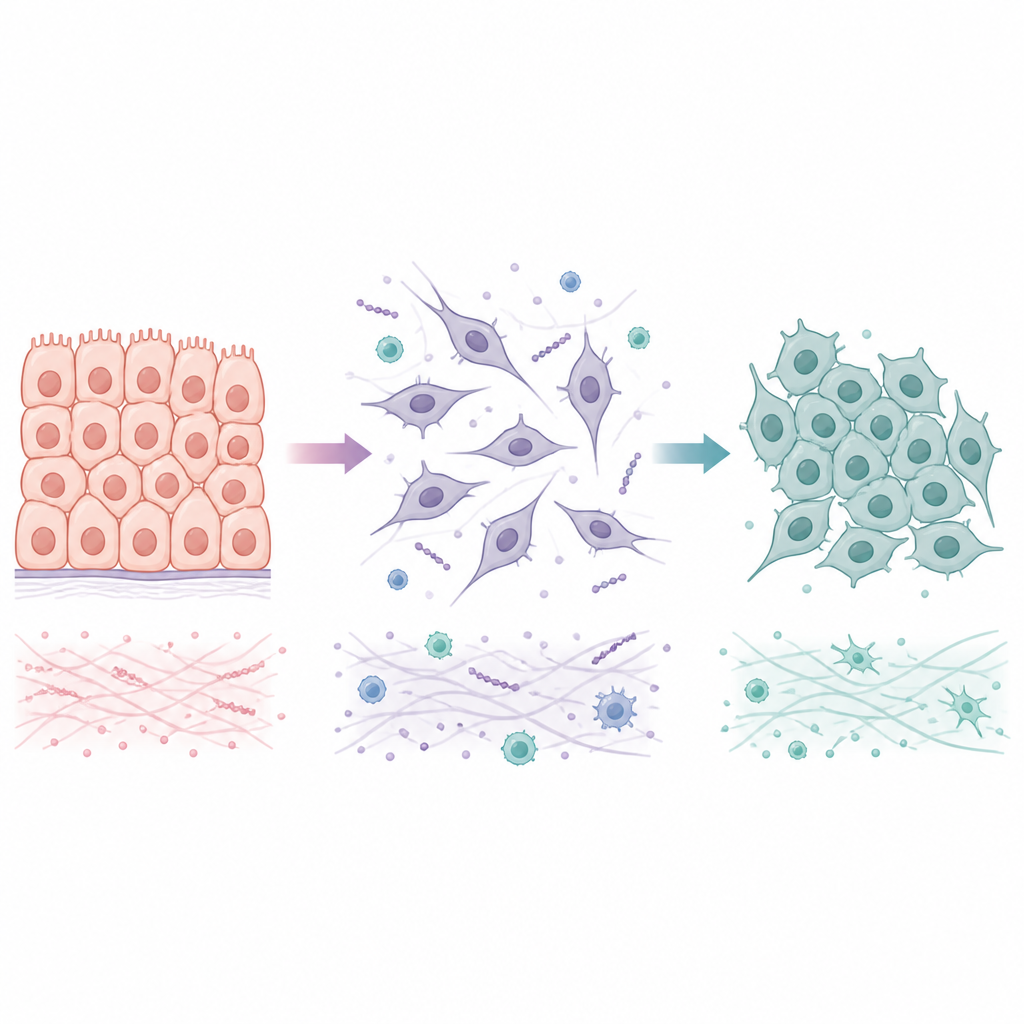
طريقتان تنتقل بهما الخلايا بين الحالات المستقرة والحركية
تبدأ العديد من الأورام كخلايا طلائية، مترابطة في صفوف منظمة. خلال عملية تسمى الانتقال من الطلائي إلى الميزنكيمالي، تفقد هذه الخلايا وصلاتها المحكمة، وتغير شكلها، وتكتسب قدرة على الحركة وغزو الأنسجة والأوعية الدموية المجاورة. عند وصولها إلى عضو جديد، غالباً ما تختبر التحول العكسي، الانتقال من الميزنكيمالي إلى الطلائي، والذي يساعدها على تكوين مستعمرات مستقرة. بدلاً من القفز بين نقطتي نهاية فقط، تشغل خلايا السرطان في كثير من الأحيان حالات هجينة تدمج ميزات الاستقرار والحركة معاً. تبدو هذه الحالات الوسطية جيدة بشكل خاص في تحمل الضغوط وتأسيس الانبثاث، مما يجعل من المهم فهم ليس فقط كيف يحدث الانتقال الأول، بل أيضاً كيف ومتى يمكن عكسه.
الإشارات التي تدفع أو تسحب هوية الخلية السرطانية
الإشارات الخارجية من بيئة الورم تؤثر بشدة على ما إذا كانت الخلية تتصرف بشكل أقرب إلى خلية طلائية أو ميزنكيمالية. المحركات المدروسة جيداً مثل TGFβ وعوامل نمو متعددة تميل إلى تشجيع الجانب الحركي والغزوي، بينما إشارات أخرى، بما في ذلك عائلة البروتينات المعروفة باسم BMP، يمكن أن تفضل العودة نحو الحالة الطلائية. داخل الخلية، تعطي شبكات الجينات والـRNA الصغيرة دعماً لهوية واحدة أو أخرى. عوامل نسخ معينة تعزز تحلل الوصلات الخلوية وإعادة تشكيل المصفوفة المحيطة، بينما تعمل مجموعة أخرى من العوامل على استعادة الاتصالات المحكمة والطابع الطلائي. تظهر الأدلة التجريبية أنه لا يوجد مسار واحد وشامل لهذه البرامج؛ بل إن النتيجة تعتمد على الإشارات الموجودة، ومدتها، ونوع الخلية.
بناء خريطة منطقية للقرارات الخلوية
بما أن العديد من الجزيئات وحلقات التغذية الراجعة متورطة، فصعب التكهن بكيفية استجابة خلية سرطانية في ظرف معين. جمع المؤلفون المعلومات المنشورة حول المسارات الرئيسية المرتبطة باتجاهي الانتقال ونظموها في شبكة تنظيمية. ثم حولوا هذه الشبكة إلى نموذج منطقي ثنائي القيم (تشغيل/إيقاف) وأجروا العديد من المحاكاة الحاسوبية. هذا النهج لا يحاول قياس كميات الجزيئات بدقة؛ بل يستكشف أي تراكيب من الإشارات والمنظمات الداخلية تؤدي إلى أنماط مستقرة من نشاط الجينات. أنتج النموذج 25 حالة طويلة الأمد تجمعت طبيعياً إلى فئات طلائية وميزنكيمالية وهجينة وساذجة، ما يعكس الطيف المرصود في الدراسات المخبرية.
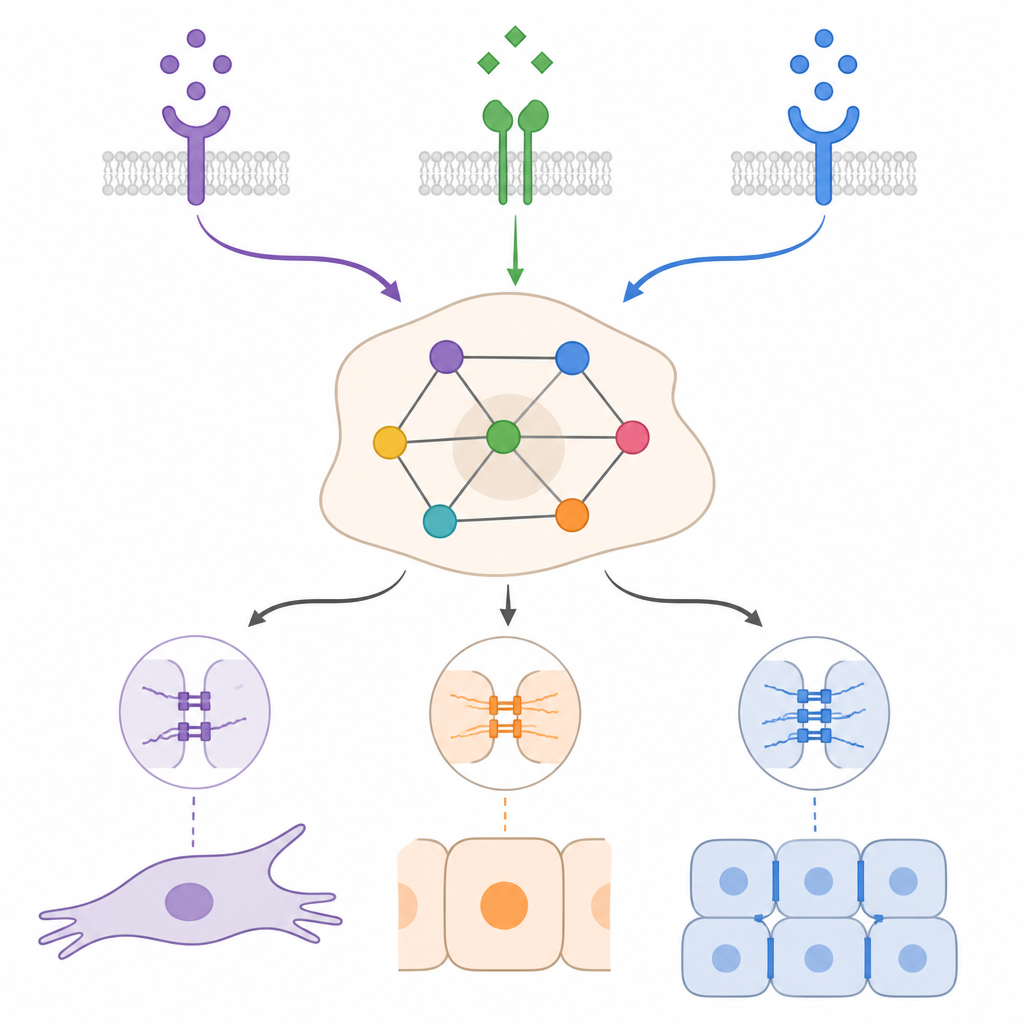
السياق يشكل مدى قدرة الخلايا على الرجوع
من خلال محاكاة شروط بدء تشبه الطلائي والميزنكيمالي تحت مجموعات مختلفة من TGFβ وBMP وعوامل النمو، أظهر النموذج أن نفس الإشارة الخارجية يمكن أن يكون لها تأثيرات مختلفة جداً اعتماداً على السياق. في كثير من الحالات، استطاع BMP إضعاف البرنامج الميزنكيمالي المدفوع بـTGFβ ودفع الخلايا نحو حالات أكثر طلائية أو هجينة، لكنه غالباً ما توقف قبل العودة الكاملة. وأبرزت المحاكاة أيضاً أهمية حلقات التغذية الراجعة المستدامة ذاتياً، حيث تنتج الخلايا السرطانية TGFβ أو إشارات عوامل نمو خاصة بها. يمكن لهذه الحلقات أن تحافظ على حالة ميزنكيمالية حتى بعد زوال التحفيز الخارجي. التنبؤات أشارت إلى أن تعطيل أجزاء محددة من هذه الحلقات، أو تعزيز منظمات مؤيدة للطالائية معينة، قد يحوّل الخلايا نحو حالات هجينة أو طلائية، لكن النتيجة الدقيقة اعتمدت مرة أخرى على مزيج الإشارات وظروف البداية.
ما الذي يعنيه ذلك لفهم الانبثاث
بشكل عام، تشير الدراسة إلى أن الانتقال من الميزنكيمالي إلى الطلائي في السرطان لا يتحكم به مفتاح رئيسي واحد، بل بشبكات متداخلة من الإشارات يكون تأثيرها معتمداً بدرجة عالية على السياق. تبدو بعض الجزيئات قادرة على دفع الخلايا نحو حالة تشبه الطلائية فقط في ظروف ضيقة، بينما تعمل أخرى على نطاق أوسع لكنها غالباً ما تترك الخلايا في حالات هجينة تحتفظ بصفات غازية. للقراء غير المتخصصين، الرسالة الأساسية هي أن الانبثاث يعتمد على هويات خلوية مرنة، وأن محاولات إجبار الخلايا على العودة لشكل أكثر أماناً وأقل حركة ستحتاج إلى أخذ حلقات التغذية الراجعة والإشارات البيئية العديدة التي تثبت هذه الحالات الوسطية الخطرة في الاعتبار.
الاستشهاد: Orozco-Ruiz, S., Ruscone, M., Barillot, E. et al. Mesenchymal to epithelial transition (MET) in cancer progression: insights from logical modeling. Sci Rep 16, 15032 (2026). https://doi.org/10.1038/s41598-026-44905-7
الكلمات المفتاحية: التحول الطلائي الميزنكيمالي, انبثاث السرطان, ليونة الخلايا, النمذجة المنطقية, بروتينات نمو العظم (BMP)