Clear Sky Science · ru
Переход от мезенхимального к эпителиальному состоянию (MET) в прогрессии рака: выводы логического моделирования
Почему важно, что раковые клетки меняют форму
Раковые клетки не только делятся; они также меняют форму и поведение, чтобы распространиться по организму. Чтобы покинуть опухоль, они ослабевают связи с соседями и становятся более подвижными. Чтобы вырастить новые опухоли в других местах, им часто нужно восстановить исходную, плотно связанную форму. Это движение туда и обратно, называемое клеточной пластичностью, лежит в основе метастазирования. В изложенном здесь исследовании используются компьютерные логические модели, чтобы понять, как раковые клетки переключаются обратно от подвижного к более осевшемуся состоянию и почему это обращение так сильно зависит от окружающих условий.
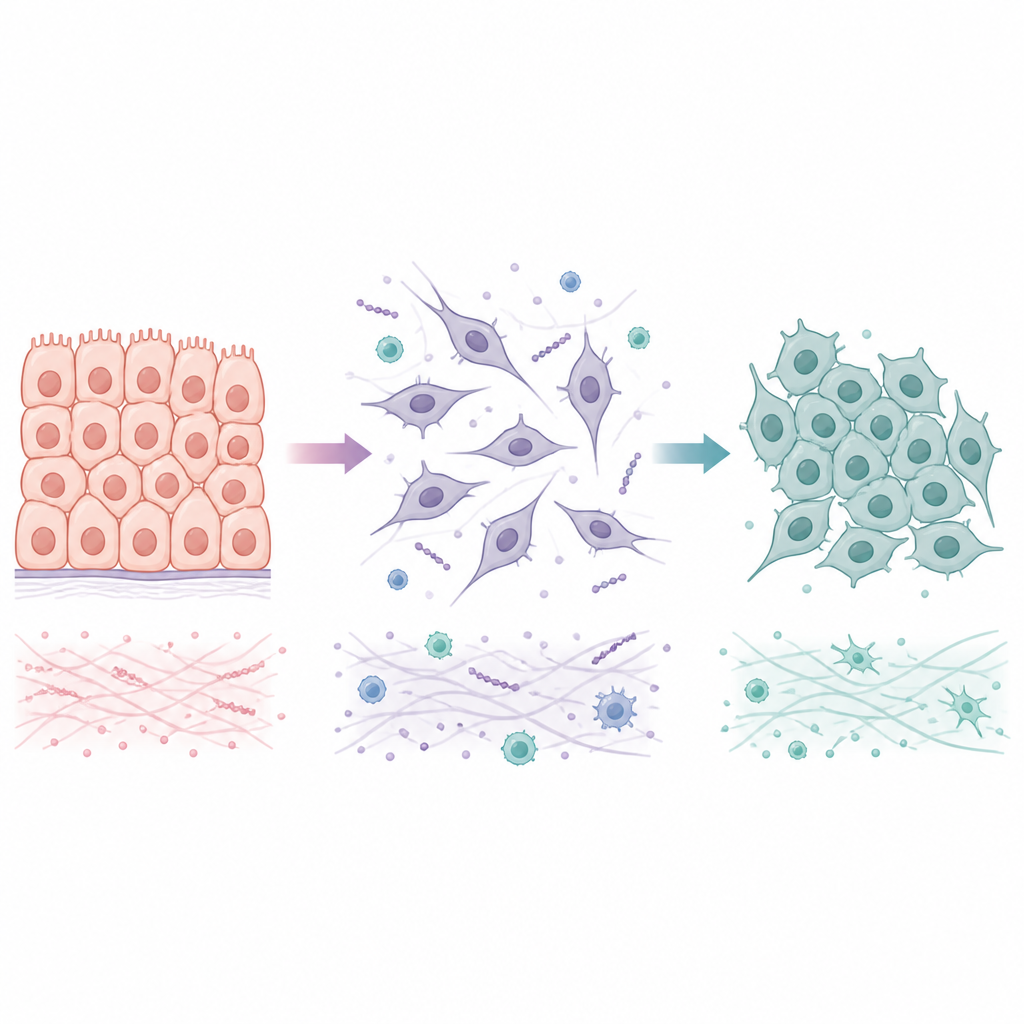
Два способа, которыми клетки переходят между осевшим и подвижным состоянием
Многие опухоли начинаются как эпителиальные ткани, где клетки плотно связаны в упорядоченные пласты. В процессе, называемом эпителиально-мезенхимальным переходом, эти клетки теряют плотные контакты, меняют форму и приобретают способность передвигаться и вторгаться в окружающие ткани и сосуды. При попадании в новый орган они часто проходят обратный сдвиг — мезенхимально-эпителиальный переход — что помогает им образовывать стабильные колонии. Вместо простого переключения между двумя крайностями, раковые клетки часто занимают гибридные состояния, сочетающие признаки осевших и подвижных форм. Эти промежуточные состояния, по-видимому, особенно устойчивы к стрессу и эффективны при посеве метастазов, поэтому важно понимать не только то, как происходит первоначальный переход, но и как и когда он может быть обращён.
Сигналы, которые «тянут» или «толкают» клеточную идентичность
Внешние сигналы из опухолевой микроокружения сильно влияют на то, будет ли клетка вести себя больше как эпителиальная или как мезенхимальная. Хорошо изученные драйверы, такие как TGFβ и различные факторы роста, склоняют систему в сторону подвижности и инвазивности, тогда как другие сигналы, включая семейство белков BMP, могут способствовать возвращению к эпителиальному состоянию. Внутри клетки сети генов и малых РНК закрепляют одну или другую идентичность. Одни транскрипционные факторы способствуют разрушению клеточных контактов и ремоделированию внеклеточного матрикса, тогда как другая группа факторов работает на восстановление плотных контактов и эпителиальных характеристик. Экспериментальные данные показывают, что нет единого универсального пути через эти программы; итог зависит от того, какие сигналы присутствуют, как долго они действуют и в каком типе клеток.
Построение логической карты клеточных решений
Поскольку вовлечено множество молекул и петлей обратной связи, трудно предсказать, как раковая клетка отреагирует в конкретных условиях. Авторы собрали опубликованные данные о ключевых путях, связанных с обоими направлениями перехода, и организовали их в регуляторную сеть. Затем они перевели эту сеть в булеву, то есть «вкл–выкл», логическую модель и провели множество компьютерных симуляций. Этот подход не пытается измерять точные количества молекул; он исследует, какие сочетания внешних сигналов и внутренних регуляторов приводят к устойчивым паттернам активности генов. Модель выделила 25 долгосрочных состояний, которые естественно группировались в эпителиальные, мезенхимальные, гибридные и наивные категории, отражая спектр, наблюдаемый в лабораторных исследованиях.
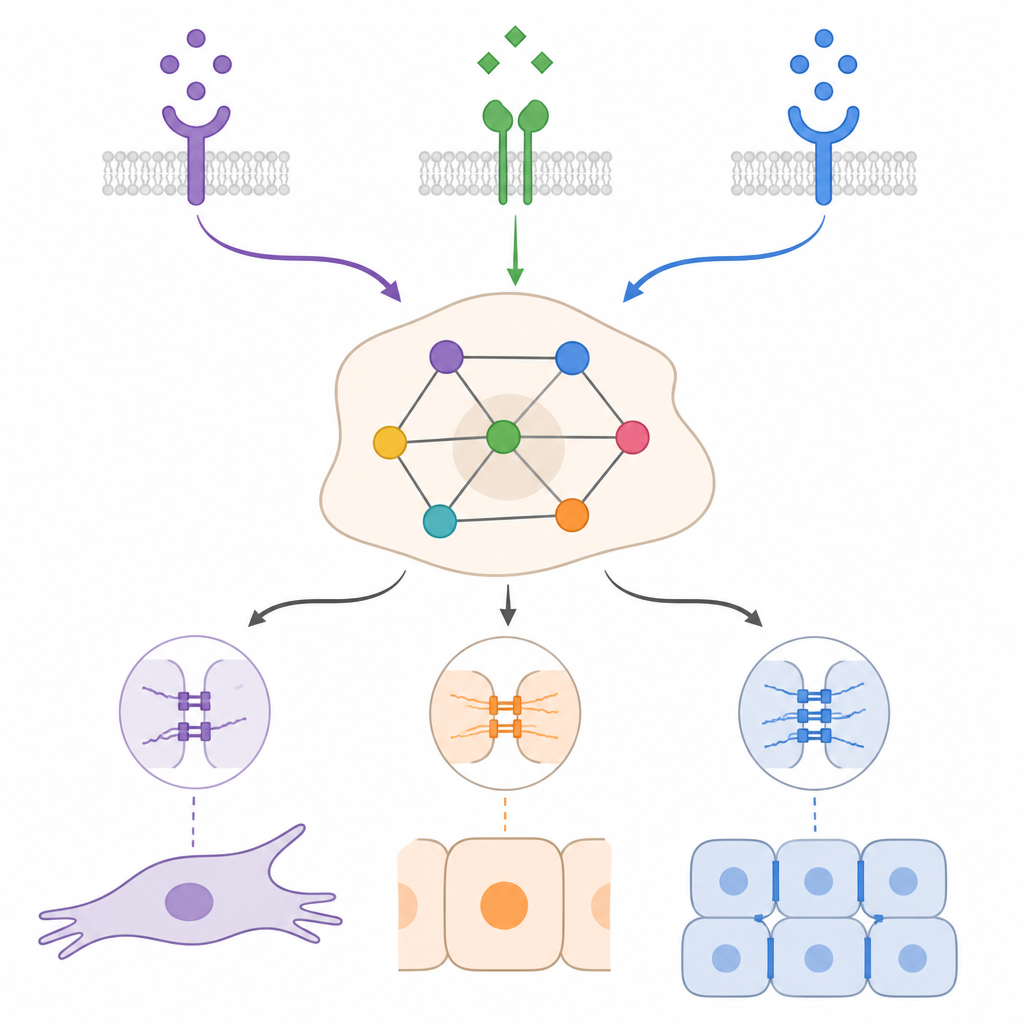
Контекст определяет, насколько далеко клетки могут вернуться
Моделируя начальные эпителиально-подобные и мезенхимально-подобные условия при разных сочетаниях TGFβ, BMP и факторов роста, модель показала, что один и тот же внешний сигнал может давать очень разные эффекты в зависимости от контекста. Во многих случаях BMP ослаблял TGFβ-опосредованную мезенхимальную программу и сдвигал клетки в сторону более эпителиальных или гибридных состояний, но часто не доводил до полного возврата. Симуляции также подчеркнули важность самоподдерживающихся петлей обратной связи, при которых клетки продуцируют собственный TGFβ или факторы роста. Эти петли могут сохранять мезенхимальное состояние даже после исчезновения внешней стимуляции. Предсказано, что разрушение конкретных звеньев таких петель или усиление определённых проэпителиальных регуляторов может сдвинуть клетки в гибридные или эпителиальные состояния, но точный исход снова зависел от комбинации сигналов и исходных условий.
Что это значит для понимания метастазирования
В целом работа указывает на то, что мезенхимально-эпителиальный переход при раке не управляется единственным главным переключателем, а перекрывающимися сетями сигналов, влияние которых сильно зависит от контекста. Некоторые молекулы способны подтолкнуть клетки обратно к эпителиально-подобному состоянию лишь в узких обстоятельствах, тогда как другие действуют шире, но часто всё же оставляют клетки в гибридных состояниях с сохраняющимися инвазивными чертами. Для неспециалиста главный вывод таков: метастазирование опирается на гибкую клеточную идентичность, и попытки принудительно вернуть клетки в более безопасную, менее подвижную форму должны учитывать многочисленные петли обратной связи и сигналы окружающей среды, которые стабилизируют эти опасные промежуточные состояния.
Цитирование: Orozco-Ruiz, S., Ruscone, M., Barillot, E. et al. Mesenchymal to epithelial transition (MET) in cancer progression: insights from logical modeling. Sci Rep 16, 15032 (2026). https://doi.org/10.1038/s41598-026-44905-7
Ключевые слова: эпителиально-мезенхимальный переход, метастазирование рака, пластичность клеток, логическое моделирование, белок морфогенетического семейства костей