Clear Sky Science · de
Mesenchymale-zu-epitheliale Transition (MET) im Verlauf von Krebs: Erkenntnisse aus logischem Modellieren
Warum die Formveränderung von Krebszellen Bedeutung hat
Krebszellen teilen sich nicht nur; sie verändern auch Form und Verhalten, um sich im Körper auszubreiten. Um einem Tumor zu entkommen, lockern sie ihre Verbindungen zu Nachbarzellen und werden beweglicher. Um an anderen Stellen neue Tumoren zu bilden, müssen sie oft ihre ursprüngliche, eng vernetzte Gestalt wiedererlangen. Dieses Hin und Her, bekannt als zelluläre Plastizität, steht im Zentrum der Metastasierung. Die hier zusammengefasste Studie nutzt rechnerische logische Modelle, um zu verstehen, wie Krebszellen von einem mobilen wieder in einen sesshafteren Zustand zurückschalten und warum diese Umkehr so stark von den Umgebungsbedingungen abhängt.
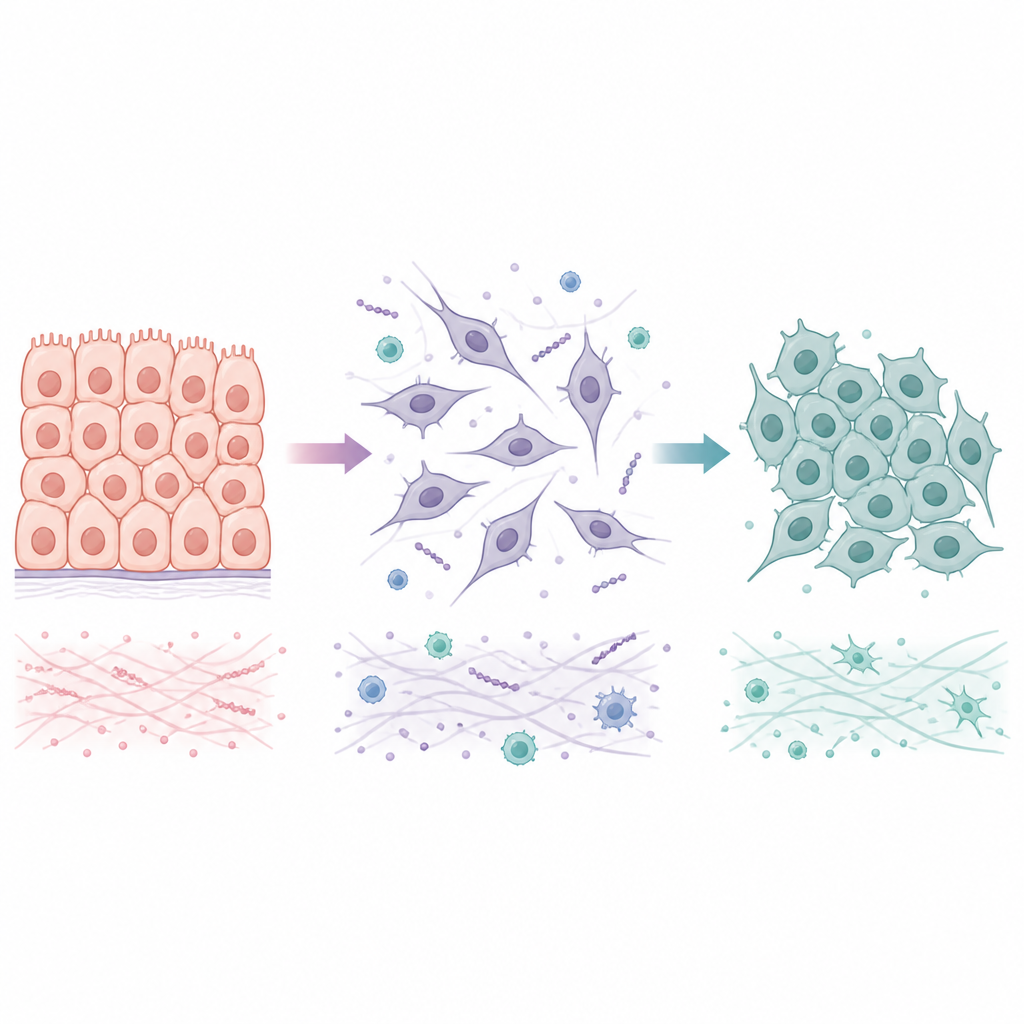
Zwei Wege, wie Zellen zwischen sessilem und mobilem Zustand wechseln
Viele Tumoren entstehen aus epithelialen Zellen, die fest in geordneten Schichten verbunden sind. Während eines Prozesses, der als epitheliale-zu-mesenchymale Transition bezeichnet wird, verlieren diese Zellen ihre engen Verbindungen, ändern ihre Gestalt und gewinnen die Fähigkeit, sich zu bewegen und in umliegendes Gewebe sowie Blutgefäße einzudringen. Wenn sie ein neues Organ erreichen, durchlaufen sie häufig die umgekehrte Verschiebung, die mesenchymal-zu-epitheliale Transition, die ihnen hilft, stabile Kolonien zu bilden. Statt einfach nur zwischen zwei Endpunkten umzuschalten, besetzen Krebszellen häufig hybride Zustände, die sessile und mobile Merkmale mischen. Diese Zwischenzustände scheinen besonders widerstandsfähig gegenüber Belastungen und geeignet zur Aussaat von Metastasen zu sein, weshalb es wichtig ist zu verstehen, nicht nur wie die erste Transition abläuft, sondern auch wie und wann sie rückgängig gemacht werden kann.
Signale, die die Identität von Krebszellen beeinflussen
Externe Signale aus der Tumorumgebung beeinflussen stark, ob sich eine Zelle eher epithelial oder mesenchymal verhält. Gut untersuchte Treiber wie TGFβ und verschiedene Wachstumsfaktoren fördern oft die mobile, invasive Richtung, während andere Signale, darunter eine Proteinfamilie namens BMP, eine Rückkehr zu einem epithelialen Zustand begünstigen können. Im Inneren der Zelle verstärken Netzwerke aus Genen und kleinen RNAs jeweils die eine oder andere Identität. Bestimmte Transkriptionsfaktoren fördern den Abbau von Zellverbindungen und die Umgestaltung der umgebenden Matrix, während eine andere Gruppe von Faktoren daran arbeitet, enge Kontakte und einen epithelialen Charakter wiederherzustellen. Experimentelle Befunde zeigen, dass es keinen einzigen, universellen Weg durch diese Programme gibt; das Ergebnis hängt vielmehr davon ab, welche Signale vorhanden sind, wie lange und in welchem Zelltyp.
Aufbau einer logischen Landkarte zellulärer Entscheidungen
Weil so viele Moleküle und Rückkopplungsschleifen beteiligt sind, ist es schwer vorherzusagen, wie eine Krebszelle in einer bestimmten Situation reagieren wird. Die Autoren sammelten veröffentlichte Informationen zu Schlüsselwegen, die mit beiden Richtungen der Transition verbunden sind, und organisierten sie zu einem Regulationsnetzwerk. Sie übersetzten dieses Netzwerk dann in ein Boolesches, also ein Ein–Aus-Logikmodell, und führten zahlreiche Computersimulationen durch. Dieser Ansatz versucht nicht, exakte Molekülmengen zu messen; vielmehr untersucht er, welche Kombinationen von Signalen und internen Regulatoren zu stabilen Mustern der Genaktivität führen. Das Modell erzeugte 25 langfristige Zustände, die sich naturgemäß in epithelial-, mesenchymal-, hybride und naive Kategorien gruppierten und das im Labor beobachtete Spektrum widerspiegeln.
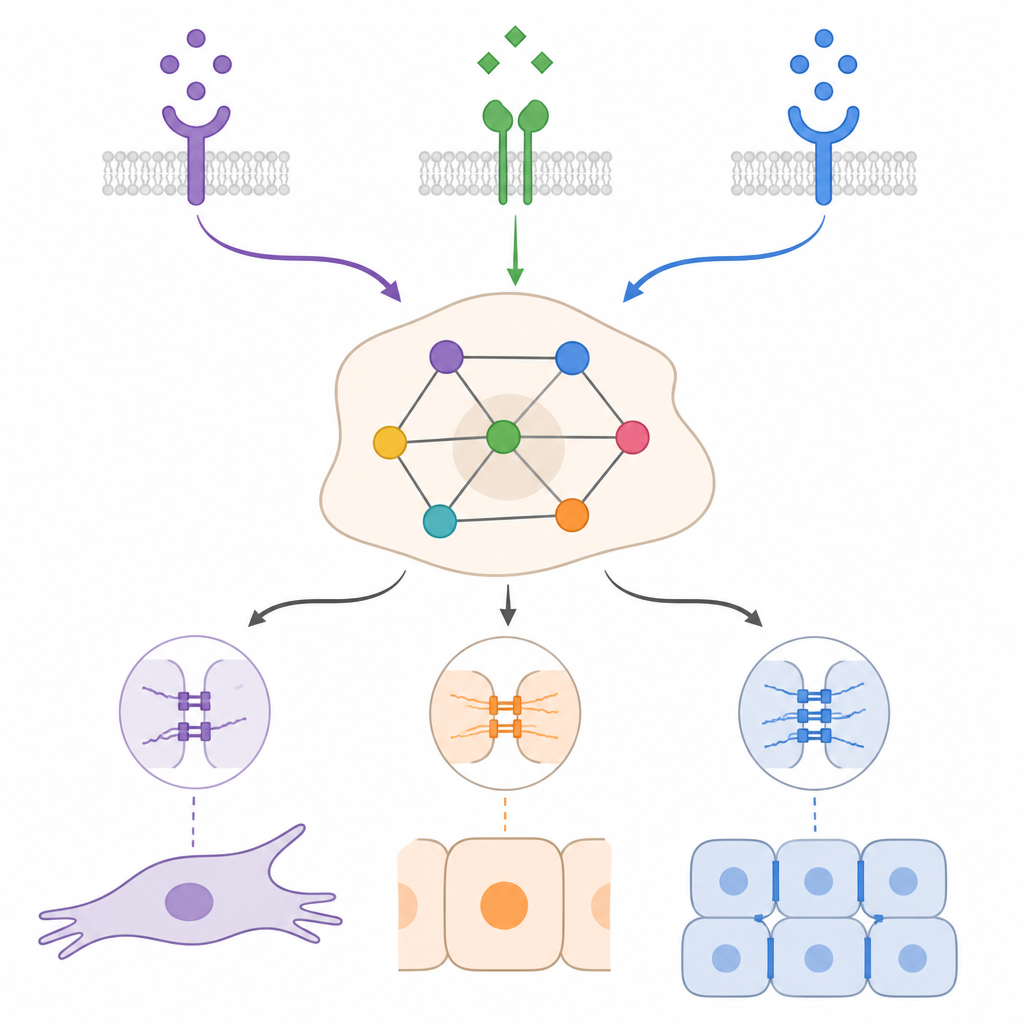
Der Kontext bestimmt, wie weit Zellen zurückkehren können
Durch Simulation von epithelial-ähnlichen und mesenchymal-ähnlichen Ausgangszuständen unter verschiedenen Mischungen von TGFβ, BMP und Wachstumsfaktoren zeigte das Modell, dass derselbe externe Reiz je nach Kontext sehr unterschiedliche Effekte haben kann. In vielen Fällen konnte BMP ein TGFβ-gesteuertes mesenchymales Programm abschwächen und Zellen in Richtung epithelialer oder hybrider Zustände drängen, erreichte aber oft nicht die vollständige Rückkehr. Die Simulationen betonten außerdem die Bedeutung selbstunterhaltender Rückkopplungsschleifen, in denen Krebszellen ihr eigenes TGFβ- oder Wachstumsfaktorsignal produzieren. Diese Schleifen können einen mesenchymalen Zustand aufrechterhalten, selbst nachdem die äußere Stimulation verschwunden ist. Das gezielte Unterbrechen bestimmter Teile dieser Schleifen oder die Verstärkung bestimmter pro-epithelialer Regulatoren wurde vorhergesagt, Zellen in hybride oder epitheliale Zustände zu verschieben, doch das genaue Ergebnis hing erneut von der Kombination der Signale und den Ausgangsbedingungen ab.
Was das für das Verständnis von Metastasen bedeutet
Insgesamt legt die Arbeit nahe, dass die mesenchymal-zu-epitheliale Transition bei Krebs nicht durch einen einzelnen Hauptschalter gesteuert wird, sondern durch überlappende Signalnetzwerke, deren Wirkung stark kontextabhängig ist. Einige Moleküle scheinen Zellen nur unter engen Bedingungen in Richtung eines epithelial-ähnlichen Zustands zu schubsen, während andere breiter wirken, aber häufig Zellen in hybriden Zuständen zurücklassen, die invasive Eigenschaften behalten. Für Nichtfachleute ist die Kernbotschaft, dass Metastasierung auf flexiblen Zellidentitäten beruht und dass Versuche, Zellen zurück in eine sicherere, weniger mobile Form zu drängen, die vielen Rückkopplungsschleifen und Umweltreize berücksichtigen müssen, die diese gefährlichen Zwischenzustände stabilisieren.
Zitation: Orozco-Ruiz, S., Ruscone, M., Barillot, E. et al. Mesenchymal to epithelial transition (MET) in cancer progression: insights from logical modeling. Sci Rep 16, 15032 (2026). https://doi.org/10.1038/s41598-026-44905-7
Schlüsselwörter: epitheliale mesenchymale Transition, Krebsmetastase, Zellplastizität, logisches Modellieren, Knochenmorphogenetisches Protein