Clear Sky Science · zh
线虫α-螺旋抗菌肽中非结构化、二硫键环化的C端增强并调节其活性
为何微小的寄生虫分子重要
随着抗生素耐药性的上升,研究人员正在寻找新的方法杀死危险细菌而不损伤我们自身细胞。一个有前景的来源是抗菌肽——许多生物用作天然抗生素的短蛋白片段。本研究考察了一种来自寄生扁形虫的非典型肽,并展示了末端一个小而松弛的尾部通过化学键束缚起来,如何微调肽杀死细菌的速度与力度。理解这个内建的控制旋钮可能帮助科学家设计更聪明、更精准的抗生素替代品。
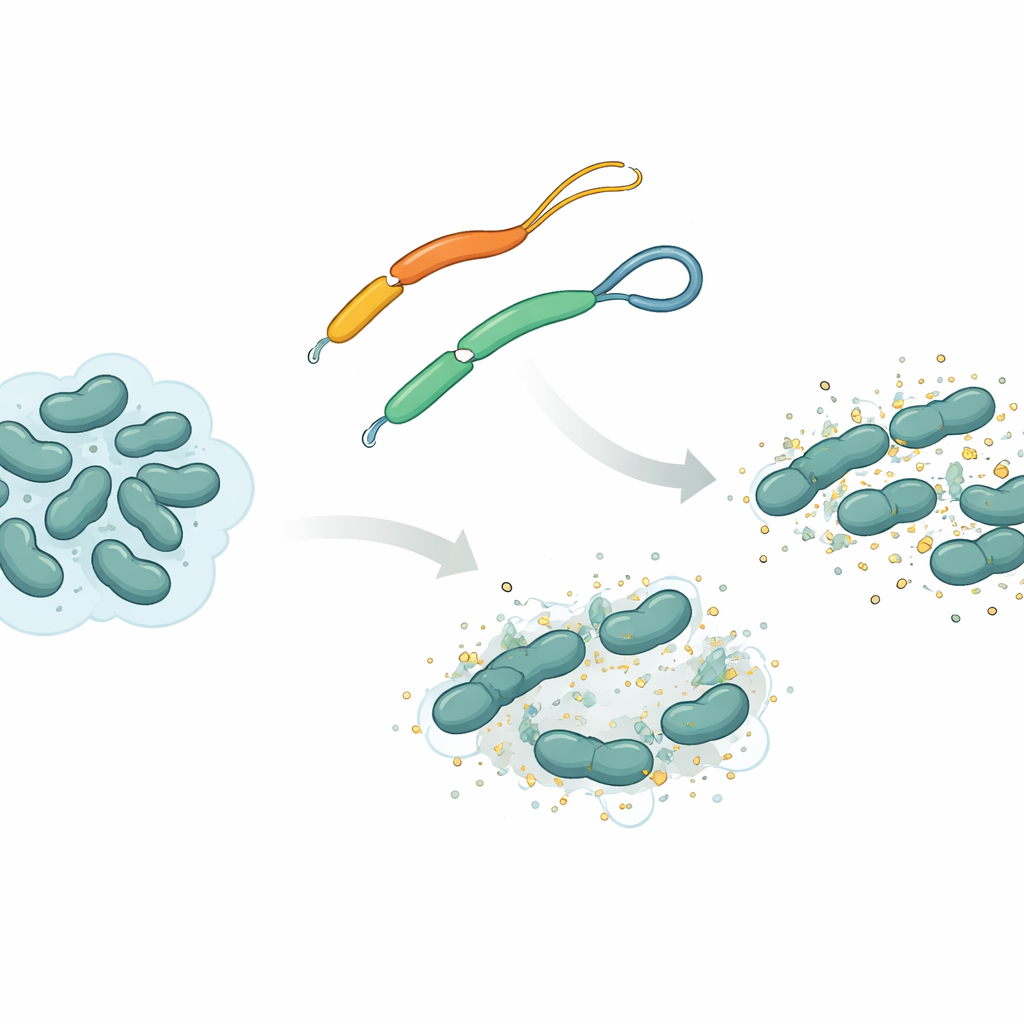
来自扁形虫的天然武器
研究团队聚焦一种名为 mesco-2 的抗菌肽,该肽存在于扁形虫 Mesocestoides corti 中。像许多此类肽一样,mesco-2 有一个刚性、螺旋状的“前段”,与细菌膜相互作用,以及一个较松散的“尾段”。在这个尾段中,两个含硫构件通过称为二硫键的化学纽带相连,形成一个小环。研究者将 mesco-2 与一个几乎相同的变体 mesco-2A 进行了比较,后者去除了该二硫键,使尾端完全开放。这个微小改变并未大幅改变整体化学成分,但改变了肽的可动性以及其攻击细菌时的行为模式。
寄生虫防御中的隐含模式
在深入研究 mesco-2 之前,科学家搜索了大量来自扁形虫及其他多种生物的预测抗菌肽数据库。他们寻找特定模式,即两个含硫单位(半胱氨酸)在分子末端相隔若干位的情况。他们发现“CXXXC”模式——与 mesco-2 中的间距相同——在扁形虫肽中出乎意料地常见,并且常位于柔性的末端片段而非有序区域。若干此类肽的计算机生成三维模型显示,这些富含半胱氨酸的基序通常位于松软的尾部,表明自然界有意将这些小环置于可移动的区域,以便调节肽的行为。
一个小环如何影响运动与协作
研究者使用分子动力学模拟来建模 mesco-2 与 mesco-2A 在简化细菌膜附近的运动。两种版本都迅速附着到膜表面,受肽上的正电荷与细菌脂质的负电荷之间的吸引力驱动。但 mesco-2 中的环状尾段促使中心螺旋区在特定位置弯曲并采用有利于部分插入膜内的取向。它还鼓励若干 mesco-2 分子聚集成小簇,特别是当它们的尾端相互靠近时,这些簇在结合膜时保持在一起。相比之下,开放尾端的 mesco-2A 在末端结构上更具柔性,不易聚集,且更倾向以单个分子而非协调组合作为表面结合者。
从结构到细菌杀伤
实验室实验证实了计算模型的结论。当这些肽与简单的膜模拟物混合时,两者在疏油或类洗涤剂环境中都会改变形状,这符合膜靶向分子的预期行为。然而,在带负电、类细菌膜上,mesco-2 更容易获得有规则的螺旋结构,并呈现与 mesco-2A 不同的构象。在对多种细菌的测试中,两种肽在总体效力上都显示出强抗菌效果。重要差异出现在未达到完全杀灭剂量以下的水平:mesco-2 即使在低浓度下也能在数小时内抑制或停止细菌生长,而暴露于开放尾 mesco-2A 的细菌恢复得更快。对膜损伤的时间分辨测量显示,mesco-2 更快地在细菌膜上打出孔洞,而 mesco-2A 除非以更高剂量使用,否则作用较慢。高分辨成像揭示了不同的表面损伤模式,再次暗示两种版本扰动细菌包膜的方式不同。关键是,在杀菌水平下,两种肽对人体免疫细胞模型的损伤都很低,表明具有良好的安全边际。
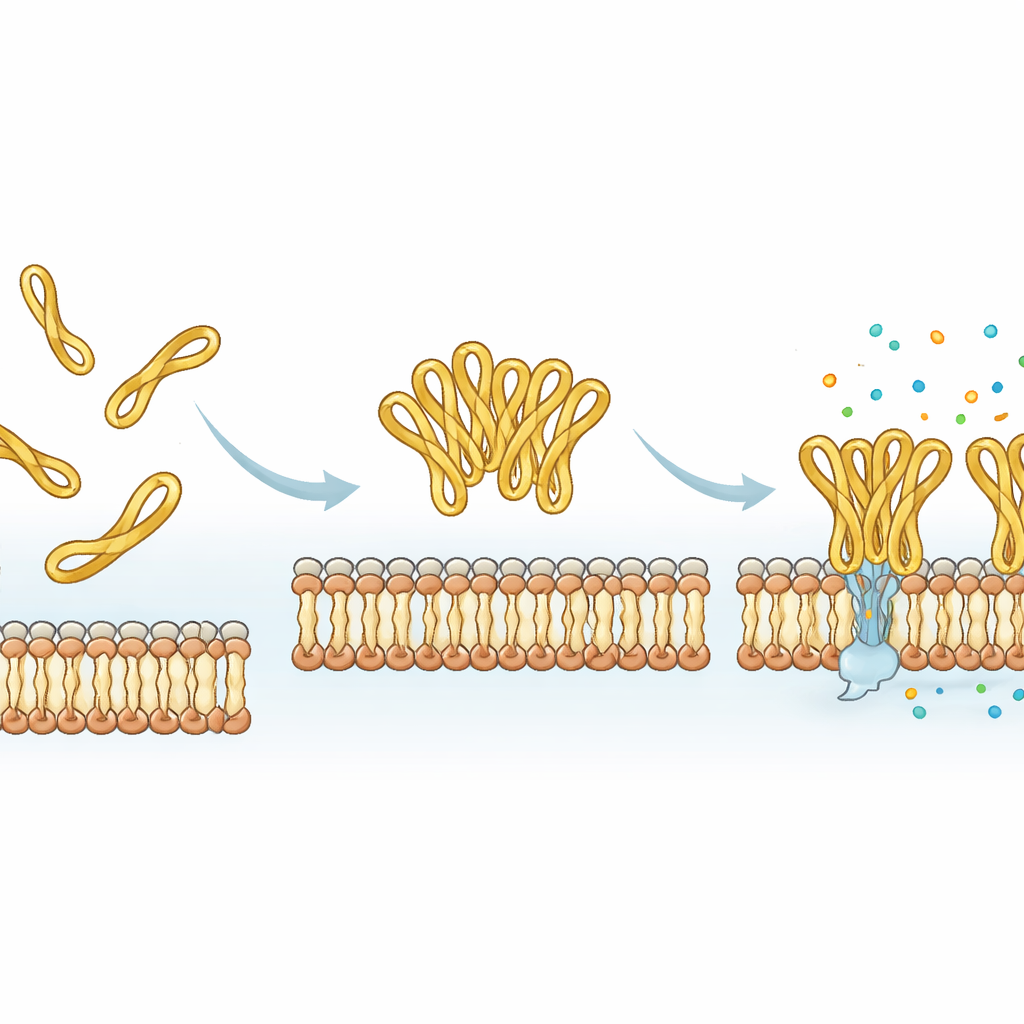
用于调节肽类药物的内建旋钮
综合所有证据,该研究表明,mesco-2 末端由二硫键连接的小尾段充当一种分子旋钮:它稳定了一种特定的弯曲构象,促使肽以簇状协同工作,并加速膜的破坏,而不会大幅增加对人细胞的损害。去除该小环可使合成更容易,甚至可能增加粘附到模型膜的分子数量,但会放慢实际杀灭过程并改变膜的损伤方式。对于基于此类肽的未来类抗生素药物而言,这意味着看似微小、柔性的末端片段——而不仅仅是主要的螺旋核心——可以被有意调整,以控制肽攻击细菌的速度、强度与协同性。
引用: Budimir, A., Stojan, I., Primorac, K. et al. Unstructured, disulfide-bridged C-terminus in helminth α-helical antimicrobial peptides enhances and modulates their activity. Sci Rep 16, 14472 (2026). https://doi.org/10.1038/s41598-026-44795-9
关键词: 抗菌肽, 扁形虫肽, 二硫键, 膜破坏, 抗生素耐药性