Clear Sky Science · ja
線虫α-ヘリカル抗菌ペプチドの非整列でジスルフィド結合されたC末端はその活性を増強し調節する
なぜ小さな寄生虫分子が重要か
抗生物質耐性が高まる中で、研究者たちは自分たちの細胞を傷つけずに有害な細菌を殺す新たな方法を探しています。有望な供給源の一つが抗菌ペプチド――多くの生物が天然の抗生物質として用いる短いタンパク質断片です。本研究は寄生性扁形動物由来の珍しいペプチドを調べ、その一端にある小さく柔らかい尾部が化学結合で束ねられていることが、ペプチドの殺菌速度や作用の強さを微調整する仕組みを示しています。この組み込まれた調整ノブを理解すれば、より賢く精密な抗生物質代替の設計に役立つ可能性があります。
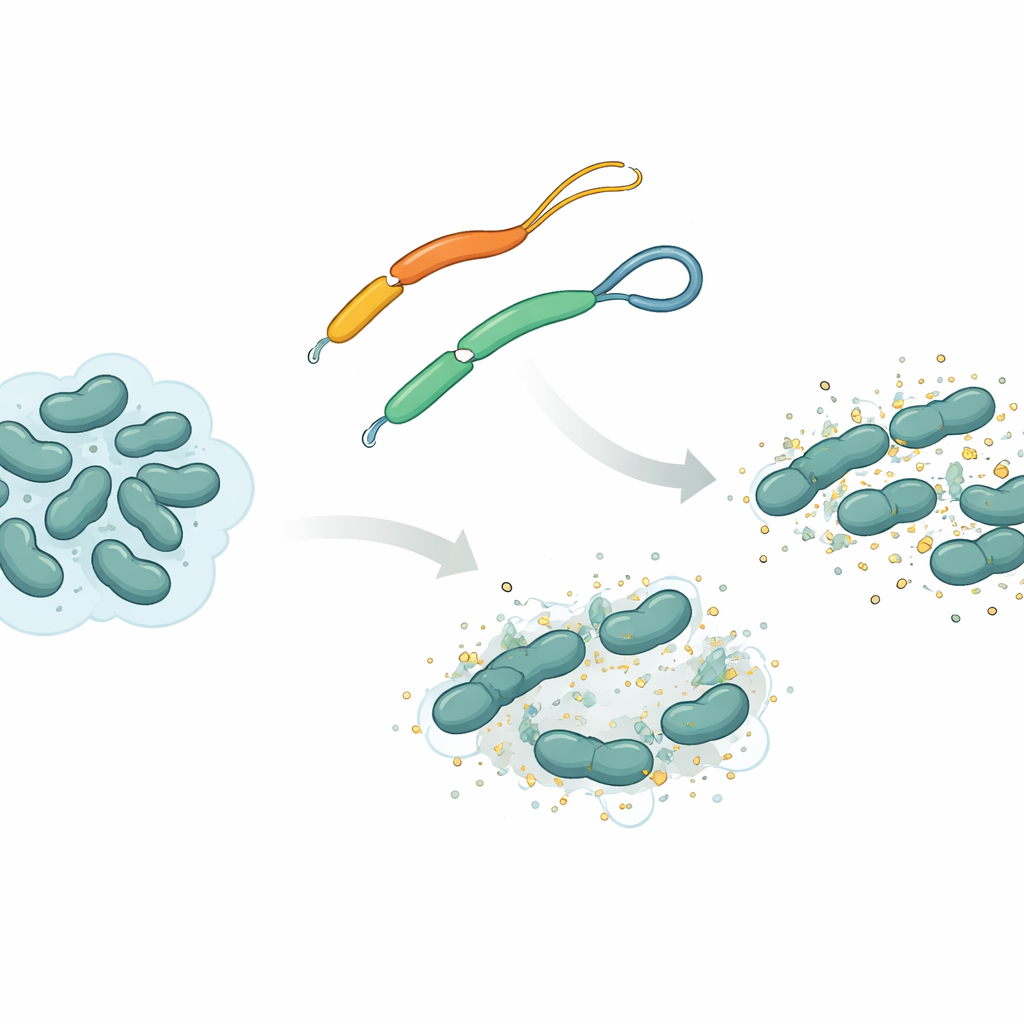
扁形動物が持つ自然の武器
研究チームは扁形動物 Mesocestoides corti に見られる抗菌ペプチド mesco-2 に注目しました。多くのこうしたペプチドと同様に、mesco-2 は細菌膜と相互作用する剛直ならせん状の「前部」と、よりゆるい「尾部」を持ちます。尾部では2つの硫黄含有残基がジスルフィド結合という化学的な結びつきでつながり、小さなループを形成しています。研究者たちはこのジスルフィドを除去して尾部を完全に開いた状態にしたほぼ同一の変異体 mesco-2A と比較しました。この小さな変更は全体の化学組成を大きく変えないものの、ペプチドの運動性や細菌攻撃時の振る舞いを変えます。
寄生虫防御に隠れたパターン
mesco-2 自身を詳しく見る前に、研究者たちは扁形動物や他の多くの生物から予測された抗菌ペプチドの大規模データベースを検索しました。分子末端近くで2つのシステイン(硫黄含有ユニット)がいくつかの残基を挟んで並ぶ特定のパターンを探したのです。彼らは mesco-2 と同じ間隔を持つ「CXXXC」パターンが扁形動物ペプチドに意外と多く見られ、その多くが秩序だった領域ではなく柔軟な末端セグメントに位置していることを発見しました。いくつかのペプチドについてコンピュータ生成の3Dモデルを作ると、これらのシステイン豊富モチーフは通常しなやかな尾部に存在し、自然はこれらのループを可動領域に配置してペプチドの振る舞いを調節していることが示唆されました。
小さなループが運動性と協同性を形作る仕組み
分子動力学シミュレーションを用いて、研究者たちは単純化した細菌膜近傍での mesco-2 と mesco-2A の動きをモデル化しました。両バージョンとも正電荷を持つペプチドと負に帯電した細菌脂質間の引力によって膜表面に素早く付着します。しかし mesco-2 のループ化した尾部は、中心のらせん領域が特定の箇所で曲がり膜に部分的に挿入されやすい配向をとるのを助けます。また、尾部が近くにあるときに複数の mesco-2 分子が小さなクラスターに集まりやすく、これらの集合体は膜に結合する際にまとまって維持されます。対照的に、尾部が開いた mesco-2A は末端がより柔軟でクラスターを形成しにくく、個々の分子として表面にとどまる傾向が強く、協調的な集団行動は控えめです。
構造から細菌殺菌まで
実験室での実験は計算モデルを裏付けました。ペプチドを単純な膜模倣物と混ぜると、両者とも脂質性や界面活性剤様の環境で形を変え、膜標的分子として期待される挙動を示しました。しかし mesco-2 はらせん構造をより容易に獲得し、負に帯電した細菌様膜上で mesco-2A とは異なる形態をとりました。いくつかの細菌種に対する試験では、両ペプチドは全体的な効力は似ているものの強い抗菌効果を示しました。重要な差は完全に殺菌する用量以下で現れました。mesco-2 は低濃度でも何時間にもわたり細菌の増殖を遅らせたり止めたりしましたが、開いた尾部の mesco-2A に曝露された細菌はより早く回復しました。膜損傷の時間分解測定では、mesco-2 が細菌膜に穴を開けるのがずっと速く、mesco-2A は高用量でないとより遅い作用を示しました。高解像度イメージングは表面損傷の異なるパターンを明らかにし、両者が細菌被膜を乱す方法が異なることを示唆しました。重要な点として、両ペプチドとも殺菌レベルでヒト免疫細胞モデルへの損傷は低く、有利な安全マージンが示されました。
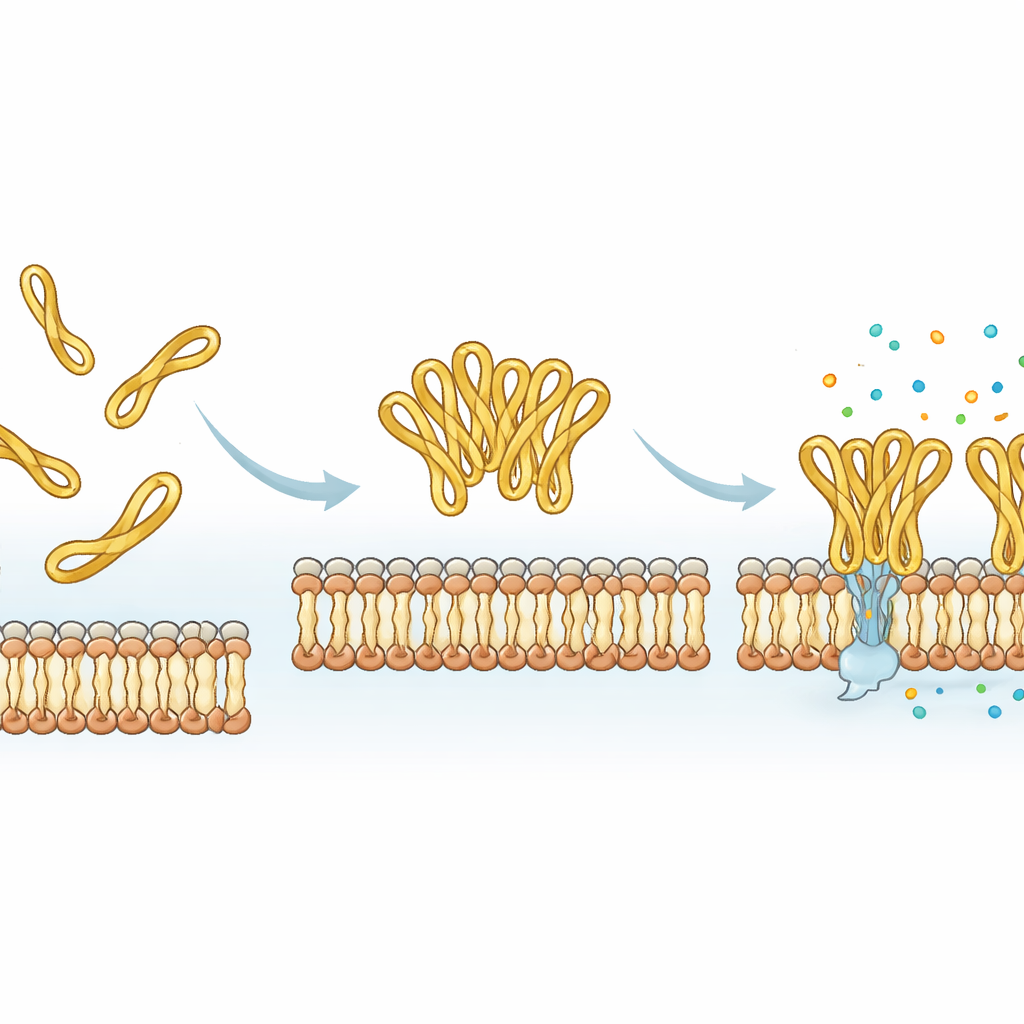
ペプチド医薬を調整するための内蔵ダイヤル
すべての証拠を総合すると、mesco-2 の末端にある小さなジスルフィドで結ばれた尾部は分子サイズのダイヤルとして働きます。それは特定の曲がった形を安定化し、ペプチドがクラスターとして協力することを促し、膜破壊を加速しますが、ヒト細胞への害を大幅に増やすことはありません。ループを除くと合成は容易になり、モデル膜への吸着量が増えることもありますが、実際の殺菌過程は遅くなり膜損傷の様相も変わります。将来こうしたペプチドに基づく抗菌様医薬品を設計する際には、主要ならせんコアだけでなく、外見上些細で柔軟な末端セグメントも、ペプチドがどれだけ速く、どれほど強く、どれほど協調的に細菌を攻撃するかを制御するために意図的に調整できることを意味します。
引用: Budimir, A., Stojan, I., Primorac, K. et al. Unstructured, disulfide-bridged C-terminus in helminth α-helical antimicrobial peptides enhances and modulates their activity. Sci Rep 16, 14472 (2026). https://doi.org/10.1038/s41598-026-44795-9
キーワード: 抗菌ペプチド, 扁形動物ペプチド, ジスルフィド結合, 膜破壊, 抗生物質耐性