Clear Sky Science · ru
Неструктурированный C-конец с дисульфидным мостиком в α-спиральных антимикробных пептидах гельминтов усиливает и модулирует их активность
Почему важны крошечные молекулы паразитов
По мере роста устойчивости к антибиотикам исследователи ищут новые способы уничтожать опасные бактерии, не повреждая наши собственные клетки. Многообещающим источником являются антимикробные пептиды — короткие фрагменты белков, которые многие организмы используют как естественные антибиотики. В этом исследовании рассматривается необычный пептид из паразитического плоского червя и показано, как маленький, подвижный хвостик на одном конце, скреплённый химической связью, способен точно регулировать скорость и силу, с которой пептид убивает бактерии. Понимание этого встроенного «регулятора» может помочь учёным проектировать более умные и точные альтернативы антибиотикам.
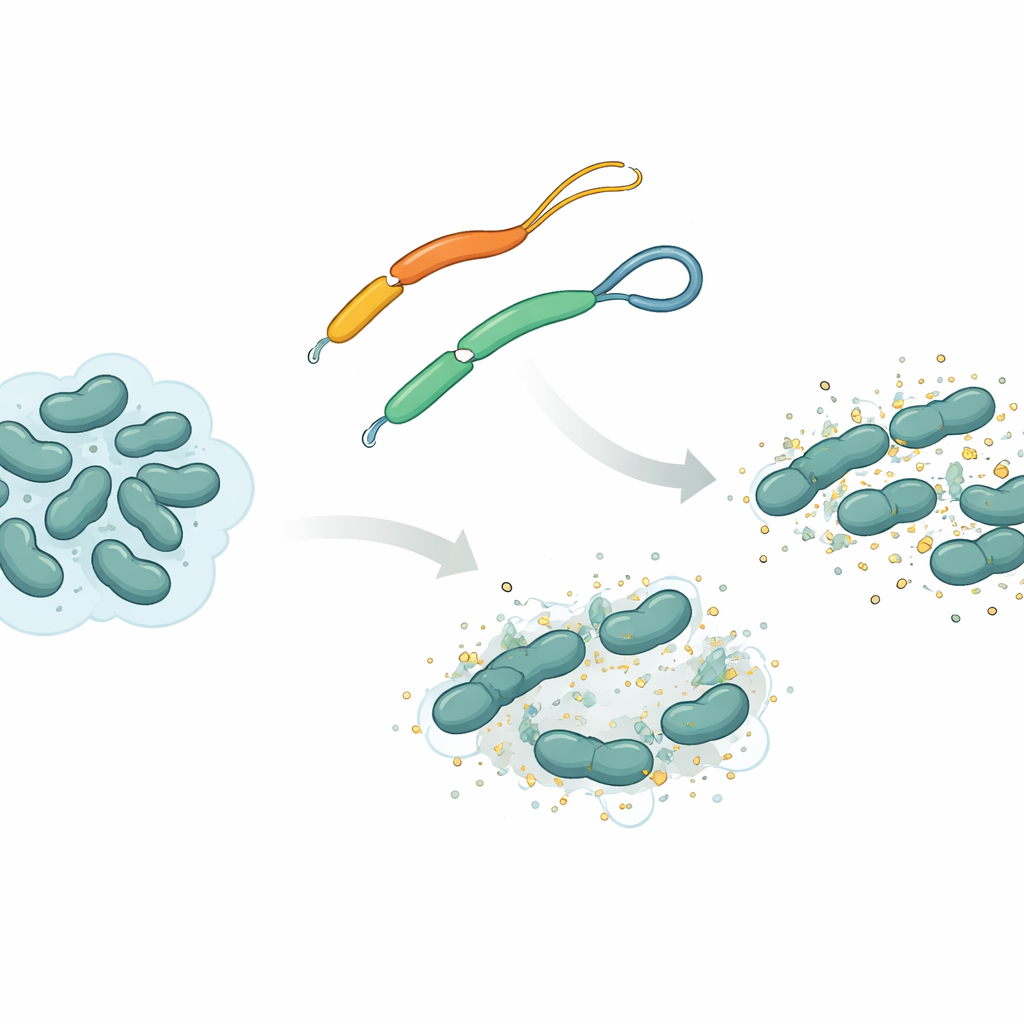
Естественное оружие плоских червей
Команда сосредоточилась на антимикробном пептиде под названием mesco-2, обнаруженном в плоском черве Mesocestoides corti. Как и у многих подобных пептидов, у mesco-2 есть жёсткая, спиралевидная «передняя» часть, взаимодействующая с бактериальными мембранами, а также более рыхлый «хвост» сзади. В этом хвосте две содержащие серу остатка связаны химической связью, известной как дисульфидный мостик, образуя крошечную петлю. Учёные сравнили mesco-2 с почти идентичной версией mesco-2A, в которой этот мостик удалён, и хвост полностью открыт. Это небольшое изменение почти не меняет общий химический состав, но изменяет подвижность пептида и его поведение при атаке на бактерии.
Скрытые закономерности в оборонительных системах паразитов
Перед тем как подробно изучать сам mesco-2, исследователи прошерстили большие базы данных предсказанных антимикробных пептидов от плоских червей и многих других организмов. Они искали специфические мотивы, где два содержащих серу остатка (цистеина) разделены несколькими другими звеньями ближе к концу молекулы. Оказалось, что шаблон «CXXXC» — та же расстановка, что и у mesco-2 — удивительно часто встречается у пептидов плоских червей и обычно располагается в гибких концевых сегментах, а не в жёстко упорядоченных областях. Компьютерные 3D-модели нескольких таких пептидов показали, что эти цистеиновые мотивы обычно находятся в подвижных хвостах, что наводит на мысль: природа целенаправленно размещает эти петли в подвижных регионах, способных модулировать поведение пептида.
Как крошечная петля формирует движение и кооперацию
С помощью молекулярно-динамических симуляций исследователи смоделировали движение mesco-2 и mesco-2A рядом с упрощённой бактериальной мембраной. Обе версии быстро присоединяются к поверхности мембраны под действием притягательных сил между положительными зарядами пептида и отрицательно заряженными липидами бактерий. Но петлевый хвост в mesco-2 помогает центральному спиральному участку согнуться в определённом месте и принять ориентацию, благоприятную для частичного внедрения в мембрану. Он также способствует тому, что несколько молекул mesco-2 собираются в мелкие кластеры, особенно если их хвосты расположены близко друг к другу, и эти сборки сохраняются при связывании с мембраной. В отличие от этого, открытый хвост у mesco-2A делает концевую часть более гибкой, он реже образует кластеры и склонен оставаться на поверхности в виде отдельных молекул, а не скоординированной группы.
От структуры к убийству бактерий
Лабораторные эксперименты подтвердили компьютерные модели. При смешивании пептидов с простыми моделями мембран обе версии изменяли форму в средах с жировыми или детергентоподобными свойствами, как ожидалось для молекул, нацеленных на мембрану. Однако mesco-2 легче приобретал регулярную спиральную структуру и принимал иное строение по сравнению с mesco-2A на отрицательно заряженных, бактериоподобных мембранах. В испытаниях против нескольких видов бактерий оба пептида проявили сильную антибактериальную активность с похожей общей эффективностью. Важные различия проявлялись ниже полностью губительной дозы: mesco-2 замедлял или останавливал рост бактерий на многие часы даже при низких концентрациях, тогда как бактерии, подвергавшиеся воздействию открытого mesco-2A, восстанавливались раньше. Временные измерения повреждения мембраны показали, что mesco-2 пробивает дыры в бактериальных мембранах значительно быстрее, тогда как mesco-2A действует медленнее, если не применяется в более высокой дозе. Высокоточное изображение выявило различные паттерны поверхностных повреждений, снова указывая на разные механизмы нарушения оболочки бактерий. Существенно, что оба пептида проявили низкую токсичность к моделям человеческих иммунных клеток на бактерицидных уровнях, что свидетельствует о благоприятном окне безопасности.
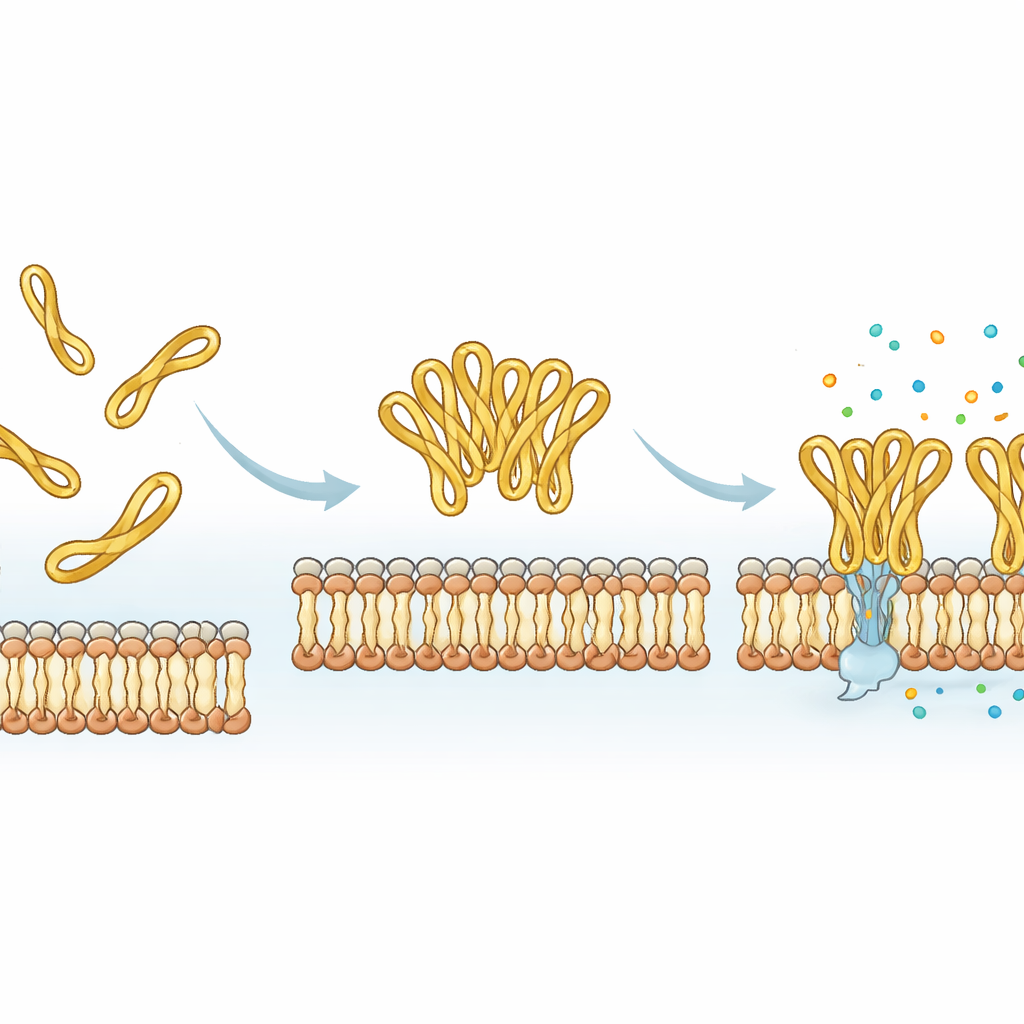
Встроенный регулятор для настройки пептидных лекарств
Сводя все данные воедино, исследование показывает, что небольшой хвост, скреплённый дисульфидом на конце mesco-2, действует как молекулярный регулятор: он стабилизирует определённую согнутую форму, способствует кооперации пептидов в кластеры и ускоряет разрушение мембраны, при этом не значительно увеличивая вред для человеческих клеток. Удаление петли упрощает синтез и даже может увеличить количество молекул, прилипших к модельной мембране, но замедляет сам процесс уничтожения и меняет характер повреждения мембраны. Для будущих антибиотико-подобных препаратов на основе таких пептидов это означает, что казалось бы незначительные гибкие концевые сегменты — а не только основной спиральный стержень — можно целенаправленно изменять, чтобы контролировать скорость, силу и кооперативность атаки пептида на бактерии.
Цитирование: Budimir, A., Stojan, I., Primorac, K. et al. Unstructured, disulfide-bridged C-terminus in helminth α-helical antimicrobial peptides enhances and modulates their activity. Sci Rep 16, 14472 (2026). https://doi.org/10.1038/s41598-026-44795-9
Ключевые слова: антимикробные пептиды, пептиды плоских червей, дисульфидный мостик, разрушение мембраны, антибиотикорезистентность