Clear Sky Science · es
Un extremo C no estructurado y puenteado por un disulfuro en péptidos antimicrobianos α‑hélice de helmintos potencia y modula su actividad
Por qué importan las moléculas diminutas de parásitos
A medida que aumenta la resistencia a los antibióticos, los investigadores buscan nuevas formas de eliminar bacterias peligrosas sin dañar nuestras propias células. Una fuente prometedora son los péptidos antimicrobianos: fragmentos cortos de proteínas que muchos organismos usan como antibióticos naturales. Este estudio examina un péptido inusual de un gusano parásito y muestra cómo una pequeña cola floja en un extremo, unida por un enlace químico, puede afinar la rapidez y la fuerza con que el péptido mata bacterias. Entender este regulador incorporado podría ayudar a los científicos a diseñar alternativas antibióticas más inteligentes y precisas.
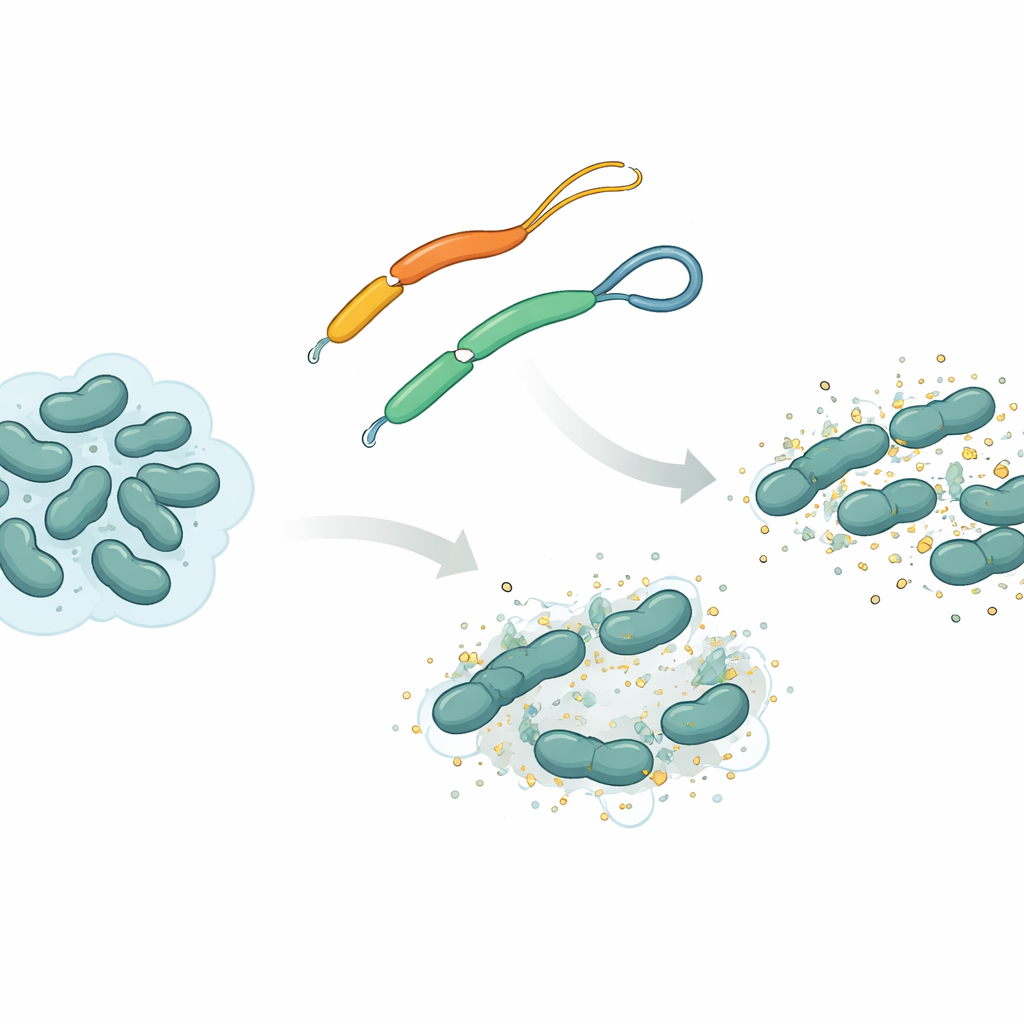
Un arma natural de los platelmintos
El equipo se centró en un péptido antimicrobiano llamado mesco‑2, encontrado en el platelminto Mesocestoides corti. Como muchos de estos péptidos, mesco‑2 tiene una sección «delantera» rígida en forma de espiral que interactúa con las membranas bacterianas, además de una «cola» más suelta en la parte posterior. En esa cola, dos bloques con azufre están enlazados por un lazo químico conocido como puente disulfuro, formando un pequeño bucle. Los investigadores compararon mesco‑2 con una versión casi idéntica, mesco‑2A, en la que ese puente se elimina y la cola queda totalmente abierta. Este pequeño cambio no altera mucho la composición química global, pero modifica cómo puede moverse el péptido y cómo se comporta al atacar bacterias.
Patrones ocultos en las defensas de los parásitos
Antes de centrarse en mesco‑2, los científicos buscaron en grandes bases de datos de péptidos antimicrobianos predichos de platelmintos y de muchos otros organismos. Buscaron patrones específicos donde dos unidades que contienen azufre (cisteínas) están separadas por unos pocos residuos cerca del extremo de la molécula. Encontraron que el patrón «CXXXC»—el mismo espaciado que en mesco‑2—es sorprendentemente común en péptidos de platelmintos y a menudo se sitúa en segmentos terminales flexibles en lugar de en regiones bien ordenadas. Modelos 3D generados por ordenador de varios de estos péptidos mostraron que estos motivos ricos en cisteína suelen ubicarse en colas flojas, lo que sugiere que la naturaleza coloca deliberadamente estos lazos en regiones móviles que pueden modular el comportamiento del péptido.
Cómo un pequeño lazo condiciona el movimiento y el trabajo en equipo
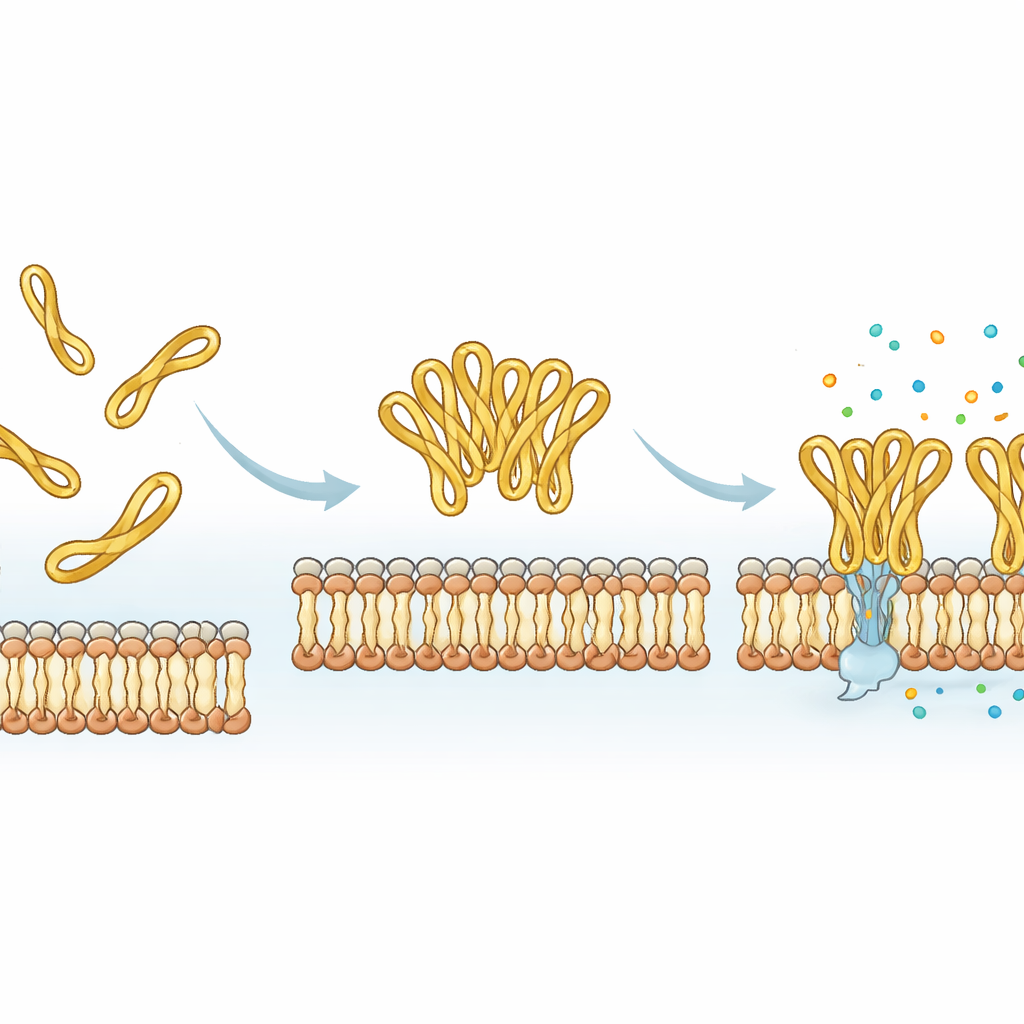
Mediante simulaciones de dinámica molecular, los investigadores modelaron cómo se mueven mesco‑2 y mesco‑2A cerca de una membrana bacteriana simplificada. Ambas versiones se adhieren rápidamente a la superficie de la membrana, impulsadas por fuerzas atractivas entre cargas positivas del péptido y las cargas negativas de los lípidos bacterianos. Pero la cola anudada en mesco‑2 ayuda a que la región espiral central se doble en un punto específico y adopte una orientación que favorece la inserción parcial en la membrana. También fomenta que varias moléculas de mesco‑2 se agrupen en pequeños cúmulos, especialmente cuando sus colas están próximas, y estos ensamblajes permanecen unidos mientras se unen a la membrana. En contraste, la mesco‑2A de cola abierta es más flexible estructuralmente en su extremo, no se agrupa tan fácilmente y tiende a permanecer más en la superficie como moléculas individuales en lugar de actuar como un conjunto coordinado.
De la estructura a la muerte bacteriana
Los experimentos de laboratorio apoyaron los modelos por ordenador. Cuando los péptidos se mezclaron con miméticos de membrana sencillos, ambos cambiaron de forma en entornos oleosos o tipo detergente, como es de esperar en moléculas que atacan membranas. Sin embargo, mesco‑2 adquirió estructura helicoidal regular más fácilmente y adoptó una conformación distinta a la de mesco‑2A en membranas cargadas negativamente, semejantes a las bacterianas. En pruebas contra varias especies bacterianas, ambos péptidos mostraron efectos antibacterianos fuertes con potencias globales similares. Las diferencias importantes aparecieron por debajo de la dosis letal completa. Mesco‑2 ralentizó o detuvo el crecimiento bacteriano durante muchas horas incluso a niveles bajos, mientras que las bacterias expuestas a la mesco‑2A de cola abierta se recuperaron antes. Mediciones temporales del daño membrana mostraron que mesco‑2 perfora las membranas bacterianas mucho más rápido, mientras que mesco‑2A actúa más despacio salvo en dosis más altas. Imágenes de alta resolución revelaron patrones distintos de daño en la superficie, lo que sugiere diferentes modos en que las dos versiones alteran el envoltorio bacteriano. De forma crucial, ambos péptidos mostraron bajo daño en modelos de células inmunitarias humanas a niveles bactericidas, lo que indica un margen de seguridad favorable.
Un control integrado para ajustar fármacos peptídicos
Al reunir todas las evidencias, el estudio muestra que la pequeña cola unida por disulfuro en el extremo de mesco‑2 actúa como un mando molecular: estabiliza una forma doblada particular, fomenta que los péptidos trabajen cooperativamente en racimos y acelera la disrupción de la membrana, todo ello sin aumentar mucho el daño a las células humanas. Eliminar el lazo facilita la síntesis e incluso puede aumentar cuántas moléculas se adhieren a una membrana modelo, pero ralentiza el proceso de muerte real y altera el modo en que se daña la membrana. Para futuros fármacos tipo antibiótico basados en tales péptidos, esto significa que segmentos terminales aparentemente menores y flexibles—y no solo el núcleo helicoidal principal—pueden ajustarse deliberadamente para controlar la rapidez, la intensidad y la cooperación con que un péptido ataca a las bacterias.
Cita: Budimir, A., Stojan, I., Primorac, K. et al. Unstructured, disulfide-bridged C-terminus in helminth α-helical antimicrobial peptides enhances and modulates their activity. Sci Rep 16, 14472 (2026). https://doi.org/10.1038/s41598-026-44795-9
Palabras clave: péptidos antimicrobianos, péptidos de platelmintos, puente disulfuro, ruptura de membranas, resistencia a antibióticos