Clear Sky Science · it
Una C-terminale non strutturata, con ponte disolfuro, nei peptidi antimicrobici α-elicoidali degli elminti ne aumenta e ne modula l’attività
Perché contano le piccole molecole dei parassiti
Con l’aumento della resistenza agli antibiotici, i ricercatori cercano nuovi modi per uccidere batteri pericolosi senza danneggiare le nostre cellule. Una fonte promettente sono i peptidi antimicrobici—brevi frammenti proteici che molti organismi usano come antibiotici naturali. Questo studio esamina un peptide insolito proveniente da un platelminto parassita e mostra come una piccola coda flessibile a una estremità, legata da un legame chimico, possa affinare la rapidità e l’intensità con cui il peptide uccide i batteri. Capire questa manopola di controllo integrata potrebbe aiutare gli scienziati a progettare alternative agli antibiotici più intelligenti e precise.
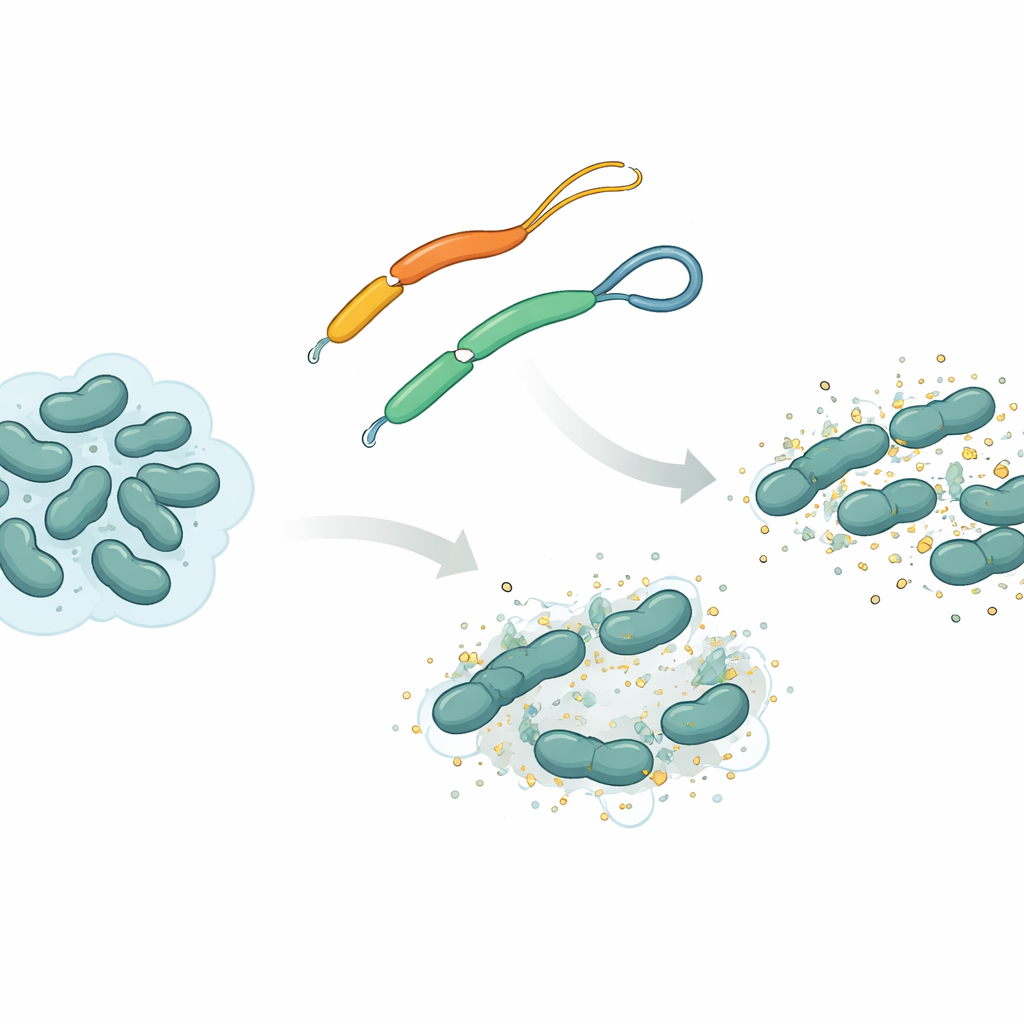
Un’arma naturale dai platelminti
Il gruppo si è concentrato su un peptide antimicrobico chiamato mesco‑2, reperito nel platelminto Mesocestoides corti. Come molti peptidi del genere, mesco‑2 ha una sezione «anteriore» rigida a spirale che interagisce con le membrane batteriche, oltre a una «coda» più lassa nella parte posteriore. In questa coda, due unità contenenti zolfo sono collegate da un legame chimico noto come ponte disolfuro, formando un piccolo anello. I ricercatori hanno confrontato mesco‑2 con una versione quasi identica, mesco‑2A, nella quale quel ponte è rimosso e la coda è completamente aperta. Questa piccola modifica non altera molto la composizione chimica complessiva, ma cambia il modo in cui il peptide può muoversi e il suo comportamento durante l’attacco ai batteri.
Pattern nascosti nelle difese dei parassiti
Prima di concentrarsi su mesco‑2, gli scienziati hanno cercato in grandi database di peptidi antimicrobici predetti da platelminti e da molti altri organismi. Hanno cercato motivi specifici in cui due unità contenenti zolfo (cisteine) sono separate da alcuni altri residui vicino alla fine della molecola. Hanno trovato che il motivo «CXXXC»—la stessa spaziatura presente in mesco‑2—è sorprendentemente comune nei peptidi dei platelminti e spesso si trova in segmenti terminali flessibili piuttosto che in regioni ben ordinate. Modelli 3D generati al computer di diversi di questi peptidi hanno mostrato che questi motivi ricchi di cisteine generalmente si collocano in code mobili, suggerendo che la natura posizioni deliberatamente questi anelli in regioni mobili che possono modulare il comportamento del peptide.
Come un piccolo anello plasma il movimento e la collaborazione
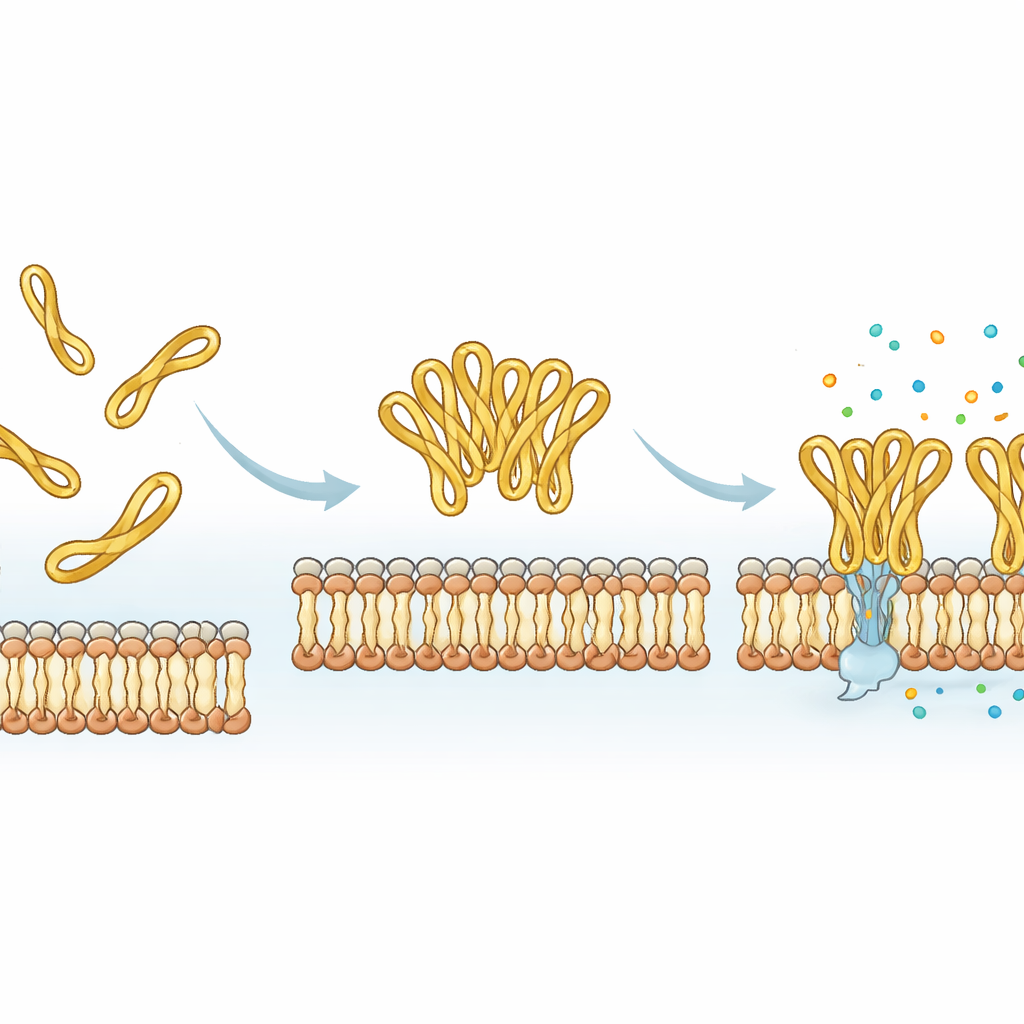
Usando simulazioni di dinamica molecolare, i ricercatori hanno modellato come mesco‑2 e mesco‑2A si muovono vicino a una membrana batterica semplificata. Entrambe le versioni si agganciano rapidamente alla superficie della membrana, spinte da forze attrattive tra cariche positive sul peptide e cariche negative sui lipidi batterici. Ma la coda ad anello di mesco‑2 aiuta la regione centrale a spirale a piegarsi in un punto specifico e ad adottare un’orientazione che favorisce un’inserzione parziale nella membrana. Promuove inoltre l’aggregazione di più molecole di mesco‑2 in piccoli ammassi, specialmente quando le code partono vicine, e questi assemblaggi rimangono coesi mentre si legano alla membrana. Al contrario, la mesco‑2A con coda aperta è più flessibile nella parte terminale, si aggrega meno facilmente e tende a rimanere più in superficie come molecole singole piuttosto che agire in gruppo coordinato.
Dalla struttura all’uccisione dei batteri
Gli esperimenti di laboratorio hanno confermato i modelli al computer. Quando i peptidi sono stati mescolati con semplici mimetici di membrana, entrambi hanno cambiato conformazione in ambienti oleosi o simili a detergenti, come ci si aspetta per molecole che prendono di mira le membrane. Tuttavia, mesco‑2 ha acquisito struttura elicoidale regolare più facilmente e ha adottato una forma diversa rispetto a mesco‑2A sulle membrane cariche negativamente, simili a quelle batteriche. Nei test contro diverse specie batteriche, entrambi i peptidi hanno mostrato forti effetti antibatterici con potenze complessive simili. Le differenze importanti sono apparse sotto la dose completamente letale. Mesco‑2 ha rallentato o bloccato la crescita batterica per molte ore anche a livelli bassi, mentre i batteri esposti a mesco‑2A a coda aperta si sono ripresi prima. Misurazioni temporali del danno alla membrana hanno mostrato che mesco‑2 perfora le membrane batteriche molto più rapidamente, mentre mesco‑2A agisce più lentamente a meno che non venga usata a dosi più alte. Immagini ad alta risoluzione hanno rivelato schemi distinti di danno superficiale, suggerendo ancora diverse modalità con cui le due versioni disturbano l’involucro batterico. Crucialmente, entrambi i peptidi hanno mostrato scarsi danni ai modelli di cellule immunitarie umane a livelli battericidi, suggerendo un margine di sicurezza favorevole.
Una manopola integrata per tarare i farmaci peptidici
Mettere insieme tutte le prove, lo studio mostra che la piccola coda legata da ponte disolfuro alla fine di mesco‑2 funge da manopola molecolare: stabilizza una particolare conformazione piegata, favorisce la cooperazione tra peptidi in cluster e accelera la disgregazione della membrana, il tutto senza aumentare molto il danno alle cellule umane. Rimuovere l’anello semplifica la sintesi e può persino aumentare il numero di molecole che si legano a una membrana modello, ma rallenta il processo di uccisione reale e modifica il modo in cui la membrana viene danneggiata. Per futuri farmaci di tipo antibiotico basati su tali peptidi, questo significa che segmenti terminali apparentemente minori e flessibili—e non solo il nucleo elicoidale principale—possono essere deliberatamente modificati per controllare quanto velocemente, quanto intensamente e quanto cooperativamente un peptide attacca i batteri.
Citazione: Budimir, A., Stojan, I., Primorac, K. et al. Unstructured, disulfide-bridged C-terminus in helminth α-helical antimicrobial peptides enhances and modulates their activity. Sci Rep 16, 14472 (2026). https://doi.org/10.1038/s41598-026-44795-9
Parole chiave: peptidi antimicrobici, peptidi di platelminti, ponte disolfuro, disgregazione della membrana, resistenza agli antibiotici