Clear Sky Science · tr
Helmint α-heliksli antimikrobiyal peptitlerde yapısal olmayan, disülfid köprülü C-terminus etkinliği artırır ve düzenler
Neden küçük parazit molekülleri önemli?
Antibiyotik direnci arttıkça, araştırmacılar insan hücrelerine zarar vermeden tehlikeli bakterileri öldürmenin yeni yollarını arıyor. Ümit verici kaynaklardan biri, birçok organizmanın doğal antibiyotik olarak kullandığı kısa protein parçaları olan antimikrobiyal peptitlerdir. Bu çalışma, parazitik bir düz solucandan gelen sıra dışı bir peptidi inceliyor ve bir ucundaki küçük, esnek kuyruğun kimyasal bir bağla bir araya getirilmesinin peptidin bakterileri öldürme hızını ve şiddetini nasıl ince ayarlayabildiğini gösteriyor. Bu yerleşik kontrol düğmesini anlamak, bilim insanlarının daha akıllı ve daha hassas antibiyotik alternatifleri tasarlamasına yardımcı olabilir.
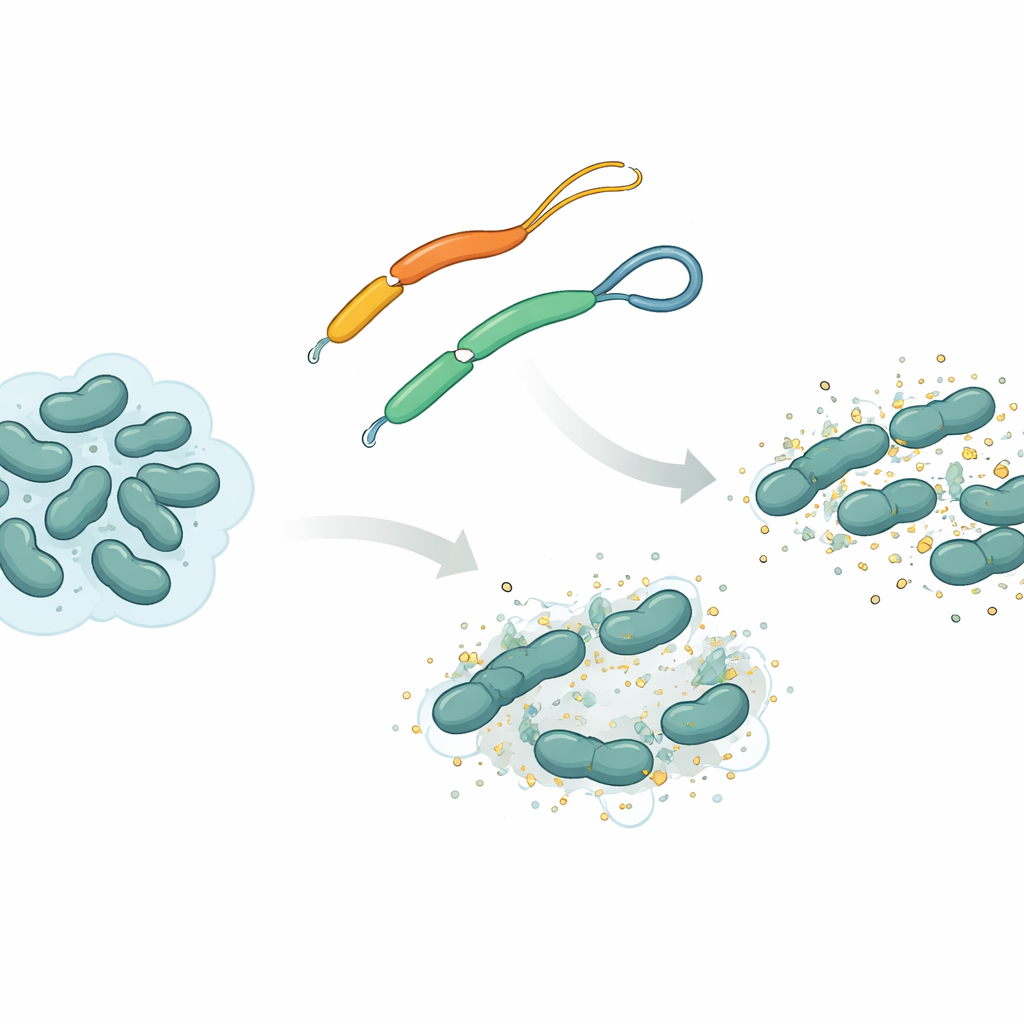
Düz solucanlardan gelen doğal bir silah
Ekip, Mesocestoides corti adlı düz solucanda bulunan mesco-2 adı verilen bir antimikrobiyal peptide odaklandı. Pek çok benzer peptitte olduğu gibi mesco-2 de bakteriyel zarlarla etkileşen sert, sarmal biçimli bir “ön” bölgeye ve daha gevşek bir “kuyruğa” sahiptir. Bu kuyrukta iki kükürt içeren yapı bir disülfid köprüsü adı verilen kimyasal bir bağla bağlanarak küçük bir halka oluşturur. Araştırmacılar, bu köprünün çıkarıldığı ve kuyruğun tamamen açık olduğu neredeyse özdeş bir versiyon olan mesco-2A ile mesco-2’yi karşılaştırdı. Bu küçük değişiklik genel kimyasal bileşimi çok değiştirmiyor, ancak peptidin hareket etme biçimini ve bakterilere saldırırken nasıl davrandığını değiştiriyor.
Parazit savunmalarında gizli kalıplar
Mesco-2’ye ayrıntılı bakmadan önce bilim insanları, düz solucanlardan ve birçok diğer organizmadan tahmin edilen antimikrobiyal peptitlerin bulunduğu büyük veritabanlarını taradı. Molekülün ucuna yakın yerde iki kükürt içeren ünitenin ( sisteinlerin) birkaç başka yapı elemanı ile ayrıldığı özgün düzenleri aradılar. Mesco-2’dekiyle aynı aralığa sahip olan "CXXXC" deseni düz solucan peptitlerinde şaşırtıcı derecede yaygındı ve genellikle iyi düzenlenmiş bölgeler yerine esnek uç segmentlerde bulunuyordu. Birkaç böyle peptidin bilgisayar tarafından oluşturulmuş 3B modelleri, bu sistein açısından zengin motiflerin genellikle oynak kuyruklarda yer aldığını gösterdi; bu da doğanın bu halkaları peptidin davranışını ayarlayabilen hareketli bölgelere kasıtlı olarak yerleştirdiğini düşündürüyor.
Mini bir halka hareketi ve işbirliğini nasıl şekillendirir
Moleküler dinamik simülasyonlar kullanarak araştırmacılar, mesco-2 ve mesco-2A’nın basitleştirilmiş bir bakteriyel zar yakınında nasıl hareket ettiğini modelledi. Her iki versiyon da pozitif yüklerin peptid üzerinde ve bakteriyel lipitlerin negatif yükleri arasındaki çekici kuvvetlerle yönlendirilerek hızla zar yüzeyine tutunuyor. Ancak mesco-2’deki halka şeklindeki kuyruk, merkezi sarmal bölgenin belirli bir noktada bükülmesine ve zar içine kısmi yerleşmeyi destekleyen bir konum almasına yardımcı oluyor. Ayrıca, kuyrukları birbirine yakın başladığında birkaç mesco-2 molekülünün küçük kümeler halinde toplanmasını teşvik ediyor ve bu yapılar zarla bağlandıkça bir arada kalıyor. Buna karşılık, açık kuyruklu mesco-2A uçta daha yapısal esnekliğe sahip, bu tür kümelenmeye daha az eğilimli ve koordineli bir grup yerine bireysel moleküller olarak daha çok yüzeyde kalma eğiliminde.
Yapıdan bakteriyel öldürmeye
Laboratuvar deneyleri bilgisayar modellerini destekledi. Peptitler basit zar taklitleriyle karıştırıldığında, her ikisi de yağlı veya deterjan benzeri ortamlarda zar hedefleyen moleküller için beklendiği gibi şekil değiştirdi. Ancak mesco-2, düzenli sarmal yapıyı daha kolay kazandı ve negatif yüklü, bakteri benzeri zarlar üzerinde mesco-2A’dan farklı bir yapı benimsedi. Birkaç bakteri türüne karşı yapılan testlerde her iki peptit de benzer genel etkinlikte güçlü antibakteriyel etki gösterdi. Önemli farklılıklar tam öldürücü doyun altında ortaya çıktı. Mesco-2, düşük düzeylerde bile bakteriyel büyümeyi saatlerce yavaşlattı veya durdurdu; açık kuyruklu mesco-2A maruz kalan bakterilerin daha çabuk toparlanmasına yol açtı. Zaman çözünürlüklü zar hasarı ölçümleri, mesco-2’nin bakteriyel zarlarında çok daha hızlı delikler açtığını; mesco-2A’nın ise daha yavaş davrandığını, ancak daha yüksek dozlarda hızlandığını gösterdi. Yüksek çözünürlüklü görüntüleme yüzey hasarının farklı desenlerini ortaya koydu ve iki versiyonun bakteriyel zarfı rahatsız etme biçimlerinin değiştiğine işaret etti. Kritik olarak, her iki peptit de bakterisid düzeylerde insan bağışıklık hücresi modellerine düşük zarar gösterdi; bu da olumlu bir güvenlik marjına işaret ediyor.
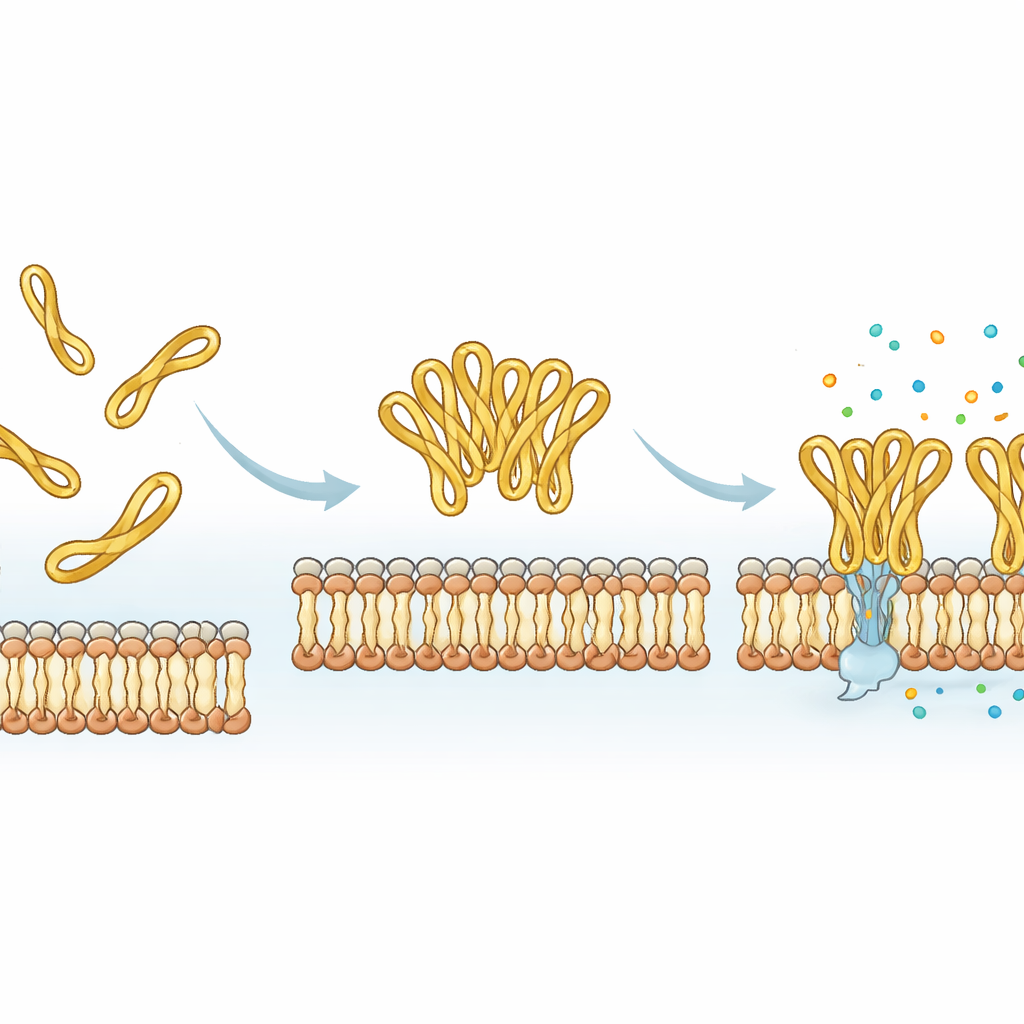
Peptit ilaçları için yerleşik bir ayar düğmesi
Tüm kanıtlar bir araya getirildiğinde çalışma, mesco-2’nin ucundaki küçük disülfid ile bağlanmış kuyruğun moleküler bir ayar düğmesi görevi gördüğünü gösteriyor: belirli bir bükülmüş şekli stabilize ediyor, peptitlerin kümeler halinde işbirliği yapmasını teşvik ediyor ve zar bozumunu hızlandırıyor; tüm bunlar insan hücrelerine büyük ölçüde daha fazla zarar vermeden gerçekleşiyor. Halkayı çıkarmak sentezi kolaylaştırıyor ve model bir zara daha fazla molekülün yapışmasını bile artırabiliyor, ancak gerçek öldürme sürecini yavaşlatıyor ve zarın hasar görme biçimini değiştiriyor. Bu tür peptitlere dayalı gelecekteki antibiyotik benzeri ilaçlar için bu, ana sarmal çekirdeğin ötesinde görünüşte önemsiz, esnek uç segmentlerin peptidin bakterilere saldırma hızını, şiddetini ve işbirliğini kasıtlı olarak kontrol etmek üzere ayarlanabileceği anlamına geliyor.
Atıf: Budimir, A., Stojan, I., Primorac, K. et al. Unstructured, disulfide-bridged C-terminus in helminth α-helical antimicrobial peptides enhances and modulates their activity. Sci Rep 16, 14472 (2026). https://doi.org/10.1038/s41598-026-44795-9
Anahtar kelimeler: antimikrobiyal peptitler, düz solucan peptitleri, disülfid köprüsü, zar bozunumu, antibiyotik direnci