Clear Sky Science · sv
Ostrukturerad, disulfidbryggad C‑terminal i helminters α‑helix‑antimikrobiella peptider ökar och styr deras aktivitet
Varför små parasitmolekyler spelar roll
När antibiotikaresistensen ökar söker forskare nya sätt att döda farliga bakterier utan att skada våra egna celler. En lovande källa är antimikrobiella peptider — korta proteinfragment som många organismer använder som naturliga antibiotika. Denna studie granskar en ovanlig peptid från en parasitisk plattmask och visar hur en liten, rörlig svans i ena änden, bunden ihop av en kemisk länk, kan finslipa hur snabbt och hur kraftfullt peptiden dödar bakterier. Att förstå denna inbyggda kontrollmöjlighet kan hjälpa forskare att designa smartare, mer precisa alternativ till antibiotika.
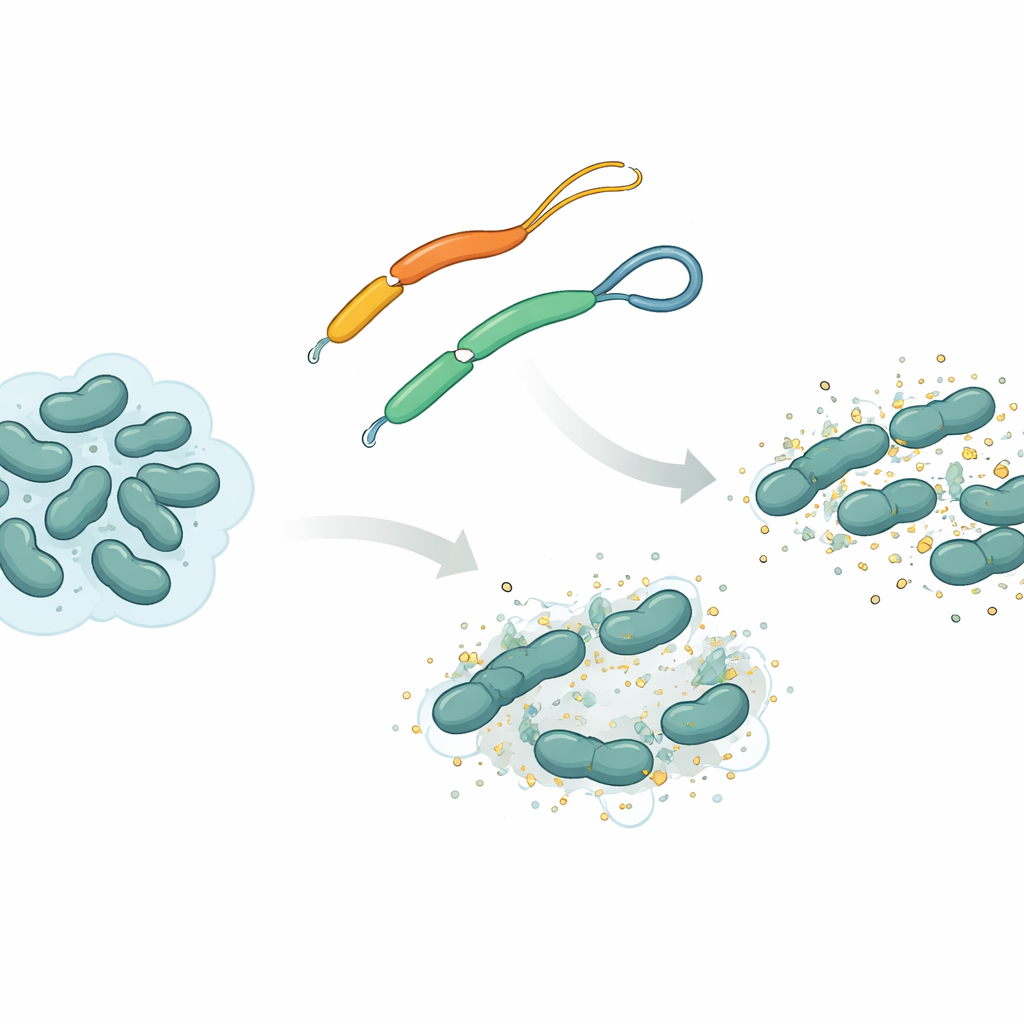
Ett naturligt vapen från plattmaskar
Teamet fokuserade på en antimikrobiell peptid kallad mesco‑2, som återfinns i plattmasken Mesocestoides corti. Liksom många sådana peptider har mesco‑2 en styv, spiralformad ”framdel” som interagerar med bakteriemembran, plus en lösare ”svans” i bakändan. I denna svans är två svavelinnehållande byggstenar sammanlänkade av en kemisk bindning, en så kallad disulfidbrygga, som bildar en liten loop. Forskarna jämförde mesco‑2 med en nästan identisk version, mesco‑2A, där den bryggan är borttagen så att svansen är helt öppen. Denna lilla förändring ändrar inte den övergripande kemiska sammansättningen mycket, men den påverkar hur peptiden kan röra sig och hur den beter sig när den anfaller bakterier.
Dolda mönster i parasitförsvar
Innan de granskade mesco‑2 närmare sökte forskarna i stora databaser med förutspådda antimikrobiella peptider från plattmaskar och många andra organismer. De letade efter specifika mönster där två svavelinnehållande enheter (cystein) är åtskilda av ett par andra byggstenar nära molekylens ände. De fann att ett "CXXXC"‑mönster — samma avstånd som i mesco‑2 — är överraskande vanligt i plattmaskpeptider och ofta sitter i flexibla ändsegment snarare än i välordnade regioner. Datorgenererade 3D‑modeller av flera sådana peptider visade att dessa cysteinrika motiv vanligtvis sitter i rörliga svansar, vilket antyder att naturen medvetet placerar dessa slingor i rörliga regioner som kan modulera peptidens beteende.
Hur en liten loop formar rörelse och samarbete
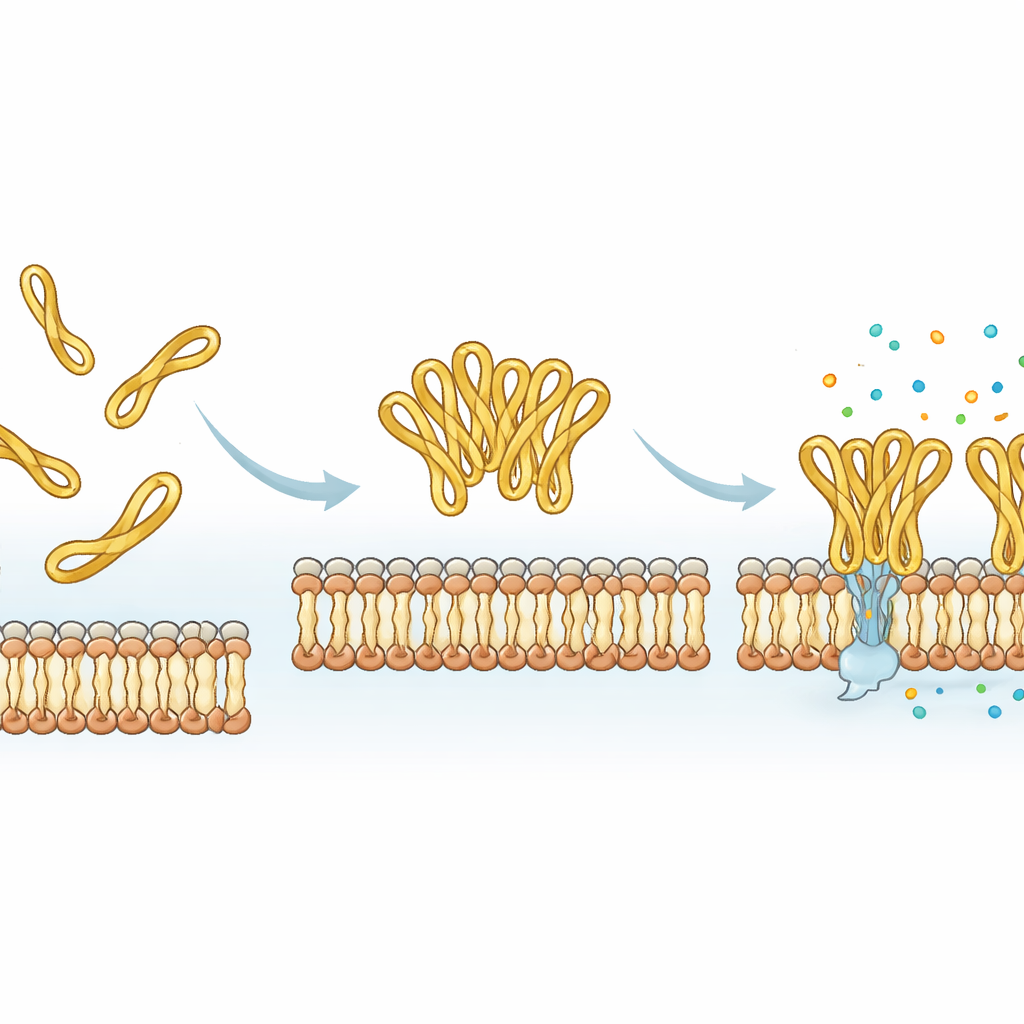
Med molekylär dynamiksimuleringar modellerade forskarna hur mesco‑2 och mesco‑2A rör sig i närheten av ett förenklat bakteriemembran. Båda varianterna fäster snabbt vid membranytan, drivet av attraktiva krafter mellan positiva laddningar på peptiden och negativa laddningar på bakterielipiderna. Men den loopade svansen i mesco‑2 hjälper den centrala spiralregionen att böja sig vid en specifik punkt och anta en orientering som favoriserar partiell insättning i membranet. Den uppmuntrar också flera mesco‑2‑molekyler att samlas i små kluster, särskilt när deras svansar börjar nära varandra, och dessa uppsättningar håller ihop medan de binder membranet. I kontrast är den öppna svansen hos mesco‑2A mer strukturellt flexibel i sin ände, klustrar sig inte lika lätt och tenderar att stanna mer på ytan som individuella molekyler snarare än som en koordinerad grupp.
Från struktur till bakteriedödande
Laboratorieexperiment stödde datorernas modeller. När peptiderna blandades med enkla membramimetika ändrade båda form i oljiga eller tvättmedelsliknande miljöer, vilket är väntat för membrantargeterande molekyler. Mesco‑2 antog dock regelbunden spiralstruktur lättare och tog en annan form än mesco‑2A på negativt laddade, bakterieliknande membran. I tester mot flera bakteriearter visade båda peptiderna starka antibakteriella effekter med liknande övergripande potens. De viktiga skillnaderna framträdde under de doser som inte fullständigt dödar. Mesco‑2 bromsade eller stoppade bakterietillväxten under många timmar även vid låga nivåer, medan bakterier exponerade för den öppna svansen mesco‑2A återhämtade sig snabbare. Tidsupplösta mätningar av membranskada visade att mesco‑2 slår hål i bakteriemembran mycket snabbare, medan mesco‑2A verkar långsammare om den inte används i högre doser. Högupplöst avbildning visade olika mönster av ytskador, vilket åter antyder skilda sätt för hur de två varianterna stör bakterieomslaget. Viktigt är att båda peptiderna visade låg skada på humana immuncellsmodeller vid bakteriedödande nivåer, vilket tyder på en fördelaktig säkerhetsmarginal.
En inbyggd ratt för att finjustera peptidläkemedel
Sammantaget visar studien att den lilla disulfidbundna svansen i slutet av mesco‑2 fungerar som en molekylär ratt: den stabiliserar en viss böjd form, främjar att peptider arbetar kooperativt i kluster och snabbar upp membranrubbo, allt utan att avsevärt öka skadan på människoceller. Att ta bort loopen gör syntesen enklare och kan till och med öka hur många molekyler som fäster vid ett modellmembran, men det saktar ner själva dödandeprocessen och förändrar hur membranet skadas. För framtida antibiotikaliknande läkemedel baserade på sådana peptider innebär detta att till synes små, flexibla ändsegment — snarare än bara den huvudsakliga spiralformen — medvetet kan justeras för att kontrollera hur snabbt, hur kraftfullt och hur kooperativt en peptid angriper bakterier.
Citering: Budimir, A., Stojan, I., Primorac, K. et al. Unstructured, disulfide-bridged C-terminus in helminth α-helical antimicrobial peptides enhances and modulates their activity. Sci Rep 16, 14472 (2026). https://doi.org/10.1038/s41598-026-44795-9
Nyckelord: antimikrobiella peptider, plattmaskpeptider, disulfidbrygga, membranrubbo, antibiotikaresistens